液相色谱-四极杆/静电场轨道阱质谱鉴定赛拉嗪在人尿中的代谢产物
崔晶晶,孙英英,沈保华,刘万卉,向 平
(1.烟台大学药学院,山东 烟台 264005;2.司法鉴定科学研究院,上海市法医学重点实验室,上海市司法鉴定专业技术服务平台,上海 200063;3.山东省威海市公安局刑事科学技术研究所,山东 威海 264200)
赛拉嗪(xylazine, C12H16N2S)是一种α2-肾上腺素受体激动剂,它通过刺激中枢神经α2-肾上腺素受体,减少中枢神经系统中去甲肾上腺素和多巴胺的释放,导致镇静、肌肉松弛和对疼痛刺激的感知减少[1],常作为动物的镇静剂、止痛药和肌肉松弛剂,又因其能产生麻醉效果,常被滥用导致中毒事故或犯罪的发生[2]。
药物辅助犯罪(drug-facilitated crime, DFC)是指在中枢神经抑制剂、兴奋剂和致幻剂等精神活性物质影响下,实施的麻醉抢劫、性犯罪等不法行为。随着网络传播和网购的盛行,药物辅助性犯罪(drug-facilitated sexual assault, DFSA)案件的数量及涉案药物种类呈上升趋势[7-8]。DFSA案件因所涉药物摄入剂量小,代谢快等是法医毒物鉴定的难点,而尿液中代谢产物检测时限长的优势在DFSA案件中发挥了重要作用[7]。赛拉嗪是近两年常出现于DFSA案件中的药物之一,但其在人体内的代谢途径以及主要代谢物的研究资料很少。
目前,代谢物确证研究多采用液相色谱-质谱法[9-10]、气相色谱-质谱法[11-12]、高效液相色谱-高分辨质谱法[13-14]等。液相色谱-四极杆-静电场轨道阱质谱(LC-Q-Orbitrap MS)是基于Orbitrap静电场轨道阱技术测定原理的液质联用技术,具有高分辨率、高精密度、高灵敏度和动态范围宽等特点,可同时获得高质量的多级质谱图(MSn),保证分析结果的可靠性和准确性[15]。Compound Discoverver软件包含丰富的工具集,可以进行预期化合物搜索及使用碎片离子搜索阐明(FIsh)结构,将多个样品数据信息合并到一份报告中,可对研究药物的体内代谢物提供技术支持。
本研究拟采用LC-Q-Orbitrap MS法及Compound Discoverver软件对赛拉嗪阳性尿液进行筛查,并对其代谢物进行结构解析,探索赛拉嗪在人体内的代谢方式及途径。
1 实验部分
1.1 主要仪器与装置
UltiMate 3000 UHPLC 液相系统,ThermoScientificTMQ-ExactiveTM组合型四极杆Orbitrap质谱仪(LC-Q-Orbitrap MS):美国Thermo Fisher Scientific公司产品,配有电喷雾离子源(HESI-Ⅱ)及XcaliburTM3.1工作站;TDZ4-WS离心机:上海卢湘仪离心机有限公司产品;XW-80A涡旋混合器:上海医大仪器有限公司产品;Milli-Q超纯水机:美国Millipore公司产品;Minspin高速离心机:德国Eppendorf公司产品;超声波清洗器:深圳市洁盟清洗设备有限公司产品。
1.2 主要材料与试剂
甲醇、乙腈:色谱纯,美国Fisher Scientific公司产品;乙酸乙酯:分析纯,上海凌峰化学试剂有限公司产品;甲酸、乙酸铵:瑞士Fluka公司产品;实验用水:超纯水,经Mili-Q系统制备;其他试剂均为分析纯。
阳性尿液来自一例DFSA案件,受害人尿液经GC/MS分析检出赛拉嗪成分。
1.3 样品前处理
1.3.1液-液萃取法 取1.0 mL待测尿液于5 mL具塞试管中,加入2.0 mL乙酸乙酯提取溶剂,涡旋振荡2 min后,以离心半径 12 cm,3 000 r/min离心3 min。转移有机层,取上层有机溶液,加入一滴NaOH(10%)溶液,重复上述步骤。合并上层有机溶液,于40 ℃空气流下吹干,向残留物中加入100 μL甲醇复溶后,待进样分析。
1.3.2蛋白沉淀法 取100 μL待测尿样于1.5 mL离心管中,加入900 μL乙腈,涡旋振荡2 min后离心3 min,上清液转移至进样衬管,取5 μL进样分析。
1.4 实验条件
1.4.1色谱条件 Thermo Scientific Hypersil GOLD PFP色谱柱(100 mm×2.1 mm×3 μm),流动相:A为5 mmol/L乙酸铵-0.1%甲酸水溶液,B为乙腈;梯度洗脱程序:0~0.5 min(98%A),0.5~10 min(98%~2%A),10~15 min(2%A),15~20 min(98%A);进样量5.0 μL;流速400 μL/min;柱温26.7 ℃。
1.4.2质谱条件 电喷雾电离正离子模式(ESI+);喷雾电压3.5 kV;壳气、辅助加热气、碰撞气:均使用高纯氮气;探头加热器温度300 ℃;毛细管温度325 ℃;鞘气流速35 arb,辅助气流速10 arb。采用一级全扫描和自动触发二级(full scan-ddMS2)的数据采集模式。
一级扫描分辨率70 000,二级扫描分辨率17 500,全质量扫描范围m/z70~1 050,可视宽度为0.7,碰撞能量为40、60、80 eV。进样前用校正液对质谱的质量轴进行校正,质量数偏差小于5×10-6。
利用XcaliburTM3.1工作站及Compound DiscovererTM3.0软件进行数据处理。
2 结果与讨论
2.1 液-液萃取法
阳性尿液经液-液萃取法前处理后,由LC-Q-Orbitrap MS分析,其全扫描总离子流图(TIC)示于图1。赛拉嗪及各代谢产物的高分辨质谱数据列于表1。赛拉嗪的保留时间为3.96 min,准分子离子峰[M+H]+为m/z221.110 58,其MS2谱图中的碎片离子为m/z164.052 76、147.091 69、90.037 21。m/z90.037 21可作为噻嗪环的特征碎片离子。对于大多数代谢物,因其分子质量太小而不能进一步碎裂,得不到MS3谱图,所以主要利用代谢物的MS和MS2谱图进行结构解析。赛拉嗪及各代谢产物(M1~M5)的MS2谱图示于图2。通过Compound Discoverer 软件分析得到5个可疑分子离子峰。准分子离子峰[M+H]+m/z237.105 48,保留时间为3.37 min,比原准分子离子大16 u,可能是增加了1个O为代谢产物M1。M1的[M+H]+离子在MS2谱图中对应的主要碎片离子为m/z163.086 55、180.047 76,比母离子的MS2碎片离子(m/z147.091 69、164.052 76)大16 u,而m/z90.037 21没有发生改变,即噻嗪环没有开裂,进一步说明羟基化反应发生在2,6-二甲基苯胺环上,但难以确认羟基化的具体位点,故推测存在羟基化的两个同分异构体(M1-1、M1-2)。
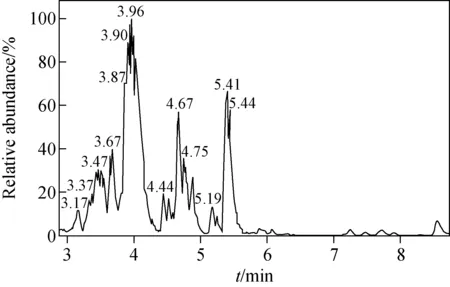
图1 样品经液-液萃取处理后的总离子流色谱图Fig.1 Total ion current chromatogram of the sampleprepared by liquid-liquid extraction
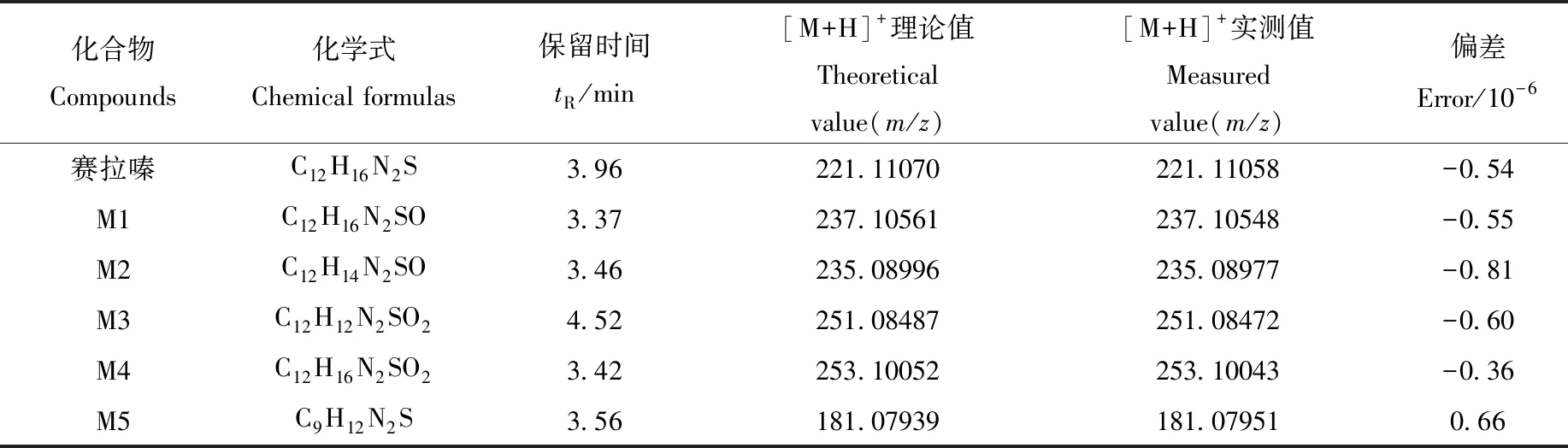
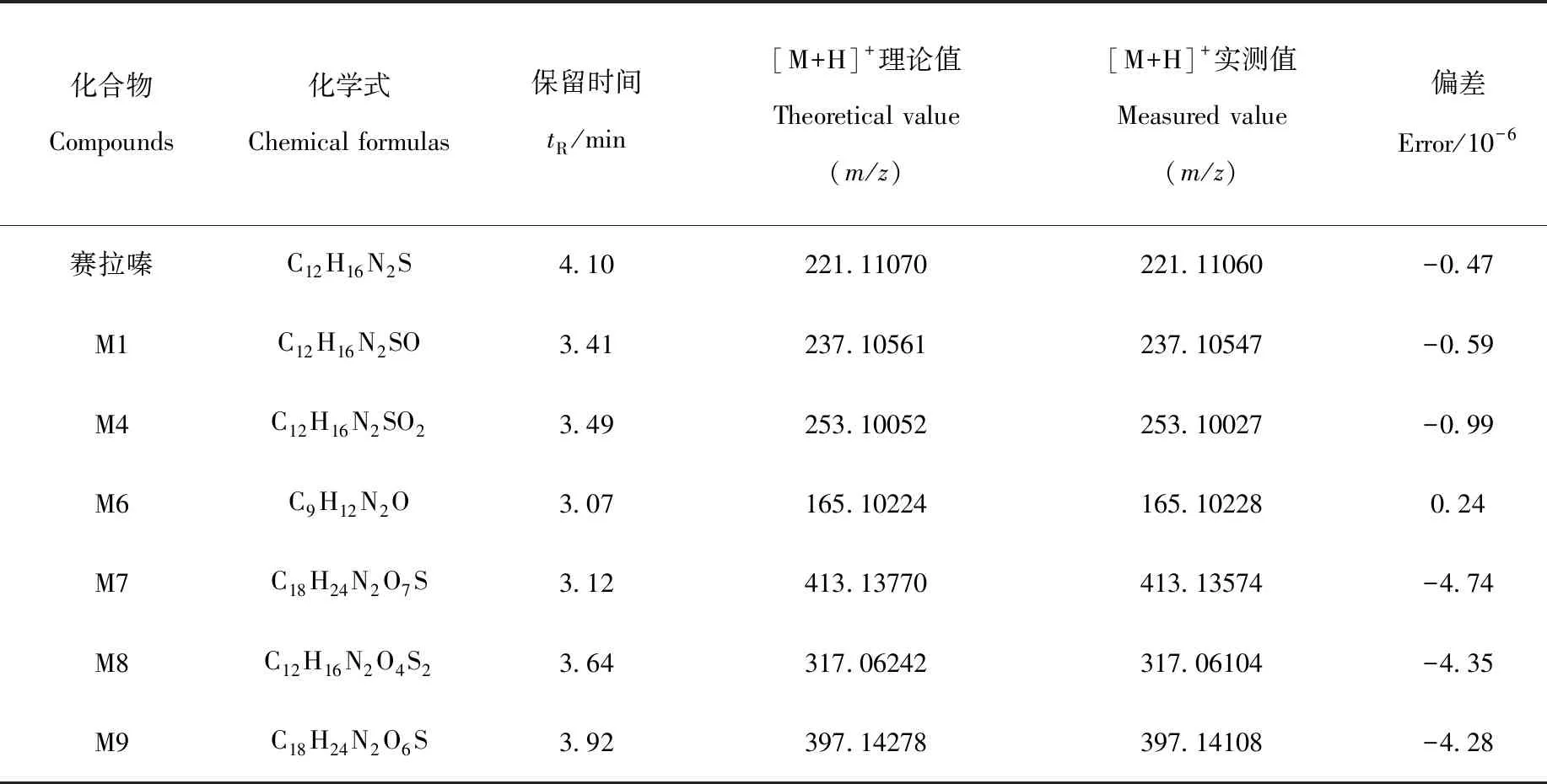
表1 赛拉嗪在人尿液中代谢产物的LC-Q-Orbitrap MS数据(液-液萃取方法)Table 1 LC-Q-Orbitrap MS data of xylazine and its metabolites in human urine(liquid-liquid extraction)

注:a.赛拉嗪;b.M2;c.M1-1;d.M1-2;e.M3-1;f.M3-2;g.M4;h.M5图2 赛拉嗪及各代谢产物MS2谱图(液液萃取法)Fig.2 MS2 spectra of xylazine and its metabolites by liquid-liquid extraction
准分子离子峰[M+H]+m/z235.089 77,保留时间为 3.46 min,比原准分子离子大14 u(+16-2),推测为赛拉嗪的氧化代谢产物M2。M2的[M+H]+离子在MS2谱图中对应的主要碎片离子为m/z181.079 51、164.052 98、136.075 82,未观察到在m/z90.037 21 处噻嗪环的特征碎片离子,表明噻嗪环发生了氧化开环。
准分子离子峰[M+H]+m/z251.084 72,保留时间为4.52 min,比原准分子离子大30 u(16+16-2),推测为赛拉嗪的氧化羟基化代谢产物M3。M3的[M+H]+离子在MS2谱图中的主要碎片离子m/z104.016 44比对应原体的碎片离子m/z90.037 21大了14 u(+16-2),表明噻嗪环发生了氧化反应。MS2谱图中m/z197.074 25、148.075 64比M2的碎片离子m/z181.079 51、132.080 7大了16 u,表明在2,6-二甲基苯胺环处发生了羟基化反应。由于难以确认发生羟基化的具体位点,故推测存在氧代羟基化的两个同分异构体(M3-1、M3-2)。
准分子离子峰[M+H]+m/z253.100 43,保留时间为3.42 min,比原准分子离子大32 u(16+16),表明存在发生二羟基化或S-氧化成砜反应的代谢产物M4。MS2谱图存在m/z147.091 67、164.052 83处的丰富碎片离子及2,6-二甲基苯胺环的特征碎片离子m/z181.079 41,排除2,6-二甲基苯胺环的羟基化反应,推断该反应发生在噻嗪环上。因未发生水的消除反应,排除了噻嗪环的二羟基化反应,因此推测M4为赛拉嗪S-氧化成砜的代谢产物。
准分子离子峰[M+H]+m/z181.079 91,保留时间为3.56 min,比原准分子离子小40 u(—C3H4),推测为赛拉嗪经N,S-脱烷基化生成N-(2,6-二甲基苯基)硫脲,为代谢产物M5。在MS2谱图中,可以观察到m/z122.096 46处的丰富碎片离子,应是赛拉嗪N-脱烷基化生成的代谢产物2,6-二甲基苯胺,m/z181.079 91可作为2,6-二甲基苯胺的前体离子存在,因其分子质量较小,未能直接检测出来。
2.2 蛋白沉淀法
由蛋白沉淀法前处理后的阳性尿液经LC-Q-Orbitrap MS进样后,出现多个色谱峰,其TIC色谱图示于图3。赛拉嗪的保留时间是4.10 min,准分子离子峰m/z221.110 60,其MS2谱图中主要特征碎片离子为m/z164.052 76、147.091 67、90.037 19,示于图4。通过Compound Discoverer 软件分析,得到7个分子离子峰。赛拉嗪及各代谢产物对应的高分辨质谱数据列于表2,其中准分子离子m/z237.105 45、253.100 27的主要碎片离子与液-液萃取法得到的代谢产物M1、M4一致,推断其结构相同。准分子离子峰m/z165.102 28,保留时间为3.07 min,与赛拉嗪相差56 u(+O—C3H4S),经Compound Discoverer软件分析为代谢产物M6,主要碎片离子为m/z148.075 82、122.096 44,推测其是由N-(2,6-二甲基苯基)硫脲分解得到的尿素结构。
准分子离子峰m/z413.135 74,保留时间为3.12 min,比原体增加了192 u,为代谢产物M7,与M1的准分子离子相比相差176 u(+C6H8O7),推测M7为M1与葡糖醛酸共轭得到的Ⅱ相代谢产物。
准分子离子峰m/z317.061 04,保留时间为3.64 min,比赛拉嗪原体增加了96 u(+SO3),为代谢产物M8,其主要碎片离子为m/z90.037 20,表明噻嗪环没有改变,m/z237.105 47与M1的准分子离子峰相同,故推断M8(M8-1/M8-2)是由M1(M1-1/M1-2)与硫酸共轭得到的Ⅱ相代谢产物。
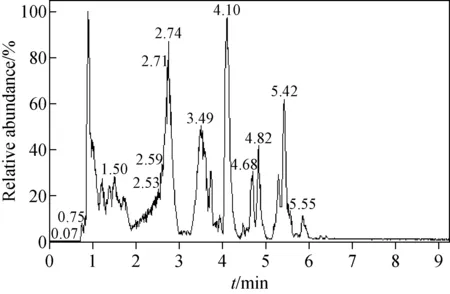
图3 经蛋白沉淀后的总离子流色谱图Fig.3 Total ion current chromatogram of the sampleprepared by protein precipitation
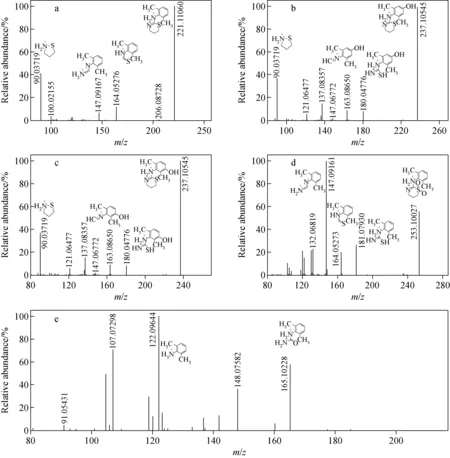
a.赛拉嗪;b.M1-1;c.M1-2;d.M4;e.M6图4 赛拉嗪及代谢产物经蛋白沉淀后得到的MS2谱图Fig.4 MS2 spectra of xylazine and its metabolites by protein precipitation
化合物Compounds化学式Chemical formulas保留时间tR/min[M+H]+理论值Theoretical value(m/z)[M+H]+实测值Measured value(m/z)偏差Error/10-6赛拉嗪C12H16N2S4.10221.11070221.11060-0.47M1C12H16N2SO3.41237.10561237.10547-0.59M4C12H16N2SO23.49253.10052253.10027-0.99M6C9H12N2O3.07165.10224165.102280.24M7C18H24N2O7S3.12413.13770413.13574-4.74M8C12H16N2O4S23.64317.06242317.06104-4.35M9C18H24N2O6S3.92397.14278397.14108-4.28
准分子离子峰m/z397.141 08,保留时间为3.92 min,比赛拉嗪原体增加了176 u(+C6H8O6),为代谢产物M9,推测为赛拉嗪发生N-葡糖醛酸结合反应得到的Ⅱ相代谢产物。
2.3 讨论
本实验利用液-液萃取法鉴定到赛拉嗪的7个代谢产物,M1-1、M1-2为羟基化产物,M2为氧化产物,M3-1、M3-2为氧代羟基化产物,M4为S-氧化产物,M5为N-(2,6-二甲基苯基)硫脲。经M5的MS2谱图推导所得的代谢产物2,6-二甲基苯胺与相关文献报道一致[9-10]。利用蛋白沉淀法鉴定到赛拉嗪的8个代谢产物,M1-1、M1-2为羟基化产物,M4、M6为S-氧化产物,M7、M8-1、M8-2、M9均为Ⅱ相代谢产物。蛋白沉淀的前处理方法能够得到更多强极性的Ⅱ相代谢产物,而液-液萃取法更容易得到水溶性强的Ⅰ相代谢产物。两种方法相互补充,能够得到更充分的数据阐明药物的体内代谢途径。
根据鉴定所得的代谢产物结构可以推断赛拉嗪及其代谢产物之间的生物转化途径,示于图5。转化途径与大鼠尿液[13]、大鼠肝微粒体[14]、马尿[12]等的研究结果相似,主要的代谢物包括羟基化产物、氧化产物及S-氧化产物等。Lavoie等[14]在大鼠肝微粒体中检测到的N-羟基化产物在人尿液中没有检测到,可能由物种不同或者浓度较低造成的。Meyer等[13]用标准尿液筛查方法(standard urine screening protocol)鉴定一例高加索人阳性案例的结果与本实验结果一致,可以认为不同人群赛拉嗪的体内代谢途径一致。经研究,建议在生物检材赛拉嗪分析时增加主要代谢物M1为目标物,以增强可靠性,延长检测时限,提供更丰富的药动学数据。含有硫脲结构的药物具有一定的毒性,赛拉嗪的代谢产物N-(2,6-二甲基苯基)硫脲的毒理学研究对于中毒后的监测具有重要的临床意义。
3 结论
本研究利用液-液萃取法和蛋白沉淀法对赛拉嗪阳性尿液进行前处理,通过LC-Q-Orbitrap MS进行解析,共鉴定到13种代谢产物。赛拉嗪在人体内发生羟基化、氧化、N-脱烷基化、S-氧化等Ⅰ相代谢反应,羟基化代谢产物可与葡萄糖醛酸及硫酸结合发生Ⅱ相代谢反应。本研究初步阐明了赛拉嗪在人体内的代谢途径和主要代谢产物。
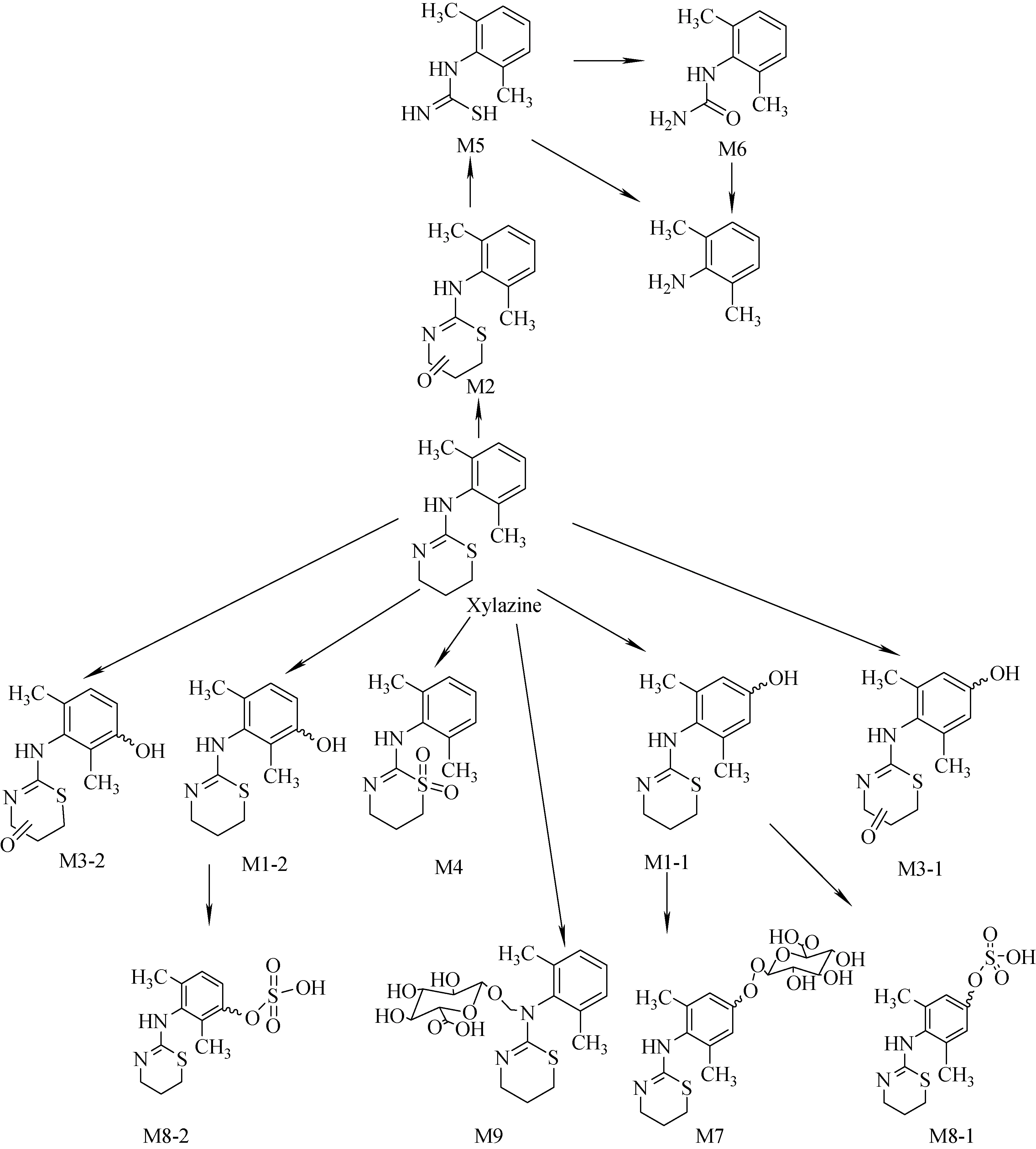
图5 赛拉嗪在人体内的代谢途径Fig.5 Proposed metabolic pathways of xylazine in humans

