六味地黄胶囊大孔吸附树脂纯化工艺的优化
吴 萍, 高 陆, 田淋淋, 任 晶, 白 冰, 徐 建∗
(1. 吉林修正药业新药开发有限公司, 吉林省中药标准化关键工程技术重点实验室, 吉林 长春 130103;2. 修正药业集团股份有限公司, 吉林 通化 134100)
六味地黄方出自钱乙《小儿药证直诀》, 由熟地黄、 牡丹皮、 酒萸肉、 山药、 泽泻、 茯苓组成,用于肾阴亏损、 头晕耳鸣、 腰膝酸软、 骨蒸潮热、盗汗遗精、 消渴[1], 六味地黄胶囊是其精制产品,服用量小, 广泛应用于临床。 在中药生产中, 工艺参数及生产过程质量控制对制剂的有效性、 均一性、 稳定性有着较大影响, 但目前关于六味地黄胶囊的研究大多涉及质量控制, 而鲜有工艺研究及生产过程质量控制的报道。 因此, 本实验以六味地黄胶囊主要药效成分莫诺苷、 马钱苷、 芍药苷[2-3]为评价指标, 对大孔吸附树脂纯化工艺进行优化[4-6], 以期保证该制剂均一稳定, 质量可靠。
1 材料
1.1 仪器 Ultimae-3000 双三元高效液相色谱仪(美国戴安公司); AE240 电子分析天平(瑞士梅特勒-托利多公司); KQ-300DE 超声波清洗器(昆山市超声仪器有限公司)。
1.2 试药 芍药苷(批号110736-201741)、 莫诺苷(批号111998-201602)、 马钱苷(批号111640-201605) 对照品均购自中国食品药品检定研究院。甲醇、 磷酸为色谱纯; 其他试剂均为分析纯; 水为纯化水。
2 方法与结果
2.1 含有量测定[7-12]
2.1.1 色谱条件 Kromasil-C18色谱柱(4.6 mm×250 mm, 5 μm); 流 动 相 甲 醇-0.1% 磷 酸(20 ∶80); 检测波长240 nm; 柱温30 ℃; 体积流量1.0 mL/min; 进样量10 μL。 色谱图见图1。
2.1.2 对照品溶液制备 精密称取莫诺苷、 马钱苷、 芍药苷对照品适量, 甲醇制成每l mL 分别含50、 30、 30 μg 上述成分的溶液, 即得。
2.1.3 供试品溶液制备 精密吸取供试液10 mL,置于具塞锥形瓶中蒸干, 精密加入25 mL 甲醇, 称定质量, 超声(250 W、 50 kHz) 30 min, 放冷,甲醇补足减失的质量, 摇匀, 滤过, 取续滤液,即得。
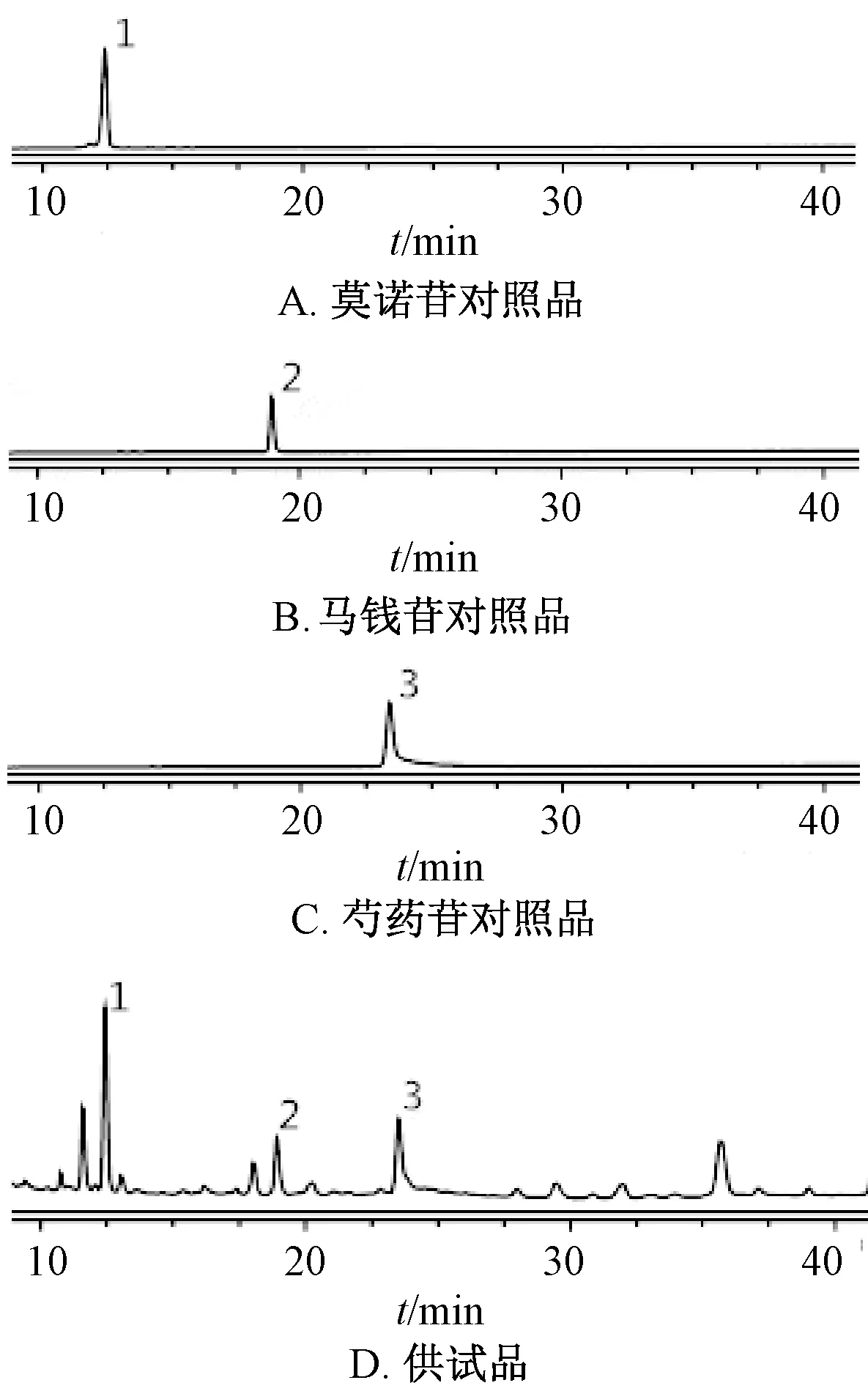
图1 各成分HPLC 色谱图Fig.1 HPLC chromatograms of various constituents
2.1.4 线性关系考察 精密吸取对照品溶液2、5、 8、 10、 15 μL, 在“2.1.1” 项色谱条件下进样测定。 以峰面积为纵坐标(Y), 进样量为横坐标(X) 进行回归, 得到莫诺苷、 马钱苷、 芍药苷回归方程分别为Y=16.872X+0.068 (r=1.000 0)、Y=26.133X+0.352 9 (r=1.000 0)、 Y=26.611X+1.271 5 (r=0.980 0), 分别在0.118 2 ~0.886 5、0.442 6~3.319 5、 0.051 ~0.382 5 μg 范围内呈良好的线性关系。
2.2 大孔吸附树脂纯化工艺优化
2.2.1 上样液前处理 称取酒萸肉(176 g) 醇提后药渣、 牡丹皮(132 g) 水蒸气蒸馏后水溶液和药渣、 熟地黄352 g、 泽泻132 g、 山药176 g, 加水煎煮3 次, 加水量依次为6、 4、 4 倍量, 每次1 h, 滤过, 滤液合并[1], 浓缩至7 000 m L (每1 mL药液含生药材0.14 g), 莫诺苷、 马钱苷、 芍药苷含有量分别为0.093、 0.057、 0.139 mg/mL。
2.2.2 泄漏曲线绘制 取湿D101 大孔吸附树脂15 g, 装入层析柱(内径1.5 cm、 高20 cm) 中,径高比1 ∶4。 另取“2.2.1” 项下水煎液200 mL上样, 体积流量1 mL/min, 每20 mL 收集1 份,共10 份, 测定每份泄漏液中芍药苷、 莫诺苷、 马钱苷含有量, 以泄漏量为纵坐标, 上样量为横坐标绘制泄漏曲线, 结果见图2。 由图可知, 上样60 mL时莫诺苷开始泄漏, 80 mL 时其他2 种成分也开始泄漏。
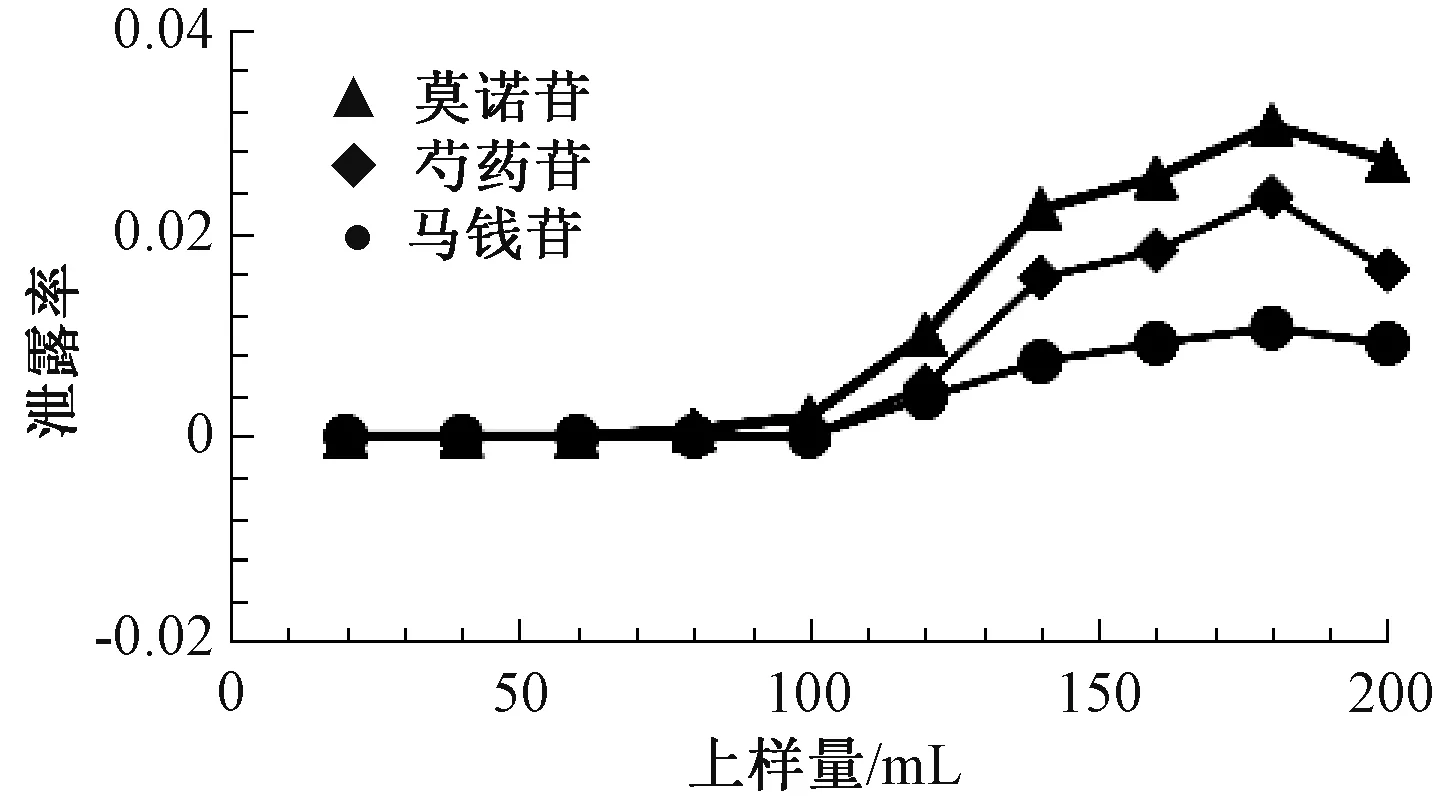
图2 各成分泄漏曲线Fig.2 Leakage curves for various constituents
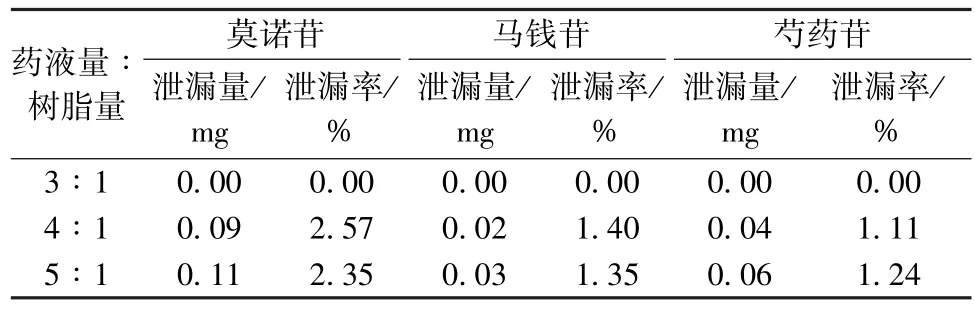
表1 药液-树脂用量比例考察结果Tab.1 Results of drug liquid-resin consumption ratio investigation
2.2.3 药液-树脂用量比例考察 取3 根相同型号的层析柱(内径1.5 cm, 高20 cm), 按径高比1 ∶4 装 柱, 湿 树 脂 量15 g, 上 样 量 75、 60、45 mL, 即药液-树脂用量比例5 ∶1、 4 ∶1、 3 ∶1,上样后纯化水洗脱, 收集水洗液, 计算泄漏量和泄漏率, 结果见表1。 由表可知, 最佳药液-树脂用量比例为3 ∶1。
2.2.4 树脂径高比考察 取3 份湿树脂, 每份15 g, 分别装入不同型号树脂柱中, 使径高比为1 ∶3、 1 ∶4、 1 ∶5, 各取45 mL 药液上样, 纯化水洗涤至流出液无色, 70%乙醇洗脱, 收集洗脱液,置于恒重的蒸发皿中蒸干, 测定固形物量及残渣中莫诺苷、 马钱苷、 芍药苷含有量, 计算收率, 公式为收率= (C1×V1/C2×V2) ×100%, 其中C1为洗脱液中莫诺苷/马钱苷/芍药苷含有量, V1为洗脱液体积, C2为水提浓缩液中莫诺苷/马钱苷/芍药苷含有量, V2为上样液体积, 结果见表2。 由表可知, 最佳树脂径高比为1 ∶4。
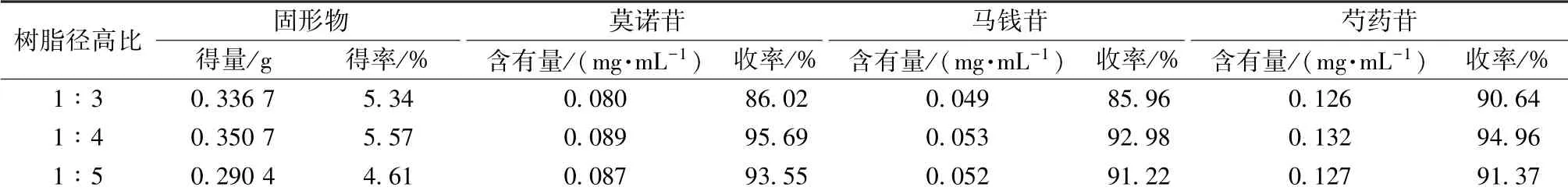
表2 树脂径高比考察结果(n=3)Tab.2 Results of resin diameter-height ratio investigation (n=3)
2.2.5 吸附体积流量考察 取3 份湿树脂, 每份15 g, 分别装入3 根相同型号的层析柱 (内径1.5 cm, 高20 cm) 中, 径高比1 ∶4, 各取45 mL药液上样, 纯化水洗涤至流出液无色, 70%乙醇洗脱, 收集洗脱液, 置于恒重蒸发皿中蒸干, 测定固形物量及残渣中莫诺苷、 马钱苷、 芍药苷含有量,按“2.2.4” 项下公式计算收率, 结果见表3。 由表可知, 最佳吸附体积流量为2 BV/h。
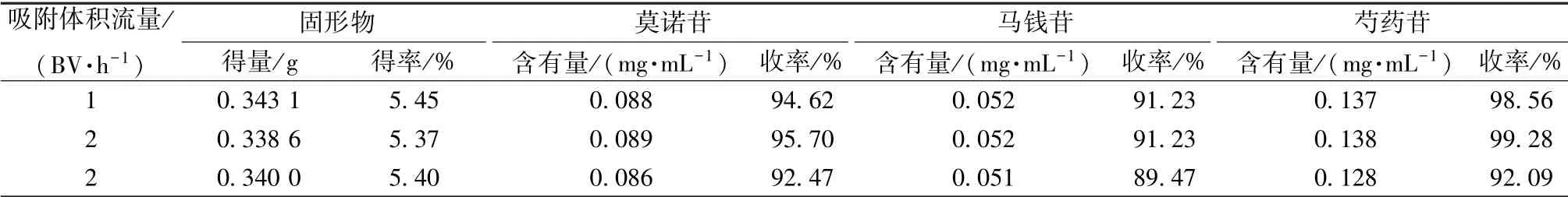
表3 吸附体积流量考察结果Tab.3 Results of adsorption volume flow rate investigation
2.2.6 洗脱体积流量考察 取3 份湿树脂, 每份15 g, 分别装入3 根相同型号的层析柱 (内径1.5 cm, 高20 cm) 中, 径高比1 ∶4, 各取45 mL药液上样, 纯化水洗涤至流出液无色, 70%乙醇洗脱, 洗脱体积流量1、 2、 3 BV/h, 收集洗脱液,置于恒重蒸发皿中蒸干, 测定固形物量及残渣中莫诺苷、 马钱苷、 芍药苷含有量, 按“2.2.4” 项下公式计算收率, 结果见表4。 由表可知, 最佳洗脱体积流量为2 BV/h。
2.2.7 洗脱剂用量考察 取3 份湿树脂, 每份约15 g, 分别装入3 根相同型号的层析柱(内径1.5 cm, 高20 cm) 中, 径高比1 ∶4, 各取75 mL药液上样, 纯化水洗涤至流出液无色, 3、 4、 5 BV 70%乙醇洗脱, 收集洗脱液, 置于恒重蒸发皿中蒸干, 测定固形物量及残渣中莫诺苷、 马钱苷、 芍药苷含有量, 按“2.2.4” 项下公式计算收率, 结果见表5。 由表可知, 最佳洗脱剂用量为5 BV。
2.3 验证试验 按优化后的大孔吸附树脂纯化条件进行3 批验证试验, 结果见表6。 由表可知, 3批纯化物中固形物得率及莫诺苷、 马钱苷、 芍药苷含有量RSD 均小于3%, 收率与工艺研究结果一致, 表明该工艺稳定可行。
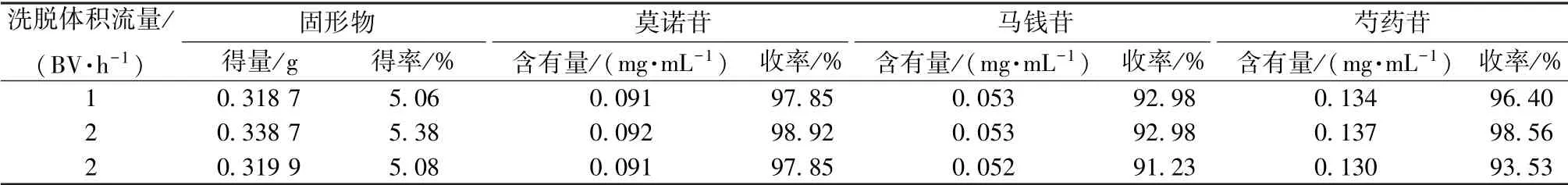
表4 洗脱体积流量考察结果Tab.4 Results of elution volume flow rate investigation
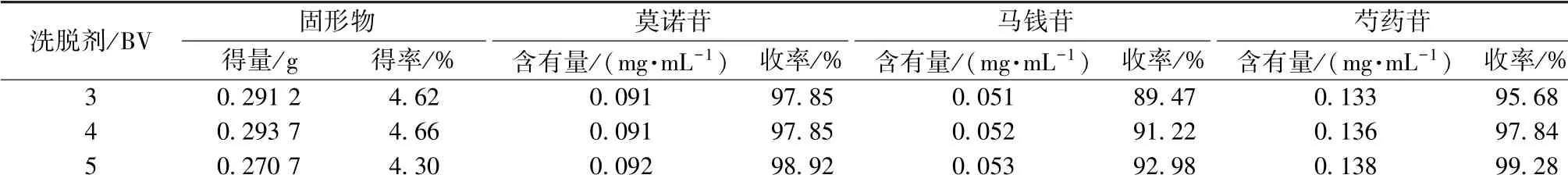
表5 洗脱剂用量考察结果Tab.5 Results of eluent consumption investigation
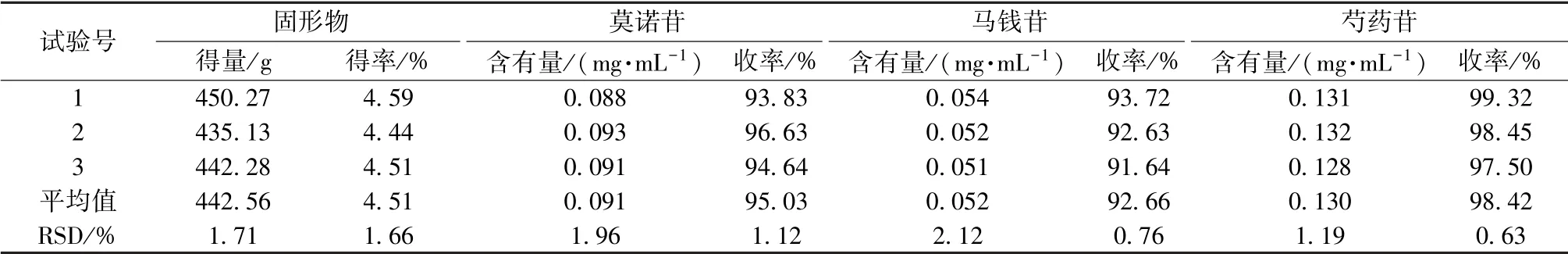
表6 验证试验结果(n=3)Tab.6 Results of verification tests (n=3)
3 讨论
中药血清药物化学研究表明, 六味地黄制剂经口服吸收入血、 在血清中含有量相对较高的药效成分主要为莫诺苷、 马钱苷、 芍药苷[2-3], 故选择三者作为检测指标。 本实验所采用的因素对大孔吸附树脂分离纯化效果均有较大影响[4-7], 其中药液-树脂用量比例考察项下的药液上样量是依据泄漏曲线测定结果而设定。
另外, 本实验取湿D101 型大孔吸附树脂反复上样、 洗脱、 再生, 发现同一份树脂再生后反复使用3 次, 莫诺苷、 芍药苷吸附量与首次洗脱液相比下降30%时, 可确定为树脂使用周期。
综上所述, 优化后的六味地黄胶囊大孔吸附树脂纯化工艺合理可行, 主要药效成分收率稳定, 可用于该制剂的生产。

