马钱子碱包合物微孔渗透泵控释片的制备
王 利, 胡瑞瑞, 郝海军
(1. 郑州澍青医学高等专科学校, 河南 郑州 450064; 2. 上海市中药研究所, 上海 201401)
马钱子碱是马前科植物马钱 Strychnos nux-vomica L. 种子的主要活性成分之一, 具有抗炎、 镇痛、 免疫抑制、 抗肿瘤等药理作用[1-3], 尤其在治疗类风湿性关节炎及镇痛方面受到广泛关注[4], 但该成分水溶性很差, 难以经胃肠道吸收进入体循环, 导致口服生物利用度很低[5], 临床应用受到一定限制。 有学者将马钱子碱制成包合物[6-7], 可大大提高该成分水溶性, 有助于促进其顺利吸收进入体循环, 提高生物利用度, 但中药活性成分制备成包合物后血药浓度波动较大[7-8], 而且马钱子碱本身具有一定毒性[9], 因此以其包合物口服给药时存在较大的安全隐患。
渗透泵缓控释制剂体外以恒速缓慢释放药物,而且体内释药过程不受胃肠道内容物、 生理因素等影响。 微孔渗透泵控释片是渗透泵缓控释制剂中的一种[10], 在包衣处方中加入一定量致孔剂, 当微孔渗透泵片进入胃肠道水环境后, 包衣膜致孔剂遇水溶解留下释药孔道, 同时片芯开始水化, 促渗聚合物发生膨胀, 从而产生了渗透压梯度, 在渗透压的作用下, 药物混悬液经释药孔道缓慢释放(图1), 该剂型无需打孔, 制备工艺得以简化。 另外,难溶性药物制备成微孔渗透泵控释片时需通过增溶技术提高难溶性药物的溶解度, 提高控释膜内外渗透压, 从而使药物顺利缓慢释放。 本实验首先制备了马钱子碱包合物, 再将其进一步与微孔渗透泵技术联合应用, 制备微孔渗透泵控释片, 以期为相关制剂革新提供参考。

图1 微孔渗透泵片释药机理Fig.1 Release mechanism of microporous osmotic pump controlled-release tablets
1 材料
1.1 仪器 Agilent 1260 型高效液相色谱仪[安捷伦科技(中国) 有限公司]; V5 型实验室粉体混匀机(广州康诺医药机械有限公司); TDP 型单冲压片机(上海第一制药机械厂); WKY-200 型小型包衣设备(沈阳明若轩制药设备有限公司); ZRS-8 型智能溶出试验仪(天津大学无线电厂); BP 210D 型电子天平[赛多利斯科学仪器(北京) 有限公司]; DZF 型真空干燥箱(北京中科仪器有限公司); HWS-12 型智能水浴锅(上海一恒科技有限公司)。
1.2 材料 马钱子碱(批号062-15, 日本和光纯药工业株式会社); 马钱子碱对照品(中国食品药品检定研究院, 批号110706-201505); 羟丙基-β-环糊精(批号20170515, 西安德立生物化工有限公司); 乳糖(批号20160517, 江苏道宁药业有限公司); 氯化钠(批号L20161124, 河北华晨药业有限公司); 醋酸纤维素(结合酸54.5% ~56.0%,国药集团化学试剂有限公司); 硬脂酸镁(批号20150617005S, 辽宁奥达制药有限公司); 聚乙二醇400 (批号72000050, 巴斯夫中国有限公司);聚氧乙烯WRS-N-10 (美国Dow 公司); 邻苯二甲酸二乙酯(批号20160316, 天津大茂试剂有限公司)。 乙腈、 甲醇为色谱纯; 其余试剂均为分析纯。
2 方法与结果
2.1 马钱子碱含有量测定
2.1.1 色谱条件 Agilent Extend C18色谱柱(250 mm×4.6 mm, 5 μm); 流动相甲醇-0.05%三乙胺(22 ∶78); 体积流量1.0 mL/min; 检测波长260 nm; 柱温35 ℃; 进样量20 μL。
2.1.2 线性关系考察 精密称取马钱子碱对照品10 mg, 置于50 mL 量瓶中, 加入约35 mL 甲醇超声溶解, 静置至室温, 甲醇定容至刻度, 得到200 μg/mL贮备液, 再进一步稀释成0.05、 0.5、1.0、 2.5、 5.0、 10 μg/mL, 在“2.1.1” 项色谱条件下进样测定。 以峰面积为纵坐标(Y), 溶液质量浓度为横坐标(X) 进行回归, 得到回归方程为Y=18.354 8X-1.992 7 (r=1.000 0), 在0.05~10 μg/mL 范围内线性关系良好。
2.1.3 供试品溶液制备
2.1.3.1 包合物 取包合物10 mg, 加入约50 mL甲醇超声30 min, 静置30 min 后甲醇-0.05%三乙胺定容至100 mL, 过0.45 μm 微孔滤膜, 即得(6.18 μg/mL)。
2.1.3.2 微孔渗透泵控释片 取微孔渗透泵控释片10 片, 研磨成细粉, 称取500 mg, 加入约50 mL甲醇超声30 min, 静置30 min 后甲醇-0.05%三乙胺定容至100 mL, 过0.45 μm 微孔滤膜,即得。
2.1.4 方法学考察 取0.05、 5.0、 10 μg/mL 马钱子碱对照品溶液, 于1 d 内在“2.1.1” 项色谱条件下进样测定6 次, 测得峰面积RSD 小于0.31%, 表明仪器精密度良好。 以羟丙基-β-环糊精溶液配制0.1、 5.0、 10 μg/mL 样品溶液, 在“2.1.1” 项色谱条件下进样测定, 测得平均回收率为98.33% ~99.24%。 精密称取9 份马钱子碱含有量已知的样品粉末, 每份约500 mg, 精密加入0.05、 5.0、 10 μg/mL 马 钱 子 碱 对 照 品 溶 液1.0 mL, 在“2.1.1” 项色谱条件下进样测定, 测得平均加样回收率为99.03%, RSD 为1.61%。 取“2.1.3” 项下供试品溶液, 于0、 1、 2、 3、 4、5 d在“2.1.1” 项色谱条件下进样测定, 测得峰面积RSD 小于1.16%, 表明溶液在5 d 内稳定性良好。 按“2.1.3” 项下方法平行制备6 份供试品溶液, 在“2.1.1” 项色谱条件下进样测定, 测得马钱子碱含有量RSD 小于1.84%, 表明该方法重复性良好。
2.2 包合物制备 取马钱子碱0.4 g, 加到20 mL无水乙醇中, 溶解后缓慢加到6 mL 羟丙基-β-环糊精溶液中 (1.0 g/mL), 50 ℃下磁力搅拌5 h,0.45 μm 微孔滤膜除去未参加包合的游离药物,-70 ℃下预冻2 d 后减压冷冻干燥, 即得, 封口袋密封保存备用。 再按照文献[7] 方法测定, 测得马钱子碱原料药溶解度为0.15 mg/mL, 制备成包合物后达到1.04 mg/mL, 提高了6.93 倍, 3 批包合物平均包封率为(98.23±0.40)%, 马钱子碱平均含有量为(61.82±0.33) mg/g。
2.3 微孔渗透泵控释片制备 取包合物200 mg(马钱子碱含有量12.36 mg)、 促渗剂(NaCl) 50 mg、 促渗聚合物(聚氧乙烯WRS-N-10) 适量、 乳糖250 mg, 等量递增法混匀, 以70%乙醇为黏合剂制备微孔渗透泵片片芯软材, 过20 目筛, 18 目筛整粒, 置于45 ℃烘箱中干燥过夜, 在干燥后的颗粒中加入1%硬脂酸镁作为润滑剂, 填充于直径8 mm 的冲模内压制片芯, 硬度45 ~65 N。 再将处方量醋酸纤维素、 聚乙二醇400、 邻苯二甲酸二乙酯溶于混合溶剂中(丙酮∶无水乙醇=95 ∶5),混匀后密封保存, 得到包衣液。 最后, 将片芯置于包衣锅中, 条件为温度35 ℃, 包衣液体积流量5 mL/min, 垂直倾角30°, 转速30 r/min, 待达到设定质量后, 将其置于40 ℃烘箱中固化, 即得。
2.4 累积释放度测定 按照2015 年版《中国药典》 四部9013 方法, 取适量微孔渗透泵控释片,以900 mL 超声后的蒸馏水为释放介质, 转速100 r/min, 温度 (37±0.5)℃, 于0、 1、 2、 4、6、 8、 10、 12 h 各取样2 mL, 补加同体积释放介质, 溶液经0.45 μm 微孔滤膜过滤(水膜), 在“2.1.1” 项色谱条件下进样测定, 计算累积释放度, 绘制相应曲线。
2.5 单因素试验 预实验发现, 微孔渗透泵控释片主要受聚氧乙烯WRS-N-10 用量、 包衣增重、 聚乙二醇400 用量、 邻苯二甲酸二乙酯用量的影响。本实验以12 h 内累积释放度及是否恒速释放为评价指标, 通过单因素试验进行考察, 为进一步正交试验优化提供参考。
2.5.1 聚氧乙烯WRS-N-10 用量 取包合物200 mg、 NaCl 50 mg、 乳糖250 mg 制备片芯, 固定包衣增重5%, PEG 400 用量30%, 邻苯二甲酸二乙酯用量20%, 考察聚氧乙烯WRS-N-10 用量10、 5、 0 mg 对体外释药行为的影响, 结果见图2。由图可知, 片芯中加入适量聚氧乙烯WRS-N-10 是有必要的。
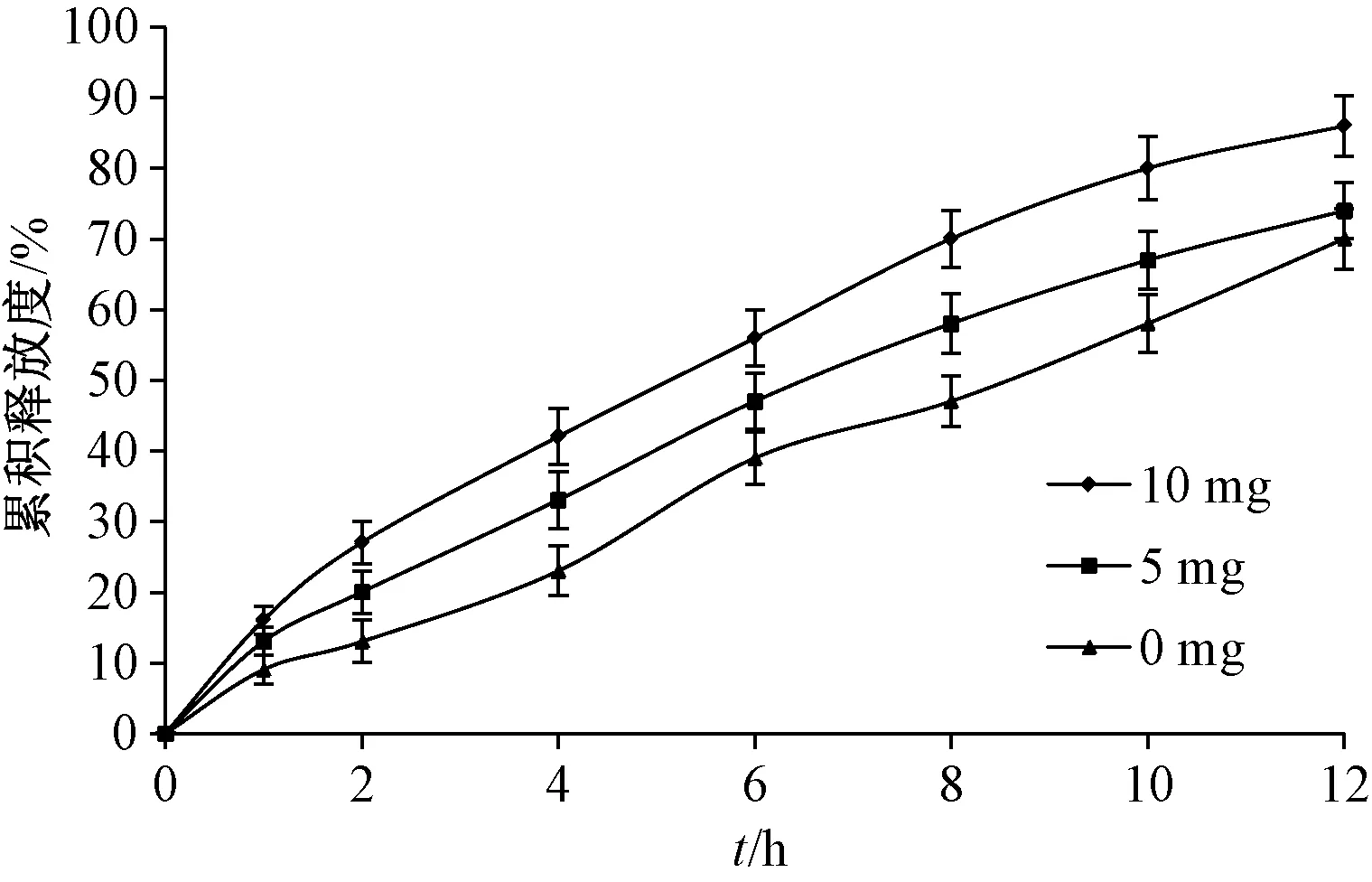
图2 聚氧乙烯WRS-N-10 用量对体外释药行为的影响Fig.2 Effect of polyoxyethylene WRS-N-10 consumption on in vitro drug release behaviors
2.5.2 包衣增重 固定片芯处方(200 mg 包合物、 50 mg NaCl、 10 mg 聚 氧 乙 烯WRS-N-10、250 mg 乳糖) 及其他条件不变, 考察包衣增重2.5%、 4.5%、 6.5%对体外释药行为的影响, 结果见图3。 由图可知, 随着包衣增重增加, 释药速率及12 h 内累积释放度逐渐下降, 虽然在2.5%时后者最高, 但药物释放非恒速, 而在4.5%时体外释药行为较理想。
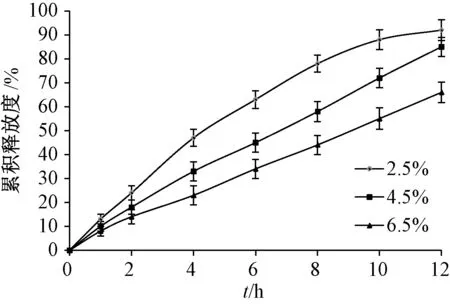
图3 包衣增重对体外释药行为的影响Fig.3 Effect of coating weight gain on in vitro drug release behaviors
2.5.3 聚乙二醇400 用量 固定片芯处方及其他条件不变, 考察聚乙二醇400 用量20%、 30%、40%对体外释药行为的影响, 结果见图4。 由图可知, 随着聚乙二醇400 用量增加, 释药速率及12 h内累积释放度逐渐增大, 其中在40% 时前期释药较快, 但后期趋缓, 故在30%时相对比较理想。

图4 聚乙二醇400 用量对体外释药行为的影响Fig.4 Effect of polyethylene glycol 400 consumption on in vitro drug release behaviors
2.5.4 邻苯二甲酸二乙酯用量 固定片芯处方及其他条件不变, 考察邻苯二甲酸二乙酯用量15%、20%、 25%对体外释药行为的影响, 结果见图5。由图可知, 随着邻苯二甲酸二乙酯用量增加, 释药速率及12 h 内累积释放度逐渐下降。
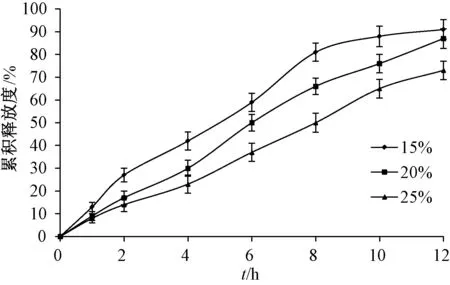
图5 邻苯二甲酸二乙酯用量对体外释药行为的影响Fig.5 Effect of diethyl phthalate consumption on in vitro drug release behaviors
2.6 正交试验 在单因素试验基础上, 选择聚氧乙烯WRS-N-10 用量(A)、 包衣增重(B)、 聚乙二醇400 用量(C)、 邻苯二甲酸二乙酯用量(D)作为影响因素, 每个因素3 个水平, 共9 次试验,考察微孔渗透泵控释片在2 h 的累积释放度(L1)以分析有无时滞或突释, 以及6 h (L2) 和12 h(L3) 的累积释放度以分析是否释放完全(权重系数设置为2), 加权法计算综合评分( | L1-0.2 | ×100×1+|L2-0.5 |×100×1+|L3-0.9 | ×100×2)。结果见表1, 方差分析见表2。
由表可知, 各因素影响程度依次为A>D>C>B, 其中因素A 有显著性差异(P<0.05)。 最优工艺为A3B1C2D3, 即聚氧乙烯WRS-N-10 用量为10 mg, 包衣增重3.5%, 聚乙二醇400 用量30%,邻苯二甲酸二乙酯用量25%, 片芯质量为510 mg。
2.7 验证试验及模型拟合 按“2.6” 项下优化工艺制备6 批微孔渗透泵控释片, 结果见图6, 可知工艺重复性良好, 处方合理, 累积释放度88.44%, 综合评分16.6。 然后, 分别采用零级、一级、 Higuchi 方程对微孔渗透泵控释片进行模型拟合, 得到方程分别为Mt/M∞=0.075 6t+0.018 9(r=0.995 6)、 ln (1-Mt/M∞) = -1 749t+0.170 7(r=0.949 2)、 Mt/M∞=0.271 9t1/2-0.129 6 (r=0.935 4), 其中Mt为t 时间累积释放度, M∞为∞时间累积释放度, Mt/M∞为t 时间累积释放率, k为常数, 以相关系数(r) 为指标进行判断, 发现零级模型拟合效果最好。

表1 试验设计及结果Tab.1 Design and results of tests
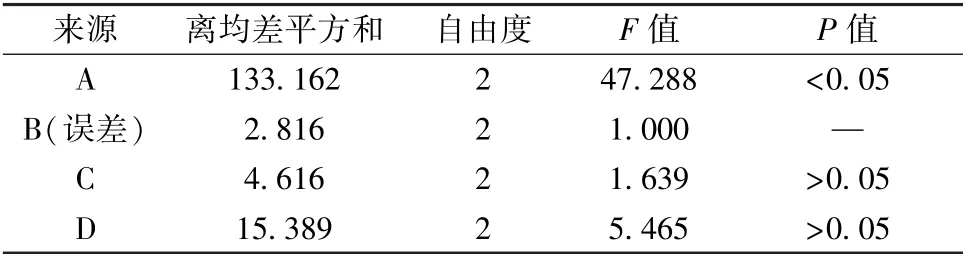
表2 方差分析Tab.2 Analysis of variance
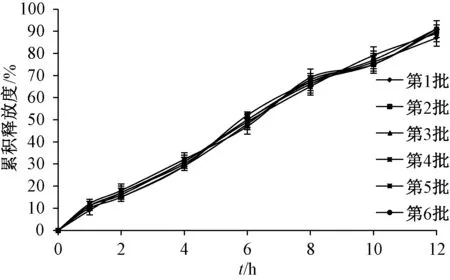
图6 微孔渗透泵控释片体外释药曲线Fig.6 In vitro drug release curves for microporous osmotic pump controlled-release tablets
2.8 体外释药行为比较 按“2.4” 项下方法测定累积释放度, 比较马钱子碱、 包合物、 微孔渗透泵控释片的体外释药行为, 结果见图7。 由图可知, 马钱子碱释放速率较低, 而制成包合物后在2 h内累积释放度达98.34%, 再制成微孔渗透泵控释片后在12 h 内恒速释药。
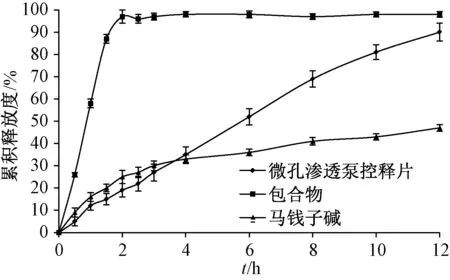
图7 不同样品体外释药行为比较Fig.7 Comparison of in vitro drug release behaviors of different samples
3 讨论
微孔渗透泵控释片是单层渗透泵控释片的一种, 主要适用于水溶性药物[10-12], 影响体外释药行为的主要因素有药物溶解度、 控释膜内外渗透压、 包衣膜通透性等。 本实验将马钱子碱制成包合物后, 其溶解度得以提高, 同时在渗透泵片片芯处方中加入一定量渗透活性物质NaCl 及助悬剂聚氧乙烯WRS-N-10 时, 可提高控释膜内外的渗透压,有助于药物顺利释放。 另外, 由于片剂在胃肠道滞留的时间一般为10~12 h, 故将马钱子碱包合物微孔渗透泵控释片的考察时间设置为12 h。
聚氧乙烯WRS-N-10 作为促渗聚合物, 可增加渗透泵控释膜内外渗透压, 是片芯处方中不可或缺的重要辅料之一。 本实验所制备的马钱子碱包合物微孔渗透泵控释片12 h 内累积释放度为88.44%,未能完全释放出去, 这可能是由于一方面聚氧乙烯WRS-N-10 在片芯中不能完全溶解, 故会吸附一定量药物, 导致其无法完全释放; 另一方面也与释药时间不够充分有关。 图7 显示, 马钱子碱原料药12 h 内累积溶出度仅为46.65%, 这与溶出介质未能达到漏槽条件有关[13]。
在马钱子碱包合物微孔渗透泵控释片制备过程中, 乳糖除了作为稀释剂、 促渗剂以增加膜内外渗透压等作用外[14-18], 还可有效防止药物与NaCl 在压片过程中形成晶状结构, 它会导致药物溶解及溶出困难[19], 优化后其重复性良好, 体外释药行为符合零级模型。 课题组前期通过统计马钱子上市品、 医院制剂等发现, 马钱子总碱(马钱子碱和士的宁) 每天总用量在2.5 ~14.9 mg 之间[20-21],而本实验制备的马钱子碱包合物微孔渗透泵控释片中马钱子碱用量为12.36 mg/片, 尽管体外释药行为达到了设计要求, 但后续还有大量研究要进行,如通过体内试验来考察其是否安全有效、 剂量是否合适等。

