肉豆蔻饮片微生物计数检查方法研究及其在霉变过程中菌落总数的测定*
杨瑞琦,王 西,陈慧荣,李佳慧,邹慧琴**,闫永红**
(1.北京中医药大学中药学院 北京 102446;2.北京三友汇智生物技术有限公司 北京 102299)
中药材的品质关系着中成药的质量和临床用药安全。近日,国家药典委员会发文道[1]药品微生物检查是药品安全性控制的重要质控项目。世界卫生组织、欧洲药典、日本药典和美国药典均对天然药制定了微生物检查方法和限度标准,并作为对这类药物的安全质控项目,如:对直接服用或炮制处理过的中药材,需氧菌总数为105cfu·g-1,霉菌和酵母菌总数为103-104cfu·g-1;需煎煮的中药材需氧菌总数106-107cfu·g-1,霉菌和酵母菌总数104-105cfu·g-1[2]。而我国关于中药饮片微生物限度的检查和限度标准的研究相对薄弱。
肉豆蔻为肉豆蔻科植物肉豆蔻(Myristica fragrans Houtt.)的干燥种仁,又名咖拘勒、豆蔻、肉果、顶头肉等,主产于马来西亚、印度尼西亚、斯里兰卡等国,我国广东、台湾、云南等地有引种栽培。其整体呈卵圆形或椭圆形,表面灰棕色或灰黄色。质坚,断面显棕黄色相杂的大理石花纹,富油性。气香浓烈,味辛。肉豆蔻味辛、温,具有温中行气、涩肠止泻的功效。近代药理学研究表明肉豆蔻挥发油可促进缺血再灌注损伤心肌的恢复[3],有心肌保护作用[4],且对行为绝望抑郁小鼠有明显抗抑郁作用等[5]。肉豆蔻中丁香酚类成分为其止泻主要成分[6,7],肉豆蔻木脂素具有明显抗炎作用[8,9],除此之外肉豆蔻亦有抗肿瘤[10,11]、抗菌[12,13]、抗氧化[14,15]等药理作用。
肉豆蔻的主要成分为挥发油和脂肪油等,营养成分丰富,极易发生霉变,是2015年版《中国药典》规定检测黄曲霉毒素限量的十九种中药之一。其在储藏过程中受到空气中霉菌孢子的污染,在适当的温度、湿度下即萌发为菌丝,分泌酵素,溶蚀药材的内部组织,使之腐坏变质,失去或降低药效,甚至产生毒素危害患者的生命安全。但是,在实验中发现肉豆蔻在不切开的情况下很难判断其是否霉变。

图1 肉豆蔻不同霉变时期样品(a:J0样品;b:J6样品;c:J13样品)
有文献报道,肉豆蔻挥发油对金黄色葡萄球菌、大肠杆菌、普通变形杆菌、沙门氏菌、蜡状芽孢杆菌、枯草芽孢杆菌共6种细菌及黄曲霉、黑曲霉等6种真菌均有抑制作用,且对细菌的抑菌活性比对真菌的抑菌活性强[16]。
本文对极易霉变又具有抑菌作用的肉豆蔻饮片进行微生物计数方法适应性验证,并考察其在不同霉变时期需氧菌、霉菌、酵母菌菌落总数,以期为中药饮品微生物限度检查法提供相关理论基础。
1 材料
1.1 样品
肉豆蔻药材购自安国市兴华中药材有限公司,经北京中医药大学中药学院中药鉴定系闫永红教授依性状鉴定为肉豆蔻科植物肉豆蔻(Myristica fragrans Houtt.)的干燥种仁。将无霉变的肉豆蔻饮片置恒温恒湿箱内(温度30℃,湿度95%)加速39天,每三天取一次样,共得到14批不同霉变程度样品。霉变不同时期样品(图1(a,b,c))。
1.2 培养基及试剂
胰酪大豆胨琼脂培养基、沙氏葡萄糖琼脂培养基、胰酪大豆胨琼脂对照培养基、沙氏葡萄糖琼脂对照培养基、聚山梨酯80均购自北京三药科技开发公司。
1.3 菌种
金黄色葡萄球菌[CMCC(B)26003 第4代]、枯草芽孢杆菌[CMCC(B)63501第4代]、铜绿假单胞菌[CMCC(B)10104 第4代]、黑曲霉[CMCC(F)98003 第4代]、白色念珠菌[CMCC(F)98001第4代]均为定量工作菌株,购自于北京三药科技开发公司。
1.4 仪器
SW-CJ-1FD型单人单面净化工作台(苏州净化设备有限公司,No:100253),MJ-70-1霉菌培养箱(上海一恒科学仪器有限公司,201309)。
2 方法与结果
参照《中国药典》2015年版第四部非无菌产品微生物限度检查通则1105:微生物计数法建立肉豆蔻饮片微生物计数方法。
2.1 菌液制备
使用前将未开启的西林瓶平衡至室温,将1.1 mL无菌生理盐水加入西林瓶中,盖上瓶盖,静置约5-10 s,无菌吸管反复吹吸10次以上使其完全溶解。吸取1 mL已完全溶解的菌液加入9 mL无菌生理盐水中,混匀,逐级进行10倍稀释,最终使其含菌数量约500-1000 cfu·mL-1。
2.2 供试液的制备
将肉豆蔻饮片置于用酒精棉球擦拭过的万能粉碎机中,粉碎,用灭菌的药匙将肉豆蔻粉末移至灭菌自封袋中备用。取10 g于灭菌研钵中,加入100 mL含0.1 mL聚山梨酯80的无菌生理盐水,迅速研磨使其溶解,制成1∶10供试液。依次制作1∶100、1∶1000、1∶10000、1∶100000、1∶1000000稀释液。
2.3 培养基适用性试验
2.3.1 需氧菌培养基适用性试验
分别移取金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌菌液1 mL(含菌量50-100 cfu)至灭菌平皿中,分别倾倒胰酪大豆胨琼脂培养基、胰酪大豆胨琼脂对照培养基15 mL,待其凝固后,倒置于恒温培养箱中30-35℃培养48 h。每个菌种每种类型培养基各做3个平行。测定菌落数。
被检固体培养基上的菌落平均数与对照培养基上的菌落平均数比值应在0.5-2范围内,且菌落形态大小与应与对照培养基上的菌落一致[17]。结果(表1,图2),被检固体培养基上的菌落平均数与对照培养基上的菌落平均数均在0.5-2范围内。被检固体培养基上菌落形态大小与比值对照培养基上的菌落一致。

表1 需氧菌培养基适用性试验结果

表2 黑曲霉、白色念珠菌培养基适用性试验结果
2.3.2 霉菌、酵母菌培养基适用性试验
分别移取黑曲霉、白色念珠菌菌液1 mL(含菌量50-100 cfu)至灭菌平皿中,分别倾倒沙氏葡萄糖琼脂培养基、沙氏葡萄糖琼脂对照培养基15 mL,待其凝固后,倒置于恒温培养箱中20-25℃培养72 h。每个菌种每种类型培养基各做3个平行。测定菌落数。
被检固体培养基上的菌落平均数与对照培养基上的菌落平均数比值应在0.5-2范围内,且菌落形态大小与应与对照培养基上的菌落一致。结果(表2,图3),被检固体培养基上的菌落平均数与对照培养基上的菌落平均数均在0.5-2范围内。被检固体培养基上菌落形态大小与对照培养基上的菌落一致。
2.4 计数方法适用性试验
2.4.1 需氧菌总数计数方法适用性试验
试验组:分别移取1∶1000、1∶10000、1∶100000供试液9.9 mL于灭菌试管中,加入制备好的金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、黑曲霉及白色念珠菌菌液0.1 mL,使其终浓度为每1 mL供试液中含菌量不大于100 cfu。从试管中移取1 mL至灭菌平皿中,立刻倾注胰酪大豆胨琼脂培养基,待其凝固后倒置于霉菌培养箱中30-35℃培养48 h。每个菌种平行制备2个平皿,测定试验组菌落数。
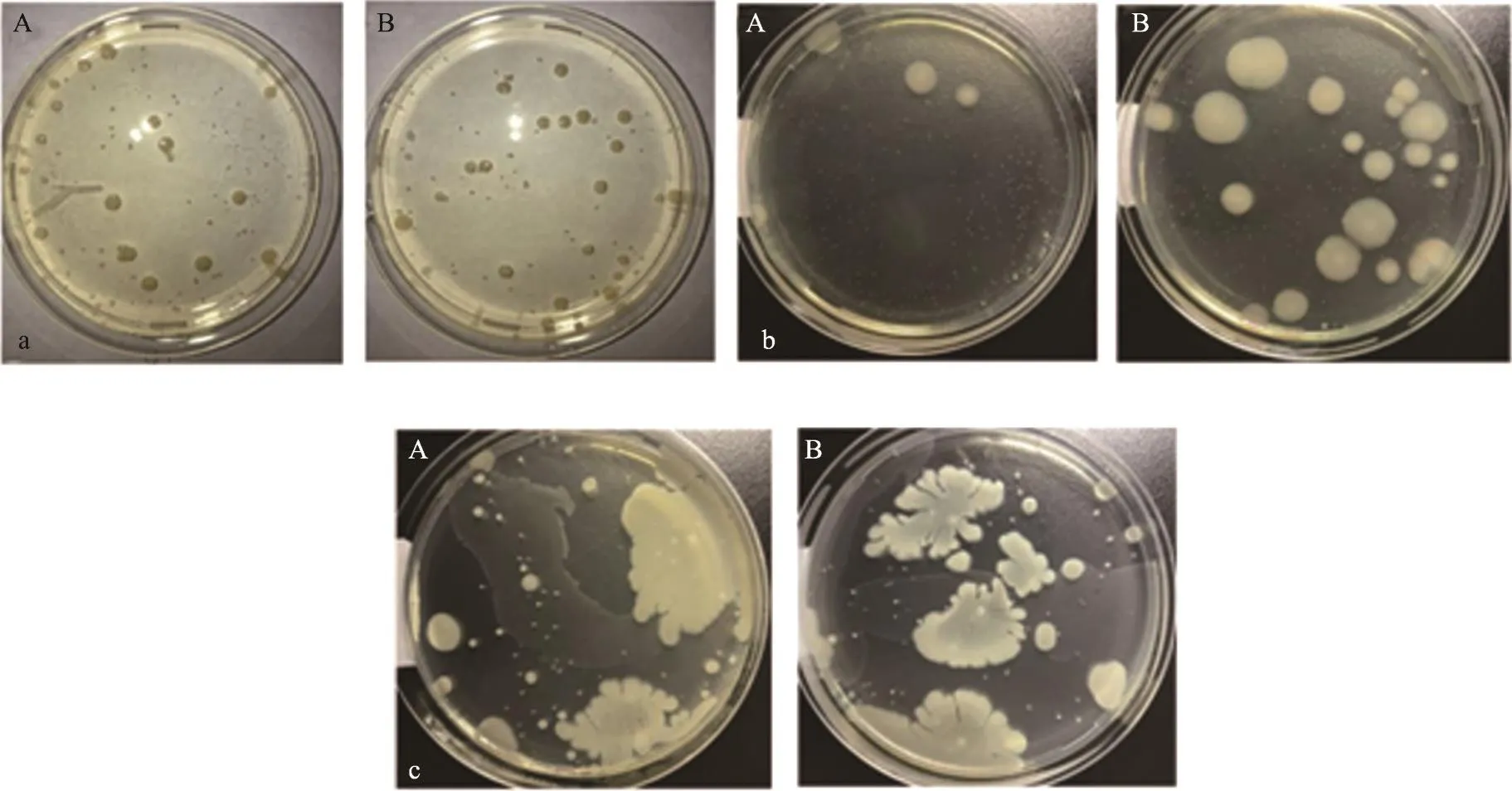
图2 a金黄色葡萄球菌;b铜绿假单胞菌;c枯草芽孢杆菌
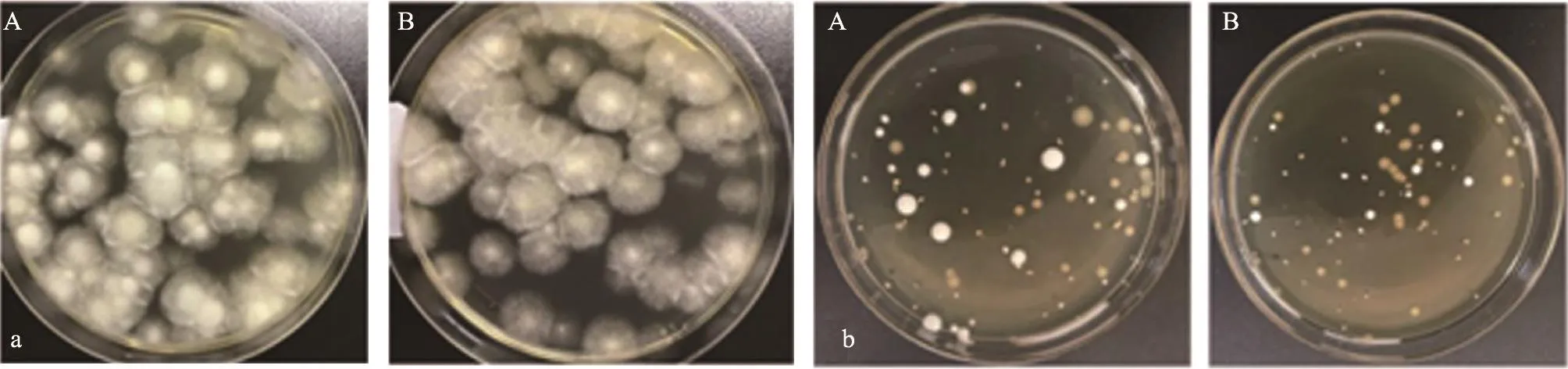
图3 a黑曲霉;b白色念珠菌
表3 需氧菌总数计数方法适用性试验结果
供试品对照组:分别移取1∶1000、1∶10000、1∶100000供试液9.9 mL于灭菌试管中,加入0.1 mL无菌生理盐水,其余按试验组操作。测定供试品对照组菌落数。
菌液对照组:取9.9 mL无菌生理盐水于灭菌试管中,加入与试验组相同的金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、黑曲霉及白色念珠菌菌液0.1 mL,使其终浓度为每1 mL供试液中含菌量不大于100 cfu,其余按试验组操作。测定菌液对照组菌落数,进行微生物回收试验。
阴性对照组:移取1 mL无菌生理盐水于灭菌平皿中,其余按试验组操作。平行制备2个平皿。
按回收率=[(试验组平均菌落数-供试品对照组平均菌落数)/菌液对照组平均菌落数]计算回收率,结果(表3)。根据2015年版《中国药典》,采用平皿法时,回收率应在0.5-2范围内。可得出,金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、黑曲霉需稀释至1∶10000,白色念珠菌需稀释至1∶100000方能达到回收率要求。
2.4.2 霉菌、酵母菌总数计数方法适用性试验
分别移取1∶10000、1∶100000、1∶1000000供试液9.9 mL于灭菌试管中,加入制备好的黑曲霉、白色念珠菌菌液0.1 mL,使其终浓度为每1 mL供试液中含菌量不大于100 cfu。从试管中移取1 mL至灭菌平皿中,立刻倾注沙氏葡萄糖琼脂培养基,待其凝固后倒置于霉菌培养箱中20-25℃培养72 h。每个菌种平行制备2个平皿,测定试验组菌落数。
同法测定供试品对照组、菌液对照组和阴性对照组菌落数。
按回收率=[(试验组平均菌落数-供试品对照组平均菌落数)/菌液对照组平均菌落数]计算回收率,结果(表4)。根据2015年版《中国药典》,采用平皿法时,回收率应在0.5-2范围内。可得出,黑曲霉需稀释至1∶10000,白色念珠菌需稀释至1∶1000000方能达到回收率要求。
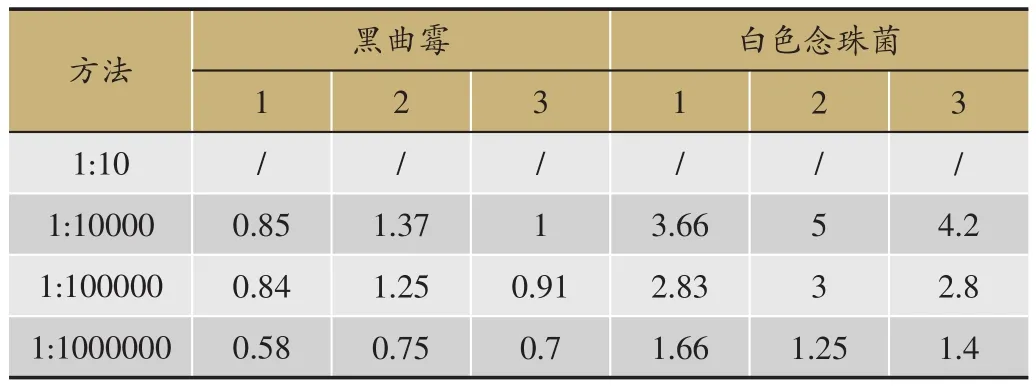
表4 霉菌、酵母菌总数计数方法适用性试验结果

表5 不同霉变程度肉豆蔻饮片菌落总数
2.5 不同霉变程度样品菌落总数测定
综上,选用 1∶1000、1∶10000、1∶100000、1∶1000000四个稀释度的供试液来测定不同霉变程度肉豆蔻饮片中需氧菌、霉菌及酵母菌的菌落总数。结果(表5)。显示,随着加速时间的延长,肉豆蔻样品中需氧菌菌落总数、霉菌、酵母菌菌落总数均呈上升趋势,且增长迅速。
3 讨论
实验结果表明金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、白色念珠菌及黑曲霉采用1:10普通平皿法进行方法适用性验证时,菌落数量较多,难以计数,不适合作为肉豆蔻饮片的微生物计数方法。经试验选用1∶1000、1∶10000、1∶100000、1∶1000000四个稀释度来进行肉豆蔻饮片微生物计数的方法学验证。其中金黄色葡萄球菌和枯草芽孢杆菌需稀释至1∶10000回收率可达到要求,而铜绿假单胞菌需稀释至1∶100000稀释级,才能达到回收率要求。黑曲霉和白色念珠菌分别在1∶10000、1∶100000稀释级时才能达到回收率要求。
通过对不同霉变程度肉豆蔻饮片微生物计数结果研究发现,随着加速时间的延长,肉豆蔻饮片霉变现象逐渐严重,且需氧菌和霉菌、酵母菌菌落总数均呈上升趋势,且加速0-6天时增长缓慢,6-9天呈爆发式增长,9-39天匀速增长。提示我们肉豆蔻作为常用药食两用药材在储藏过程中应实时监控其菌落总数,必要时增设微生物限度检查以保证用药的安全性与有效性。
有文献报道,中药饮片普遍受到多种微生物的污染,污染程度十分严重且污染的优势菌属大都是已知的产毒霉菌[18,19],因此在后续研究中应进一步研究肉豆蔻在霉变过程中产毒霉菌及控制菌的变化规律,及霉变产生的菌株对肉豆蔻饮片药效成分含量的影响,为建立更完善的肉豆蔻饮片质量标准提供依据。

