572张肿瘤患者肠外营养处方用药分析
邵 恒
(安徽医科大学附属六安医院/六安市人民医院药学部,安徽 六安 237005)
肠外营养(parenteral nutrition,PN)制剂是将机体所需的3大营养物质(葡萄糖、脂肪乳和氨基酸)与电解质、维生素等其他营养素根据患者病情按一定剂量和比例混合后配制于营养袋中的一种静脉输液,主要用于肠道功能异常而无法进食或进食量不足等各类危重症患者,提供患者每日所需的能量和营养物质,保证基本代谢,改善或维持患者的营养状况。营养不良是恶性肿瘤患者的主要死亡原因之一。流行病学调查结果显示,31%~87%的恶性肿瘤患者存在营养不良,消化道肿瘤更易发生营养不良[1]。营养不良严重影响肿瘤患者的治疗效果,甚至缩短生存期,营养支持治疗可纠正或改善非终末期恶性肿瘤患者的营养状况及免疫功能,减少并发症,提高生活质量,延长生存期,为进一步抗肿瘤治疗提供了物质基础[2-4]。营养不良已成为临床肿瘤防治中不容忽视的问题,因此,早期发现、评估患者营养不良风险至关重要[5]。但部分临床医师对患者营养问题关注不够,对PN缺乏相应的了解和认识,处方存在一定问题。现对某三级甲等医院(以下简称“该院”)静脉用药调配中心接收的肿瘤患者PN处方进行统计分析,了解肿瘤患者PN制剂使用情况,以期为规范PN的临床应用提供参考,提高PN治疗的安全性和有效性。
1 资料与方法
回顾性调查2016-2018年该院静脉用药调配中心接收、审核并调配的肿瘤患者PN处方,共572张(涉及患者572例)。依据《肿瘤营养学》(2012年版)、《恶性肿瘤患者的营养治疗专家共识》(2012年版)等对PN处方进行合理性审核,审核内容包括是否有PN适应证、成分配比是否合理及疗程是否合理等。
2 结果
2.1 应用PN患者的基本情况、疾病分布
572例应用PN的患者中,男性患者409例(占71.5%),女性患者163例(占28.5%);≤18岁者1例,>18~70岁者417例,>70岁者154例,见表1。消化系统肿患者使用PN较为广泛,尤其是肠癌、胃癌和食管癌患者,见表2。
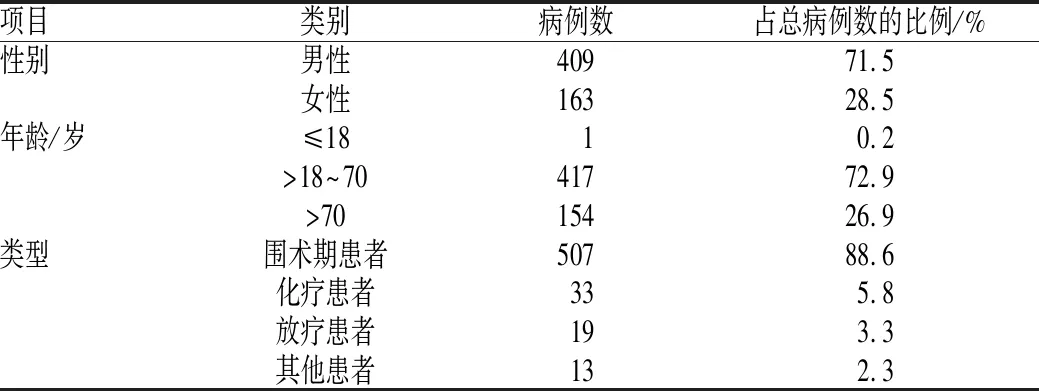
表1 应用PN患者的基本情况Tab 1 General information of patients with PN
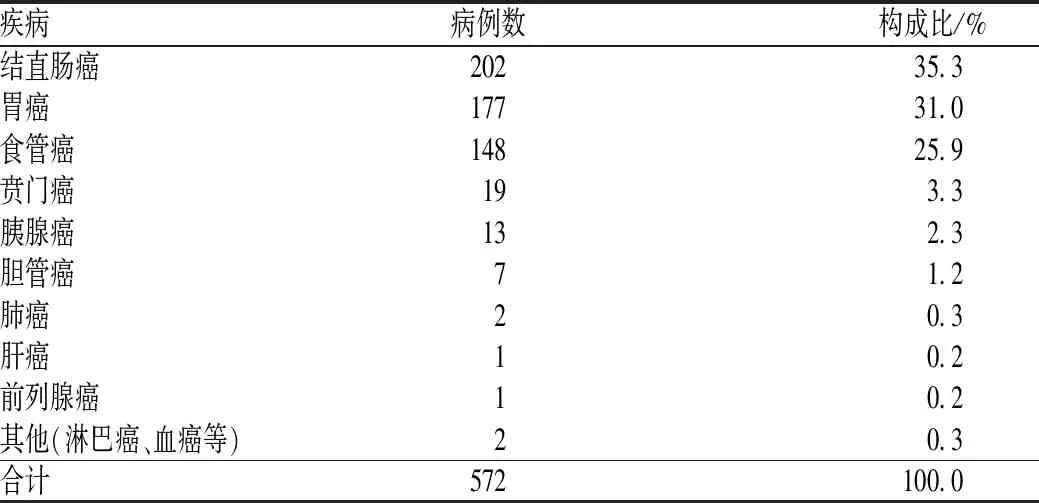
表2 应用PN患者的疾病分布Tab 2 Distribution of diseases in patients with PN
2.2 PN处方中药物品种分布
572张PN处方涉及17种药品制剂,均使用了葡萄糖、脂肪乳和氨基酸等3大基础营养素;此外,丙氨酰谷氨酰胺注射液的使用也较为频繁(53张,占9.3%),见表3。
2.3 PN处方合理用药考察结果
PN处方中,成分配比合理性的考察因素包括热氮比、糖脂比、总热量和液体量。本调查结果显示,PN处方主要不合理因素包括:热氮比不在肠外肠内营养指南规定的(100~200) ∶ 1范围内;糖脂比不在(1~2.3) ∶ 1范围内;提供的总热量不足或超量[正常值为25~30 kcal/(kg·d)];液体量不在25~35 ml/(kg·d)范围内,见表4。

表3 PN处方中药物品种分布Tab 3 Distribution of drug varieties in PN prescriptions
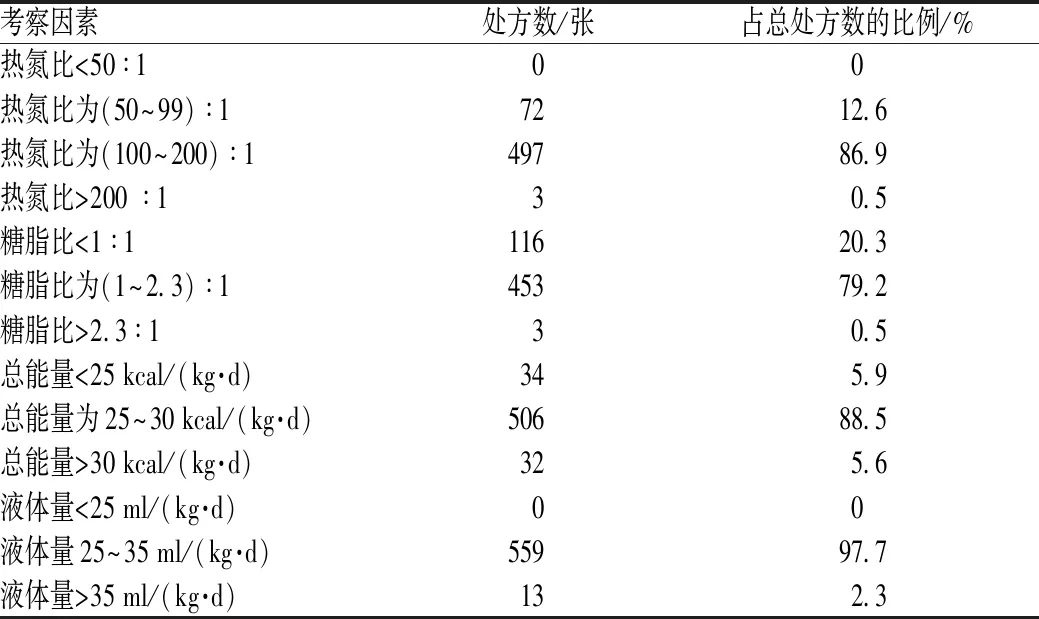
表4 PN处方合理用药考察结果Tab 4 Investigation results of rational drug application in PN prescriptions
2.4 PN处方的用药疗程分布
572张PN处方中,用药疗程<5 d的处方有12张(占2.1%);用药疗程为5~14 d的处方有486张(占84.9%);用药疗程>14 d的处方有74张(占13.0%)。
3 讨论
3.1 PN治疗的适应证
应对肿瘤患者进行合理的营养治疗,正确评定患者的营养状况,筛选出有适应证的患者,及时给予营养支持治疗。营养风险筛查工具为目前中华医学会推荐使用的《营养风险筛查表2002》(NRS2002),当NRS2002 总分≥3分时,提示患者存在营养风险,应结合临床,制订营养支持方案[6]。《肿瘤患者肠外营养指南》中规定,PN适应证包括:当患者可能存在长期(>10 d)的肠内营养摄入不足(<60%需要量)时,可考虑采用PN支持;围术期有营养风险或营养不良的患者及各种原因导致连续5~10 d及以上无法经口摄食达到营养需要量的患者,应给予PN支持[7]。临床医师应根据患者的实际情况选择合适的营养治疗方式,如果患者具有肠道功能,应首选肠内营养[8]。本调查中,绝大部分患者存在营养风险,应该给予营养支持治疗。
3.2 总能量供给
肿瘤患者与正常人的能量需求几无差别,卧床患者可用20~25 kcal/(kg·d)来计算,可以下床活动的患者以25~30 kcal/(kg·d)计算[9]。本调查中,88.5%的PN处方总能量达到25~30 kcal/(kg·d);5.9%的PN处方总能量<25 kcal/(kg·d);5.6%的PN处方总能量>30 kcal/(kg·d)。
3.3 糖脂比
糖和脂肪是PN的主要能源物质,不合理的糖脂比会增加患者代谢并发症发生概率。一般情况下,脂肪乳所提供的能量应占非氮供能的30%~50%。大量数据显示,肿瘤患者PN采用较高的脂肪供能比(约占非氮供能的50%),有较好的节氮作用[10]。本调查中,PN处方糖脂比合理率为79.2%,20.8%的PN处方糖脂比不在合理范围内。
3.4 热氮比
热氮比在合理范围内,可减少机体蛋白质分解,促进蛋白质合成,使之达到正氮平衡,而总热量达标和蛋白质达标正是恶性肿瘤患者需要的[11-12]。一般情况下,PN处方中的热氮比为(100~200) ∶ 1[13]。在不同疾病状况下,需要根据病情调整热氮比,如感染患者应增加氮量,降低非蛋白热量;肾衰竭和氮质血症患者应减少氮量,提高非蛋白热量。本调查中,大部分PN处方的热氮比处于合理范围之内,有3张(占0.5%)PN处方的热氮比>200 ∶ 1,有72张(占12.6%)PN处方的热氮比<100 ∶ 1。热氮比过低,提示机体利用氨基酸注射液作为能量来源之一,成本-效益比降低;热氮比过高,则表明患者氨基酸补充量不足,需要增加氨基酸注射液的使用剂量。
3.5 液体量
PN补液量一般按照25~35 ml/(kg·d)给予,同时需要结合具体病情考虑。本调查中,2.3%的PN处方液体量不在合理范围内。
3.6 给药途径及疗程
在选择PN制剂的给药途径时,应考虑渗透压和输注时间。一般情况下,通过外周静脉输注时的渗透压应<900 mOsm/L,渗透压过高易引起静脉炎。疗程<5 d是PN治疗的禁忌证,因为短期治疗对疾病本身并无益处。本调查中,PN制剂的给药途径采用中心静脉导管或外周静脉导管置管,有12张PN处方的疗程<5 d,原因是患者自动出院;有74张PN处方的疗程>14 d。
3.7 丙氨酰谷氨酰胺、维生素和胰岛素的使用情况
丙氨酰谷氨酰胺是一种高浓度溶液,不可直接静脉输注,用时需加入至5倍体积以上的其他氨基酸或含有氨基酸的溶液中,其供给的氨基酸量不应超过全部氨基酸供给量的1/5。大量研究证实,谷氨酰胺对于增强免疫功能和胃肠道功能、维护胃肠黏膜屏障及减少肠源性感染具有十分重要的意义[14]。相关研究结果认为,在小鼠模型中,谷氨酰胺起到了一定的抑制全身肿瘤转移的作用,在小鼠结肠癌模型上的研究结果显示,谷氨酰胺与n-3多不饱和脂肪酸联合应用能使接受伊立替康和氟尿嘧啶化疗的小鼠对化疗的耐受程度明显增强,但其在人类中是否有同等效应还有待研究证实。加入维生素是PN治疗中不可缺少的措施,尤其是对于处于应激状态或长期使用PN的危重症患者,补充维生素显得尤为重要。建议在营养支持一开始就加用维生素,因为有效利用蛋白质和能量需要足量的微量营养素作为基础[15]。本调查中,使用丙氨酰谷氨酰胺的PN处方有53张(占9.3%),均存在使用指征。脂溶性维生素及水溶性维生素的使用率达100%。胰岛素的使用率也为100%,且均为直接加入全营养混合液3 L袋输注,并顺利完成PN支持治疗,无患者发生低血糖昏迷及非酮症高渗性糖尿病昏迷。胰岛素与葡萄糖的比例范围较宽,一般为1 U胰岛素配3~10 g葡萄糖。但将胰岛素添加在PN营养袋中与单独使用哪种方式更为有利,尚有争议。相关研究认为,全营养混合液3 L袋及调配所用注射器材质的主要成分为聚乙烯醋酸酯和聚氯乙烯,对胰岛素的吸附作用较弱;而且,全营养混合液中的多种成分可以减少胰岛素吸附,起到一定的保护作用。
综上所述,该院PN处方总体情况良好,但仍有部分临床医师对PN的合理用药缺乏规范化指导,错误地认为只要简单地将葡萄糖、氨基酸或脂肪乳混合输注就是PN治疗,对各种营养成分的用量和配比没有充分的重视,需引起关注。只有合理、科学的PN处方,才能发挥其在危重症救治中的作用,不合理的PN处方甚至可能增加患者的肝肾负担,加重病情。PN治疗对医师的用药能力有一定的要求,需引起临床医师的足够重视和慎重对待。建议可以参照国内外的经验,建立由医师、营养师、药师和护师等共同组成的营养支持小组,对PN的合理应用进行正确科学的干预和指导。

