板芪口服液的工艺研究
董蒨蒨,孙耀贵,孙 娜,尹 伟,范阔海,李宏全
(山西农业大学动物科技学院,山西 太谷 030801)
板芪口服液的处方是本实验室前期筛选出来用于治疗猪病毒性心肌炎的复方中药。为了能更简便、有效的使用此方剂治疗疾病,本实验室依据此处方将其研制为口服液。口服液的研制过程包括提取、纯化和成型工艺。其中提取工艺影响着中药制剂的质量、药用资源及临床疗效,关系到中药制药产业的发展。不良的提取工艺造成中药制剂提取周期长、有效成分损失多、提取物中杂质量高等问题[1],影响中药的推广。纯化工艺与口服液的澄清度有关,澄清度是口服液的重要质控指标,它反映了产品稳定性,是口服液制备中的关键问题[2]。因此,必须在传统中医药基础上进一步优化中药制剂工艺使其更符合现代化生产并且建立科学可行的质量控制体系,这对中兽药制剂的研发甚至中兽药事业的发展具有极其重要的意义[3]。本实验围绕板芪口服液工艺的提取、纯化、防腐等环节进行优化,旨在建立更有效、更稳定的工艺,为板芪口服液申报新兽药提供数据支持。
1 仪器与试剂
1.1 仪器 Agilent 1260高效液相色谱仪(Agilent公司);自动煎药包装机(中国吉首市中诚制药机械厂);旋蒸仪(Buchi公司);数显恒温水浴锅(江苏金坛市金城国胜实验仪器厂);电子分析天平(赛多利斯公司);SB25-12D超声清洗机(Scientz公司)。
1.2 试药 黄芩苷对照品(批号110715-201720)。原料药材板蓝根、黄芩、黄芪、丹参、连翘、蒲公英由山西奥信动物药业有限公司提供。甲醇为色谱纯(Merck公司),水为超纯水,其他试剂均为分析纯。
2 方法与结果
2.1 吸水率的考察 按组方称取板蓝根10 g、黄芪10 g、黄芩5 g、丹参5 g、连翘5 g、蒲公英5 g药材3组,加入10倍量水,封口,室温放置,分别于0.5 h、1 h、1.5 h、2 h、2.5 h、3 h 取出1 份药材,滤除水,称重,计算吸水率。如表1在1.5 h后吸水量明显减少,故在煎煮之前需加10倍量水浸泡1.5 h。

表1 板芪口服液药材吸水率
2.2 黄芩苷的含量测定
2.2.1 色谱条件 色谱柱:Agilent ZORBAX SBC18(250 mm ×4.6 mm,5 μm),流动相:甲醇:水:磷酸(47∶53∶0.2),流速:1 mL/min,检测波长:280 nm,柱温:25 ℃,进样量:10 μL,以黄芩苷计理论塔板数不低于2 500[4]。
2.2.2 样品溶液的制备 对照品制备:精密称定黄芩苷对照品12.25 mg,加甲醇稀释制成61.25 μg/mL的对照品溶液。供试品制备:精密量取板芪口服液5 mL于100 mL容量瓶中,加入70%乙醇定容至刻度,摇匀,滤过,取续滤液1 mL加甲醇至10 mL,即得供试液。
2.2.3 线性范围考察 精密吸取黄芩苷对照品溶液(3.828 mg/mL)1 mL,2 mL、3 mL、4 mL、6 mL、8 mL置于25 mL容量瓶中,加甲醇稀释至刻度,摇匀,按照2.2.1项的条件进行进样,记录峰面积,以进样量为横坐标,峰面积为纵坐标,绘制标准曲线,计算得回归方程y=3 021.3x-31.634,R2=0.999 9,结果表明,黄芩苷进样量在0.153 1~1.225 μL之间线性关系良好。
2.3 板芪口服液水提工艺的考察 根据表2进行L9(34)正交试验。每次按照处方称取药材40 g,按表添加相应倍量水,回流提取,过滤,提取液浓缩至40 mL,根据2.2项的方法计算黄芩苷的含量,结果如表3与表4。表3极差分析结果表明,各因素对水提液中黄芩苷提取影响的大小顺序为C(提取次数)>A(加水量)>B(提取时间)。表4方差分析结果表明,因素C对黄芩苷提取结果有极显著的影响,因素A、B各水平间无显著性差异,但考虑到生产周期与成本,最终确定板芪口服液的最佳提取条件为A2B2C2,即加10倍量水浸泡1.5 h后,煎煮2次,每次1.5 h。并根据最佳工艺进行3次验证试验,得到黄芩苷的平均含量为5.59 mg/mL,相对标准偏差(Relativestandarddeviation,RSD)为0.62%,小于1%。

表2 板芪口服液水提工艺正交表

表3 板芪口服液水提工艺参数确定正交试验结果

表4 方差分析表
2.4 板芪口服液醇沉工艺的考察 按照以上工艺制备板芪口服液的水提样品,根据表5进行L9(34)正交试验,得到结果表6与表7。表6极差结果表明,各因素对水提液中黄芩苷提取影响的大小顺序为B(醇沉浓度)>A(生药浓度)>C(静置时间)。方差分析结果表明,因素A与B对黄芩苷提取结果有极显著的影响,故选择A1B1。因素C无显著性差异,但是,乙醇加入量随着提取液浓度升高而减少,综合考虑黄芩苷损失率和乙醇用量最终确定板芪口服液的最佳醇沉条件为A2B1C1,即药液浓缩至1.5 g/mL,加入乙醇至含醇量为60%,4℃放置12 h。根据最佳工艺进行3次验证实验,得到黄芩苷的平均含量为3.38 mg/mL,RSD为0.87%,小于1%。

表5 板芪口服液醇沉实验正交表

表6 板芪口服液醇沉工艺参数确定正交试验
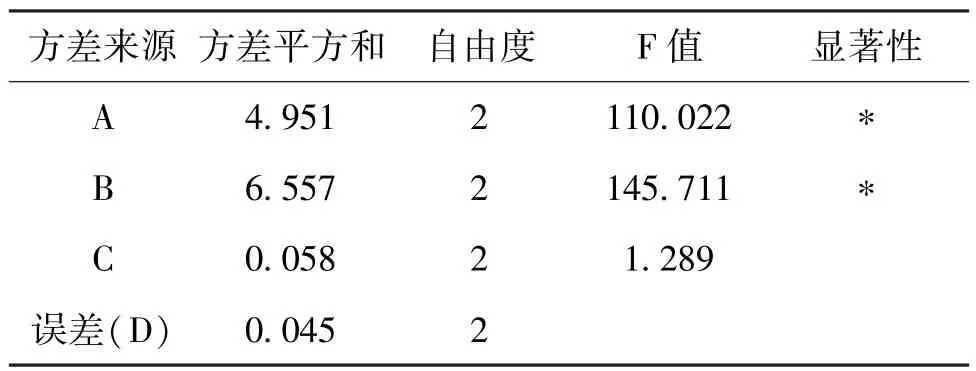
表7 方差分析表
2.5 板芪口服液的水沉工艺 由于挥发乙醇后的样品加入蒸馏水有明显的沉淀产生,所以考察不同静置时间24 h、48 h、72 h对样品澄清度的影响。结果得到3种静置时间的样品澄清度相似,48 h后沉淀不再增多,所以选择静置时间为48 h。最终确定板芪口服液的水沉工艺为回收乙醇后加水至生药浓度为1 g/mL,4℃静置48 h,过滤。
2.6 板芪口服液的防腐工艺 取经以上工艺制得的板芪口服液样品加入3‰苯甲酸钠,进行需氧菌、真菌、酵母菌、大肠杆菌的微生物限度检查试验,各种数目均符合兽药典中的规定。所以确定防腐剂为3‰苯甲酸钠。
2.7 三批样品的验证实验 按照板芪口服液的处方称取3份药材,根据所确定的最佳提取、醇沉、水沉和防腐工艺进行制备,得到3批样品,其中黄芩苷的平均含量为2.05 mg/mL,RSD为1.76%。
3 讨论
本试验中的板芪口服液是主要由板蓝根、黄芪、黄芩等组成的中药复方制剂。黄芩苷是黄芩药材的主要活性成分,具有抗炎的作用,主治诸热、恶疮[5],并且黄芩苷的含量高,提取过程中误差小,具有统计学意义。所以将黄芩苷作为板芪口服液工艺检测的指标成分。
板芪口服液在提取工艺之前进行了吸水率的测定,主要目的是为了让有效成分更完全的溶解到溶剂中,1.5 h后药材吸水率变化逐渐减小,因为口服液的制备周期不宜过长,所以选择了在提取前浸泡药材1.5 h。根据预试验和实验室前期经验设计了提取工艺中正交试验的3种因素:加水量、提取时间和提取次数,并分别设计了3个水平。其中提取时间过长或过短都不利于口服液的质量,所以3个水平设计的时间分别为1 h、1.5 h、2 h。
板芪口服液醇沉工艺中生药浓度浓缩至2g/mL以上时不但很难再浓缩并且无法精确测量其体积,所以设计的生药浓度分别为1g/mL、1.5 g/mL、2 g/mL。醇沉浓度在预试验过程中,尝试从10%到90%乙醇浓度进行醇沉,浓度过低时不产生沉淀,浓度低于60%时沉淀较少,浓度过高时考虑到实际生产中的乙醇的耗费,最终选择60%、70%、80%乙醇浓度。对静置时间的设定考虑到口服液工艺的生产周期,所以不宜过长,选择了12 h、24 h、36 h这3个静置时间。
板芪口服液的水沉工艺采取了冷藏水沉法[6],考察到不同静置时间对口服液澄清程度的影响与工艺的生产周期,选择了48 h的静置时间。板芪口服液的防腐工艺是依据兽药生产经验与相关文献选择了3‰ 苯甲酸钠[7]作为防腐剂。最终确定板芪口服液的工艺为一份药材加10倍量水浸泡1.5 h后煎煮2次,每次1.5 h,药液浓缩至1.5 g/mL,加入乙醇至含醇量为60%,4℃静置12 h,回收乙醇,加水至生药浓度为1 g/mL,4℃静置48 h,过滤,加入3‰的苯甲酸钠。
本试验从口服液提取、醇沉、水沉、防腐工艺环节出发,优化了板芪口服液工艺,为板芪口服液申报新兽药奠定了数据基础。

