肝脏神经内分泌癌的CT及MRI特征
史芳芳 郑增 任洪伟 安维民 董景辉
神经内分泌瘤(neuroendocrine carcinoma,NEC)是一种起源于神经内分泌细胞和肽能神经元的肿瘤,胰腺、胃肠道、肾上腺、肺、胆囊等内分泌器官或非内分泌器官均可见。胃肠道的病变常常转移至肝脏,但肝脏原发的神经内分泌肿瘤非常少见。本文回顾性分析肝脏NEC(HNEC)的临床、影像及病理资料,总结其特征性表现,以期提高对该病的诊断及鉴别诊断水平。
资料和方法
一、研究对象
回顾性分析2011年至2017年解放军第三〇二医院经病理证实的37例HNEC患者的临床资料。37例HNEC患者中,原发11例,转移26例。原发组病灶均经过全身检查,包括超声、CT和MRI、胃肠镜等相关影像检查未发现其他器官NEC,临床随访一年以上未发现肝外存在原发肿瘤。其中男7例,女4例,年龄30~74岁,平均年龄48岁。4例患者有肝炎病史,3例患者有腹痛或腹胀表现;AFP及 CA19-9均在正常范围,2例CA125升高,2例CEA升高,3例NEC升高。转移组26例病灶中来源于胃肠道14例,胰腺6例,胆囊4例,肺2例;男16例,女10例,年龄30~76岁,平均54岁。16例患者有肝炎病史,11例患者有腹痛或腹胀表现;检测4例CA19-9升高,4例CA125升高,7例CEA升高,13例NEC升高。
二、研究方法
采用GE公司64排Discovery CT750 HD或Lightspeed VCT机器进行CT扫描。肝脏平扫及动态增强三期扫描,层厚5 mm,重建间隔5 mm,螺距1.5。造影剂碘普罗胺300~370 mg/mL,以1~1.5 mL/kg计算造影剂总量,经肘静脉团注,速率3.0~4.5 mL/s;动脉期20~30 s,门脉期60 s,平衡期150~180 s。
MR检查采用GE 3.0T Signa HDXt及1.5T Signa HDx磁共振扫描仪。扫描序列:轴位T1WI平扫WATER: BH L-Flex Mask(3.0T)或LAVA Mask(1.5T),T2WI fs FRFSE, BH DWI b=800 s/mm2,双回波成像InPhase/OutPhase:BH L-Flex Mask(3.0T)或BH T1WI Dual(1.5T);三维动态增强扫描:LAVA-XV+C,动脉期(早、晚两期)18~20 s,门脉期(早、晚两期)60 s,冠状位平衡期(3 min),延迟期5 min。造影剂使用钆喷酸葡胺注射液,以0.1 mL/kg计算总重量,经肘静脉团注,速率2.5 mL/s。
三、观察指标
图像由两位具有腹部诊断专长的放射科高年资主治医师在不知道病理结果的情况下独立通过PACS系统阅片,意见不一致时经协商达成共识。分析病灶的数目、大小、平扫和增强扫描影像表现,并注意观察肿瘤周围血管、胆道的改变。病变大小以病变延迟期扫描最大径测量;病灶平扫及增强扫描的密度及信号强度以周围肝实质为参照,低于临近正常肝实质为低密度或低信号,与肝实质相似为等密度或等信号,高于肝实质为高密度或高信号。
结 果
原发组免疫组织化学结果触突素(Syn)阳性10例,嗜铬蛋白颗粒(CgA)阳性9例,CD56阳性9例;转移组免疫组织化学结果触突素(Syn)阳性25例,嗜铬蛋白颗粒(CgA)阳性15例,CD56阳性22例。9例患者原发性HNEC为单发,CT表现肿瘤平扫为低密度或混杂低密度占位,肿瘤常见囊变区,1例伴出血时内见斑片状稍高密度,增强扫描呈快进快出或快进慢出,肿瘤实性部分门脉及平衡期CT值高于动脉期;转移性HNEC均为多发、体积较大,CT平扫呈稍低密度,增强扫描呈环形或不均匀明显强化门脉及平衡期相对肝实质呈等或稍低密度。见图1,2。
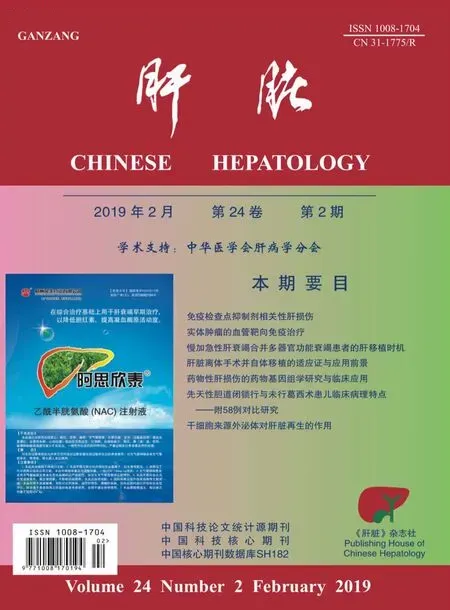
A.平扫病变内见高密度出血;B.动脉期轻度不均匀强化;C.门脉期呈不均匀稍低密度;D.平衡期呈低密度
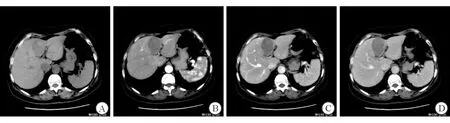
A.平扫多发稍低密度结节;B.动脉期部分病变边缘强化;C.门脉期病变边缘强化;D.平衡期造影剂渗入
原发性HNEC磁共振DWI呈均匀或厚壁样稍高信号,T2WI呈混杂稍高信号,部分病变内见高信号囊变区(5/8),T1WI呈稍低信号,部分病变呈稍高信号,增强扫描呈中度均匀强化或边缘强化,部分病变(3/8)内可见粗大供血动脉,门脉及延迟期呈等或稍低信号部分病变可见完整或不完整假包膜,肿瘤周围门脉及肝静脉受压移位,但无癌栓形成。转移性HNEC磁共振DWI多呈环形高信号(11/17),T2WI呈稍高信号, T1WI呈稍低信号,大部分病变内见囊变坏死区(12/17),增强扫描动脉期不均匀强化或环形强化,门脉及延迟期多数(9/17)呈“同心圆样”改变,部分(2/17)门脉血管内可见癌栓。见图3,4。
讨 论
NEC起源于神经嵴kulchisky细胞(嗜银细胞),也称类癌或嗜银细胞瘤,可伴发或不伴类癌综合征[1],大部分原发于胃肠道及胰腺,肝脏是常见的转移部位[2-3]。本组26例转移性NEC中20例来源于胃肠道及胰腺,占77%,与文献报道相近。多数学者认为原发性HNEC是肝内胆管上皮散在分布的神经内分泌细胞增殖形成的。本病早期常无明显的症状、体征,少数出现类癌综合征。本组37例中23例无明显的症状,14例因腹痛腹胀就诊,与文献报道不太一致,分析原因可能是因为本病早期缺乏临床症状而就诊相对较晚,当病灶较大时出现了压迫症状才就诊。文献报道HNEC病灶常较小,转移性病灶直径常<3 cm[4],原发病灶可相对稍大,本组病变较文献报道要大,<3 cm者仅有2例。患者AFP均为阴性,少部分患者出现CA125、CA19-9、CEA轻度升高,16例患者出现NEC升高,可见NEC的检查可能对该病有一定提示作用。 NEC的确诊需要病理和免疫组织化学的支持,一般认为, CgA、Syn 、CD56及 NSE 阳性 是确诊的依据[5-7]。本组 37 例患者Syn 阳性35例、CgA 阳性24例、CD56阳性31例,与文献报道基本一致。但9例行NSE检查者仅有2例阳性。单纯病理免疫组织化学检查很难区分原发性与转移性,还需要依赖影像学做全面系统的检查及临床随访来加以鉴别。
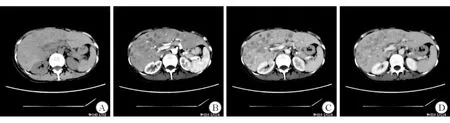
A.DWI呈不均匀高信号;B.T2WI病变内见多发小囊变区;C.动脉期病变见粗大供血动脉;D.延迟期见纤维包膜环形强化
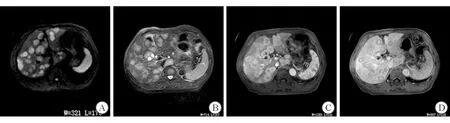
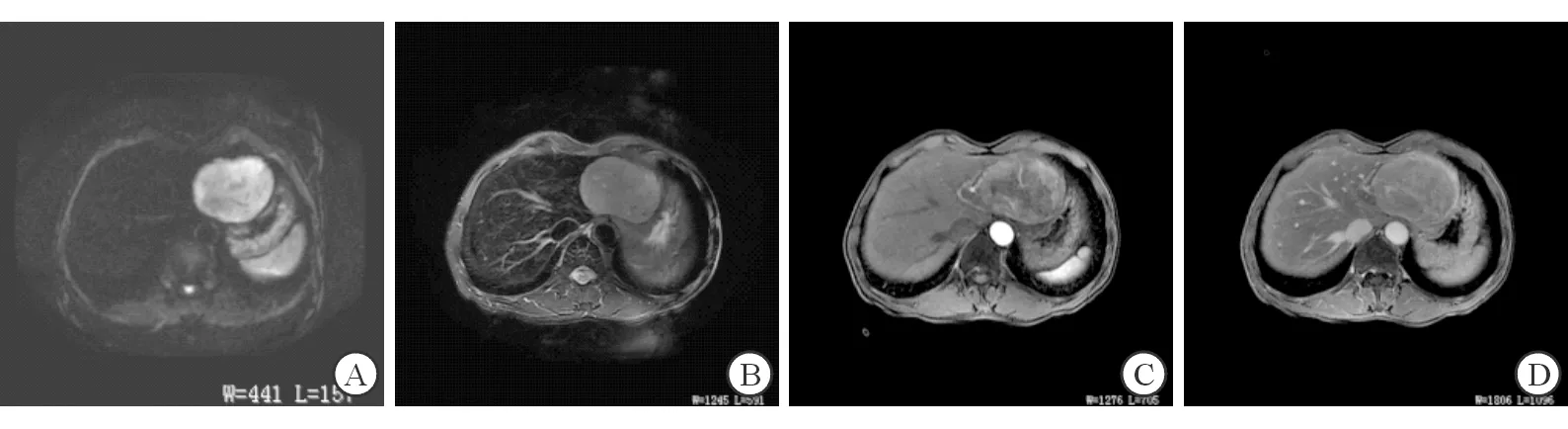
A.DWI肝内多发厚环样高信号;B.T2WI部分病变内见高信号囊性区;C.动脉期病变呈环形强化;D.延迟期呈靶环征
HNEC 都表现为囊实性的肿块或结节,原发者常为单发,少数病例可见子灶,转移者均为多发,CT平扫呈低密度,境界清楚,囊变坏死较明显[8],部分病例可显示病灶内出血,病灶内罕见有钙化,CT 表现增强扫描动脉期病灶可见厚壁样强化, 内壁不规则,门静脉期及延迟期病灶持续性强化或稍减低,呈现快进快出或快进慢出的强化方式,这与病变内纤维成分比例有关,此期大部分病灶可清晰显示包膜强化[9-12],原发性与转移性强化特点相似,CT检查很难鉴别。
有研究表明,原发性HNEC的MR特征与其他肝脏恶性肿瘤相似,表现为DWI呈厚壁或结节样高信号,T1WI 呈低信号,T2WI呈混杂高信号,多数病灶内可见点片状长T2 信号,这与病变内成分有关,病理证实病变内囊性T2WI高信号区为含有黏液的囊性变区,故其分布呈偏心性或弥漫性灶状分布,较大的囊性变可有黏液分层表现[13]。本组25例MR检查病例中17例T2WI出现明显囊变区,与文献报道基本一致。增强扫描原发性NEC肿瘤实性部分多呈现 “快进快出”的强化方式。肿瘤较大时可见瘤内增粗迂曲的供血动脉及粗大引流静脉,延迟期可出现纤维包膜的强化,但病灶不论大小均未出现门静脉内癌栓形成,胆管未见侵犯及胆管扩张征象[14-16]。转移性病灶平扫特点与原发性相似,但肿瘤常为多发,增强扫描大部分表现为动脉期病变边缘强化,门脉期及延迟期造影剂逐渐渗入,延迟期部分病变可呈现“偏心性靶环征”。有学者认为,肝脏转移性NEC与其原发灶间的血供特点有一定相关性[17],如胰腺来源的HNEC主要表现为血供丰富的均匀强化结节。本组17例转移性HNEC的MR无类似表现。
HNEC 应与以下肿瘤进行鉴别,①原发性肝细胞肝癌:多有肝炎肝硬化的背景,60%左右病例AFP明显升高,典型的CT 及MR动态增强扫描呈“快进快出”强化,延迟期多数病灶可见假包膜环形强化,较大病灶常伴门脉癌栓;部分较小病灶或分化较好的病灶可出现“快进慢出”的强化方式[18]。HNEC多无肝硬化背景,AFP不高,不伴门脉癌栓。②肝内多发转移瘤:多有原发肿瘤病史,肝内多发病灶多呈乏血供,病灶内的囊变坏死多呈类圆形位于病灶中心,增强典型者可见“牛眼征”改变[19]。HNET的囊性变为偏心性。③肝内胆管细胞癌:肝内胆管细胞癌血清CA19-9常升高,多伴有病灶远端肝内胆管扩张、临近肝包膜凹陷、肝门区及腹膜后淋巴结转移等,增强扫描动脉期病变边缘轻度强化,门脉期向心性填充强化,延迟期周边区造影剂消退呈稍低信号或密度,中心纤维成分缓慢持续强化呈稍高信号或密度[20]。HNEC多无肝内胆管扩张,不伴有肝包膜凹陷。
综上所述,HNEC作为肝脏少见的恶性肿瘤,其影像学表现具有一定的特征性,原发性病灶常单发,无肝炎肝硬化病史,多伴有偏心性囊变区,增强为富血供,不伴门脉及胆管癌栓;临床上病人AFP不高。转移性病灶常多发,可见偏心性囊变,增强动脉期边缘环形强化,门脉及延迟期可呈现“偏心性靶环征”。影像上表现出上述特征时应考虑到该病可能,但最终确诊仍需要取得组织病理学、免疫组织化学证据。