原发性肝细胞癌组织PD-L1、MDR1表达变化及其临床意义
苏纯洁,何前进,毛伟明,张喜华,岑红兵,张松柏
(1 荆门市第一人民医院,湖北荆门448000;2 黄冈市中心医院)
原发性肝细胞癌(以下称肝癌)是临床常见的消化系统恶性肿瘤之一,其发病率和病死率分别居所有恶性肿瘤的第三位和第二位。虽然根治性手术是治疗肝癌的最有效手段,但由于其早期症状不明显,多数患者就诊时已错过了最佳手术时机,化疗成为中晚期肝癌综合治疗的重要手段。但肝癌常产生多药耐药(MDR)现象,导致化疗效果明显下降[1]。因此,探索引起肝癌MDR的机制具有重要意义。细胞程序性死亡受体1(PD-1)与其配体PD-L1属于CD28/B7家族,是一对共刺激分子,具有负性调控作用。PD-1通过与其受体PD-1结合,可降低T细胞的免疫应答,继而抑制T细胞的抗肿瘤作用,使肿瘤细胞逃避机体免疫系统的监视和清除[2,3]。有研究发现,肺癌、乳腺癌等肿瘤组织PD-L1表达明显升高,且其表达越高,患者预后越差[4~6]。多药耐药基因1(MDR1)是ATP结合盒载体超家族成员之一,其基因编码的蛋白产物P-gp可将细胞内多种抗肿瘤药物泵出细胞外,还可使抗肿瘤药物在细胞内再分布,从而使抗肿瘤药物无法有效杀灭肿瘤细胞。P-gp高表达是肿瘤细胞MDR的主要原因[7,8]。有研究发现,乳腺癌组织PD-L1表达与MDR1表达密切相关[9]。但二者在原发性肝癌组织中的关系尚不清楚。为此,我们进行了如下研究。现报告如下。
1 材料与方法
1.1 材料 选择2013年3月~2016年12月黄冈市中心医院手术切除的原发性肝癌组织及其配对的癌旁正常组织标本各90例份。标本来源患者纳入标准:①经组织病理学检查,明确原发性肝癌诊断;②均接受肝癌根治性手术;③术前未接受过任何抗肿瘤治疗。排除标准:①转移性肝癌者;②入院前已接受过化疗、放疗或其他抗肿瘤治疗者;③伴有严重营养不良、精神障碍或不愿参与本研究者。其中,男63例、女27例,年龄27~69岁、平均46.5岁,乙肝表面抗原阳性72例。本研究经黄冈市中心医院医学伦理委员会批准,患者或其家属知情同意。
人肝癌细胞株Huh7,购自中国典型培养物保藏中心。鼠抗人PD-L1单克隆抗体,美国Proteintech公司;鼠抗人MDR1、β-actin单克隆抗体,美国Santa Cruz公司。即用型SABC免疫组化染色试剂盒,北京中杉金桥生物技术有限公司。TRIzol、SYBR®Green PCR Master Mix、Lipofectamine2000,美国Life Technologies公司;RIPA裂解液,美国Sigma公司。PD-L1过表达质粒pEGFP-PD-L1,由上海吉凯基因化学技术有限公司合成。所有引物序列由武汉谷歌生物科技有限公司设计合成。
1.2 原发性肝癌组织及其配对的癌旁正常组织PD-L1、MDR1表达检测 采用免疫组化法。取手术切除的原发性肝癌组织及其配对的癌旁正常组织,4%多聚甲醛固定,梯度乙醇脱水,二甲苯透明,石蜡包埋,3 μm厚连续切片;将切片置于65 ℃烤箱内烤片2 h,二甲苯脱蜡,梯度乙醇脱水,3%过氧化氢溶液室温孵育10 min,阻断内源性过氧化物酶活性;10%山羊血清封闭,37 ℃孵育1 h,分别加入鼠抗人PD-L1单克隆抗体、鼠抗人MDR1单克隆抗体、鼠抗人β-actin单克隆抗体,4 ℃孵育过夜;次日,滴加山羊抗鼠二抗,37 ℃孵育30 min;DAB显色,苏木素复染,梯度乙醇脱水,二甲苯透明,中性树胶封固,显微镜下观察。采用双盲法由两位经验丰富的病理科医师独立阅片,结果有争议时请第三位病理科医师阅片,以两个相同结果为准。PD-L1阳性染色定位于细胞质或细胞膜,呈棕黄色颗粒;MDR1阳性染色定位于细胞膜,呈棕黄色颗粒。参照文献[4,9]评判PD-L1、MDR1阳性表达情况。
1.3 PD-L1过表达对MDR1表达的影响
1.3.1 细胞传代培养 Huh7细胞复苏后,接种于含10% FBS的DMEM培养基,置于37 ℃、5% CO2、饱和湿度的细胞培养箱中培养。每2 d换液一次,待细胞生长融合约80%时,按1∶4传代。取传3代、对数生长期细胞用于后续实验。
1.3.2 质粒转染 取传3代、对数生长期Huh7细胞,接种于6孔板,每孔6×105个。随机分为观察组、对照组,每组设3个复孔。将6孔板置于37 ℃、5% CO2、饱和湿度的细胞培养箱培养。待细胞生长融合约60%时,观察组和对照组分别加入1.2 μg Lipofectamine2000包裹的pEGFP-PD-L1和pEGFP-N1质粒,37 ℃、5% CO2、饱和湿度的细胞培养箱继续培养48 h。
1.3.3 PD-L1、MDR1 mRNA和蛋白表达检测 ①PD-L1、MDR1 mRNA表达:采用real-time PCR法。收集两组继续培养48 h细胞,TRIzol法提取细胞总RNA,经紫外分光光度计鉴定,提取的细胞总RNA浓度和纯度合格。取总RNA 1 μg,按cDNA逆转录试剂盒说明逆转录为cDNA。以cDNA为模板,按照SYBR®Green PCR Master Mix(2×)试剂盒说明进行PCR扩增。引物序列:PD-L1上游引物5′-TTCAGGGACGGATAAAGCTG-3′,下游引物5′-CGTCTCTGAGCTTCACGTTG-3′,扩增温度59 ℃,扩增产物片段93 bp;MDR1上游引物5′-ATATCAGCAGCCCACATCAT-3′,下游引物5′-GAAGCACTGGGATGTCCGGT-3′,扩增温度60 ℃,扩增产物片段154 bp;β-actin上游引物5′-AGTTGCGTTACACCCTTTCTTGAC-3′,下游引物5′-GCTCGCTCCAACCGACTGC-3′,扩增温度60 ℃,扩增产物片段171 bp。PCR反应体系共20 μL:cDNA模板1.5 μL,上下游引物各0.2 μL,SYBRGreen Mix 10 μL,ddH2O 8.1 μL;反应条件:94 ℃ 30 s,95 ℃ 10 s、60 ℃ 30 s共33个循环,最后95 ℃ 15 s、60 ℃ 60 s、95 ℃ 15 s。以β-actin为内参,采用2-ΔΔCT法计算目的基因相对表达量。实验重复3次,取平均值。②PD-L1、MDR1蛋白表达:采用Western blotting法。收集两组继续培养48 h细胞,RIPA裂解液提取细胞总蛋白,BCA法蛋白定量合格。然后加入上样缓冲液,100 ℃水浴,使蛋白充分变性。取变性蛋白20 μg,SDS-PAGE(5%浓缩胶、12%分离胶)分离蛋白。电泳结束,将蛋白电泳产物转印至PVDF膜上,5%脱脂奶粉封闭1 h,分别加入鼠抗人PD-L1、MDR1、β-actin单克隆抗体,4 ℃孵育过夜。次日,加入辣根过氧化物酶标记的二抗,室温孵育1 h,ECL发光,暗室中显影、定影。采用Image J软件分析各蛋白电泳条带灰度值。以β-actin为内参,以目的蛋白电泳条带灰度值与内参蛋白电泳条带灰度值的比值作为目的蛋白相对表达量。实验重复3次,取平均值。
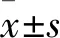
2 结果
2.1 原发性肝癌组织及其配对的癌旁正常组织PD-L1、MDR1表达比较 原发性肝癌组织与癌旁正常组织PD-L1阳性表达率分别为57.8%(52/90)、26.7%(24/90),MDR1阳性表达率分别为55.6%(50/90)、30.0%(30/90)。原发性肝癌组织PD-L1、MDR1阳性表达率均明显高于癌旁正常组织(P均<0.01)。
2.2 原发性肝癌组织PD-L1表达与MDR1表达的关系 90例份原发性肝癌组织中,PD-L1阳性表达52例份,其中MDR1阳性表达42例份、阴性表达10例份;PD-L1阴性表达38例份,其中MDR1阳性表达8例份、阴性表达30例份。Spearman秩相关分析显示,原发性肝癌组织PD-L1表达与MDR1表达呈正相关关系(r=0.594,P<0.01)。
2.3 两组转染48 h PD-L1、MDR1表达比较 见表1。

表1 两组转染48 h PD-L1、MDR1表达比较
注:与对照组比较,*P<0.01。
3 讨论
近年来,原发性肝癌的发病率呈明显上升趋势,全世界每年约有70万新发病例。目前,原发性肝癌的总体治疗效果仍不理想,大部分患者因肿瘤转移而丧失根治性手术治疗机会,化疗成为中晚期肝癌综合治疗的重要手段,但MDR现象导致化疗效果明显下降[7]。因此,逆转MDR成为近年肝癌治疗中的研究热点。
肝癌的发生是一个多基因参与、多途径调控的复杂过程,免疫抑制和免疫逃逸在其发生、发展过程中具有重要作用。研究发现,免疫抑制与免疫逃逸和肿瘤细胞PD-L1过表达密切相关[2,3]。肿瘤细胞表面的PD-L1与T细胞表面的PD-1结合,可使T细胞不能识别和杀伤肿瘤细胞,导致肿瘤细胞免疫逃逸[2,3]。临床研究发现,多种肿瘤组织PD-L1高表达,且其表达越高,患者预后越差[10~13]。本研究结果显示,原发性肝癌组织PD-L1阳性表达率明显高于癌旁正常组织,与以往报道一致。除了肝癌细胞免疫抑制和免疫逃逸外,在综合治疗过程中还易出现化疗耐药现象。目前认为,化疗耐药的产生与肝癌细胞中耐药蛋白过表达密切相关。其中,MDR1及其蛋白产物P-gp与肝癌化疗耐药的关系最为密切[7,8]。P-gp是一种跨膜糖蛋白,具有能量依赖性药泵功能,能主动将肿瘤细胞内的化疗药物泵至细胞外,降低肿瘤细胞内药物浓度,从而产生耐药性[7,8]。本研究结果发现,原发性肝癌组织MDR1阳性表达率明显高于癌旁正常组织,与以往文献[7,8]报道一致。有研究认为,肝癌组织MDR1高表达的原因与缺氧、低糖微环境及HBV感染有关[14,15]。本研究结果发现,原发性肝癌组织PD-L1表达与MDR1表达呈正相关关系,说明PD-L1过表达也可能是引起肝癌MDR的原因之一。为进一步观察PD-L1表达与MDR1表达的关系,本研究观察了PD-L1过表达对肝癌Huh7细胞MDR1表达的影响,结果发现,观察组转染48 h PD-L1、MDR1 mRNA和蛋白表达均明显高于对照组。说明PD-L1除了参与肝癌细胞的免疫抑制和免疫逃逸外,还可参与肝癌的化疗耐药。
综上所述,原发性肝癌组织PD-L1表达明显升高,其表达变化可能与肝癌化疗耐药有关。

