应用RT-PCR-RFLP鉴别2014年新余市麻疹病毒感染病例
文奇 ,廖秀海 ,潘虹 ,胡传琛 ,龚甜 ,李健雄
(1.新余市疾病预防控制中心,江西 新余 338000;2.江西省疾病预防控制中心,江西 南昌 330029)
麻疹是麻疹病毒引起的一种传染性很强的急性呼吸道疾病,在疫苗可预防的病毒性传染病中,麻疹的发病数和死亡数位居前列[1]。消除麻疹是全球共同致力于实现的目标[2]。中国大陆作为WHO西太区成员之一,自2006年开始实施消除麻疹行动计划和方案,通过落实含麻疹成分疫苗(Measles-containing Vaccine,MCV)接种、加强麻疹监测和疫情调查处置等综合消除措施,麻疹报告发病率自2009年逐年下降,而2012年之后却有所回升[3-5],麻疹消除工作面临较大的挑战。加强MCV适龄儿童的基础免疫接种、开展特定人群的补充免疫活动(Supplementary Immunization Activity,SIA)仍是当前消除工作的首要任务。监测发现,少部分人在MCV接种后出现发热、出疹症状,这些病例究竟是疫苗相关麻疹病例还是偶合感染麻疹野病毒[6-8],需要认真对待并加以区分。本文引进周剑惠、龚甜等人创建的麻疹疫苗株与野毒株鉴别方法[9,10],用以鉴别新余市2014年部分麻疹确诊病例,现将有关分析情况进行报告。
1 材料与方法
1.1 标本来源 2014年新余市辖区内共采集47例麻疹疑似病例咽拭子标本,市疾控中心对这些标本进行麻疹、风疹病毒核酸检测。选择8例麻疹病毒核酸检测阳性的病例标本作为研究对象,选择北京天坛生物公司的麻疹风疹联合减毒活疫苗(内含S191麻疹疫苗株,批号:201501007)作为阳性对照,各选取1例2014年麻疹和风疹病毒核酸检测均阴性、风疹核酸检测阳性的病例标本作为阴性对照,编号分别为M1409、M1424。
1.2 麻疹病毒RNA提取 根据Qiagen公司的RNeasy Mini Kit试剂盒 (Cat.No:74106,Lot No:145022097)说明书提取麻疹病毒RNA。
1.3 RT-PCR扩增麻疹病毒H基因 采用Qiagen公司 One Step RT-PCR Kit试剂盒(Cat:210212,Lot No:148047795)进行 RT-PCR 反应。上游引物:5′-CTCAATCGAGCATCAGGTCA-3′,下游引物:5′-TACATTCCCTGGGACGTCAT-3′。 RT 反应条件:60℃ 1min,42℃ 10min,50℃ 30min,95℃ 15min。PCR 循环如下:94℃ 30s,50℃ 30s,72℃ 60s,30 次循环,72℃ 10min,在 MJ Research PTC-200 仪器上进行扩增,扩增片段长度为438bp。
1.4 RFLP分析 每份RT-PCR产物均设立对照管和RFLP管,对照管为10μl的DNA产物,RFLP管为酶切产物,酶切反应体系是:Takara公司AflII限制 性 酶 (Lot No:1236A)1μl, 缓 冲 液 2μl,DNA 10μl,37℃下酶切 1h。麻疹疫苗株 (A基因型)被AflII酶切成287bp和151bp 2个片段,而麻疹野病毒(非A基因型)不能被酶切。
1.5 电泳 One Step RT-PCR扩增产物及其RFLP产物采用1.5%琼脂糖凝胶、北京六一产的DYY-6C型电泳仪电泳 1h,BIO-RAD公司 Universal HoodⅡ凝胶成像仪观察电泳结果。
2 结果
2.1 2014年新余市麻疹、风疹阳性病例特征 2014年新余市共检测47例麻疹疑似病例标本,检出麻疹核酸阳性11例、风疹核酸阳性2例。这些阳性病例中,男、女比例为 1.17:1;MCV 接种史情况如下:0次的有3例 (均为<8月龄的婴儿),1次的有2例 (其中1例为首剂MCV接种第10d出疹的患儿,编号为M1415),2次的有1例,接种史不明的有7例(其中5例>15岁);<8月的小月龄人群和>15岁的大年龄人群的人数占总阳性病例数的61.5%(8/13)。
2.2 麻疹病毒H基因的RT-PCR-RFLP结果分析选取的新余市麻疹阳性标本 M1415、M1430、M1431、M1432、M1434、M1435、M1436、M1443 在AflII酶切前、后仅可见大小约438bp的RT-PCR产物 (未被酶切消化),2例阴性对照标本M1409、M1424均未出现扩增产物,而阳性对照S191麻疹疫苗株的RT-PCR产物可被酶切成大小约为287bp、151bp的两个片段(图 1),表明 2014年新余市被分析的8例麻疹病例(包括MCV首剂接种第10d出疹的患儿)均为麻疹野病毒感染所致。
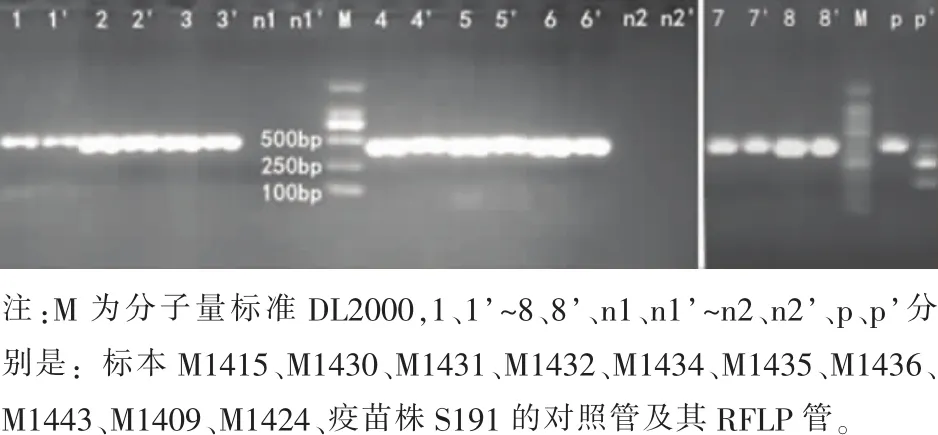
图1 新余市2014年部分麻疹病毒H基因RT-PCR产物及其RFLP产物电泳图谱
3 讨论
目前我国儿童实行2剂次的MCV免疫程序,即8月龄接种第1剂(麻疹-风疹联合疫苗),18月龄~24月龄接种第2剂 (麻疹-流腮-风疹联合疫苗)[11]。MCV接种后若出现发热、出疹症状,存在以下三种情形:一是由于疫苗中微量的鸡胚细胞、小牛血清和抗生素等杂质引起的过敏反应,通常在接种后十几小时或几十小时内产生一过性皮疹[12,13],大约有 2%的受种者出现此类反应[14,15];二是人工感染,疫苗中的减毒活病毒在机体内复制、产生免疫应答而形成的疫苗相关病例[16],一般发生在接种后1~2周内[17],多见于首次接种MCV的婴儿[18];三是偶合感染麻疹野病毒或其他发热出疹性疾病,在接种疫苗时已处在发病的潜伏期[18]。在麻疹消除工作的关键时期,如何从病原学方面鉴别MCV受种者感染的麻疹病毒是疫苗株还是野生株,是个值得深究的课题。
基因序列分析无疑是最准确、可靠的方法,但在基层实验室受条件所限,只能将标本外送测序,不仅费时费力,而且代价昂贵,难以大范围推广运用。周建惠等人受到Mori的启发[19],建立了利用RT-PCR-RFLP方法来鉴别中国麻疹病毒疫苗株与野生株的检测技术。她们在研究中国麻疹病毒疫苗株与23种野生代表株的基因差异后,发现疫苗株H基因7666bp~7671bp上存在AflII酶切位点(CTTAAG),其长度为438bp的目的扩增片段可被AflII酶切成287bp、151bp的2个片段,23种野生株在相应位置均无AflII酶切位点却不被酶切消化,借此区分麻疹病毒疫苗株与野生株。相比于序列分析,RT-PCR-RFLP方法简便、快速,更具经济实用性,非常适合基层实验室使用。
在江西省疾控中心疾检所工作人员的协助下,我们成功引进并验证了上述麻疹病毒的RT-PCR-RFLP鉴别技术。疫苗株S191的扩增产物被AflII酶切成大小约为287bp、151bp的2个片段,2例麻疹阴性标本 (含1例风疹阳性标本)未被扩增,8例待分析的麻疹阳性病例标本成功得到扩增但不被AflII酶所消化,说明8例麻疹阳性病例均由麻疹野病毒所引起的,这与我省宜春市的报道相一致[20];M1415患儿在MCV接种时已偶合感染麻疹野病毒,不属于疫苗相关病例。另外通过对新余市2014年麻疹、风疹病例信息进行分析,我们发现这些阳性病例几乎不体现出性别差异,年龄分布呈“双向移位”趋势,主要是<8月的婴儿和>15岁的人群,原因是<8月的婴儿尚未接种疫苗,而>15岁的人群常为无MCV接种史。

