太湖蓝藻多糖应用于重金属离子吸附
黄依佳,吴剑荣,朱 莉,詹晓北
(江南大学生物工程学院糖化学与生物技术教育部重点实验室,江苏无锡214122)
蓝藻水华是世界上普遍存在的环境问题,其中微囊藻是一种常见蓝藻,其产生的蓝藻毒素危害人类和动物的健康[1-2]。蓝藻是以菌落的形式或聚集体趋向于飘浮,成长后期蓝藻细胞破裂释放蓝藻毒素,严重影响湖泊、河水的质量[3]。蓝藻含有丰富的蛋白、色素和多糖,具有潜在应用价值[4],例如,蓝藻可以制造成生物塑料,还用于堆肥做肥料或发酵产沼气。其他藻类应用中,螺旋藻藻蓝蛋白已用于化妆品商业生产[5],藻类多糖具有抗氧化[6]、抗病毒[7]、抗肿瘤[8]和吸附重金属[9-10]等作用。目前打捞蓝藻成为治理太湖主要手段,但是打捞蓝藻的资源化利用成为瓶颈,如何较高附加值利用打捞蓝藻成为关键问题。蓝藻蛋白质经过水解可以制成富营养多肽、氨基酸混合液,用于饲料[11]或微生物营养[4],而蓝藻多糖的资源化利用研究相对比较少。
铅、镉等重金属污染是工业生产过程中排入水体或土壤的,这会造成环境问题[12]。一般用吸附法治理铅、镉等重金属污染,传统吸附剂主要包括活性炭、硅藻土和壳聚糖等,这些吸附剂的吸附时间长且平衡吸附容量仅为8~10 mg/g,同时价格昂贵[13]。鉴于成本和环境治理综合考虑,可以使用环境友好的天然吸附剂来吸附铅、镉等重金属,例如植物细胞壁中的纤维素、半纤维素、果胶和木质素作为主要成分作为可重金属再生的吸附剂[14]。另外,许多生物吸附剂如细菌、酵母和真菌也可用于重金属的去除[15]。微生物多糖作为新型吸附剂,优点是多糖官能团的吸附位点和离子之间的相互作用[16],能很好地吸附金属离子。
本研究旨在采用超声波辅助热水浸提的方法提取蓝藻多糖,然后将其应用于重金属离子吸附测试,以期综合利用大量打捞的蓝藻资源,并将蓝藻多糖应用于重金属吸附中。
1 材料与方法
1.1 材料
蓝藻粉,无锡德林海公司;其余所用试剂均为市售分析纯。
1.2 仪器与设备
SpectrAA-220/220Z型原子吸收分光光度计,美国瓦里安公司;傅里叶变换红外光谱仪,美国尼高力仪器公司(NEXUS)。
1.3 方法
1.3.1 蓝藻多糖的提取
称取干燥蓝藻粉末以液料比30∶ 1 mL/g加入水中,超声处理30 min(400 W、20 kHz),再在60 ℃、100 r/min条件下振荡3 h,然后于8 000 r/min离心10 min,沉淀经相同体积水浸提1次,离心后合并上清即为多糖提取液。上清液中加入5倍体积的95%乙醇,4 ℃静置过夜后沉淀即为蓝藻粗多糖,烘干称质量。
1.3.2 蓝藻多糖对水溶液中重金属离子Pb2+和Cd2+的吸附
在1 L烧杯中装入1 000 mL质量浓度为500 mg/L的Pb2+和Cd2+溶液,然后精确称取80.0 mg蓝藻多糖复溶成20 mL多糖溶液,装入经过预处理的透析袋中,透析袋两端用封口夹夹好后放入装有Pb2+和Cd2+溶液的烧杯中,在室温下置于磁力搅拌器上以120 r/min的速度进行搅拌。
吸附3 h后取出透析袋,放入装有去离子水的烧杯中进行搅拌透析,以去除未被蓝藻多糖结合的Pb2+和Cd2+,期间每隔2 h换1次去离子水,10 h后取出透析袋,将透析袋内的溶液倒入到25 mL的容量瓶中定容,将定容后的溶液进行消解。用同等体积的去离子水代替蓝藻多糖溶液,其他条件不变,作为空白实验,各实验分别进行3次平行实验。平衡吸附量Q的计算具体见式(1)。
(1)
式中:ρf为吸附后透析袋内的重金属质量浓度,mg/L;ρ0为吸附铅透析袋内的重金属浓度,mg/L;V为透析袋内总体积,mL;m为装入透析袋内的蓝藻多糖的质量,mg。
1.3.3 重金属含量测定
采用原子分光光度计测量Pb2+和Cd2+的浓度,重金属含量检测方法参照贡小清等[17]所述方法。
1.3.4 等温吸附模型
等温吸附模型通过考察吸附剂的吸附能力,采用热力学模型拟合后可通过相关方程参数分析其热力学吸附机制,常用Langmuir和Freundlich等温吸附方程对吸附等温线进行拟合[18]。
Langmuir吸附等温式最初用来描述理想均匀基质表面的单分子层气固吸附,现也已多用于固液吸附过程,其模型方程见式(2)。
Ce/Qe=1/kLQm+Ce/Qm
(2)
式中:kL为Langmuir等温吸附平衡常数,L/mg;Qm为饱和吸附量,mg/g;Ce为平衡质量浓度,mg/mL;Qe为平衡吸附量,mg/g。分别以Ce、Ce/Qe为横、纵轴,线性拟合得直线方程,通过方程的斜率1/Qm以及截距1/kLQm,分别计算出Qm和kL。
Freundlich热力学模型为经验模型,假定吸附发生于非均匀基质表面,且为多分子层吸附,适用浓度范围广,其模型方程见式(3)。
lgQe=lgkF+1/nlgCe
(3)
式中:kF、n为Freundlich等温方程参数。分别以lgCe、lgQe为横纵轴,线性拟合得直线方程,通过方程的斜率1/n以及截距lgkF,分别计算出n和kF。
1.3.5 红外光谱分析
取冻干的多糖样品和吸附重金属铅和镉后的多糖样品1~2 mg分别与溴化钾按1∶ 200的比例研磨,压片后检测利用红外光谱在4 000~4 00 cm-1范围内进行检测。
2 结果与讨论
2.1 蓝藻多糖的提取结果
热水提取法常用于天然多糖的提取,另外在热水浸提的同时,采用一些辅助方法(如超声波处理)可以有效提高多糖的得率[19-20]。考察蓝藻多糖提取条件,结果见图1。
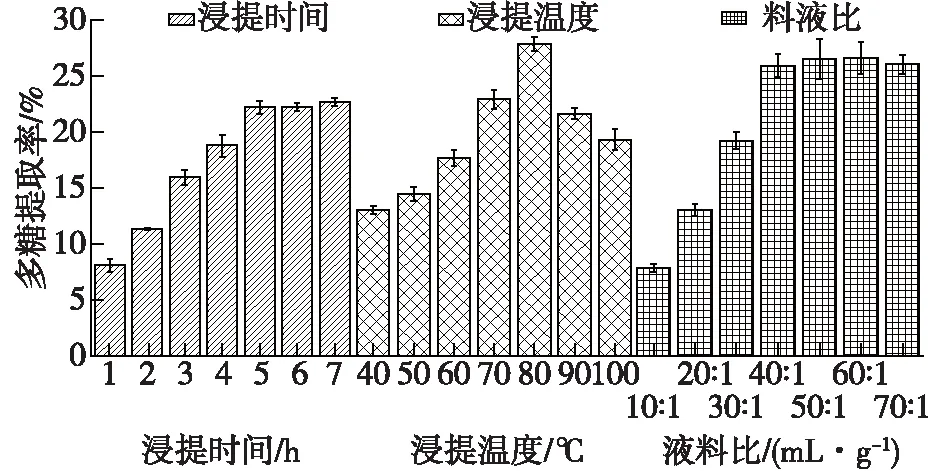
图1 不同条件对蓝藻粗多糖提取率的影响Fig.1 Effects of different conditions on isolation of Cyanobacteria polysaccharide
由图1可知:随着料液比由10∶ 1提高至40∶ 1,蓝藻多糖得率由6.5%提高至最高21.5%,蓝藻胞外多糖存在于荚膜或黏液层,液料比的增加可以加速胞外多糖的流出[21]。较高温度可以促使细胞上多糖释放或溶出,随着温度升高多糖得率增加,在温度为80 ℃时多糖得率达到25.1%;当温度高于80 ℃则多糖得率降低,可能是因为高温下多糖与其他物质反应,使溶出多糖减少。另外,随着提取时间的增加,多糖得率升高,但超过5 h后不再增加。最终确定蓝藻多糖提取条件为料液比40∶ 1 mL/g、浸提温度80 ℃下提取5 h。
2.2 蓝藻多糖投加量对Pb2+和Cd2+吸附的影响
蓝藻多糖主要存在于细胞外部,在水体中能使蓝细菌聚集成团。由于蓝藻多糖结构上含有大量羟基和羧基,因此能够与水体中金属离子发生相互作用。为了测试提取的蓝藻多糖是否具有应用于吸附重金属的潜力,将蓝藻多糖装入透析袋后置于重金属溶液中进行吸附实验。考察不同蓝藻多糖的投加量对重金属离子Pb2+和Cd2+吸附的影响,结果如图2所示。
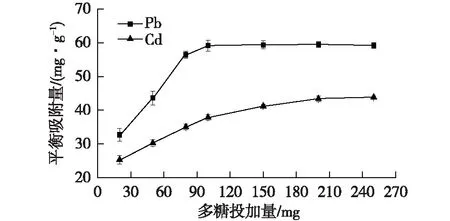
图2 蓝藻多糖投加量对Pb2+、Cd2+吸附的影响Fig.2 Effects of Cyanobacteria polysaccharide addition on adsorption of Pb2+ and Cd2+
由图2可知:随着蓝藻多糖投加量的增加,Pb2+和Cd2+的吸附效率也增加。当多糖投加量从20 mg增加到100 mg时,Pb2+的吸附效率增加了44.7%;当多糖投加量从20 mg增加到150 mg时,Cd2+的吸附效率增加了38.5%。当多糖投加量超过150 mg时,Pb2+和Cd2+的吸附效率基本持平。多糖投加量提高会增加吸附基团数量,使重金属吸附效率提高;但在固定体积的透析袋内,金属离子通过渗透进入膜内与多糖相互作用,当蓝藻多糖过量时,一方面多糖之间相互作用可能抑制与重金属结合,另一方面金属离子进入多聚糖核心需要更大浓度梯度差[22]。吸附剂用量的进一步增加导致吸附能力下降,这可能导致溶液中金属离子在表面多糖吸附位点的聚集,降低整体吸附表面积[23]。活性炭吸附能力强,吸附Cd2+吸附容量仅为8.45 mg/g,且价格昂贵,很难达到工业要求,应用受到限制[24];壳聚糖在酸性条件下易发生质子化,吸附效果没有生物吸附效果好,在pH为5、25 ℃条件下,Cd2+的吸附容量仅达到9.1 mg/g[25]。
2.3 吸附时间对蓝藻多糖吸附Pb2+和Cd2+的影响
在pH为7.0、25 ℃条件下进行,多糖投加量为80 mg,Pb2+和Cd2+的质量浓度都为500 mg/mL,考察蓝藻多糖对吸附Pb2+和Cd2+的平衡吸附量,结果如图3所示。
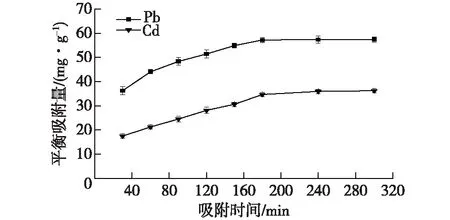
图3 吸附时间对多糖吸附Pb2+、Cd2+的影响Fig.3 Effects of treating time on adsorption of Pb2+ and Cd2+ by Cyanobacteria polysaccharide
由图3可以看出,重金属吸附过程经历快速吸附、缓慢吸附和平衡3个阶段。在0~150 min时为多糖吸附的快速阶段,Pb2+的平衡吸附量从36.2 mg/g上升到54.9 mg/g,而Cd2+的平衡吸附量从17.5 mg/g上升到30.6 mg/g;后面的60 min为缓慢吸附阶段,3 h之后基本持平,Pb2+和Cd2+的平衡吸附量分别为57.2和36.2 mg/g。在重金属吸附过程中,蓝藻多糖的吸附位点随着时间的延长逐渐减少,由快速吸附逐渐变为缓慢吸附,最后达到吸附平衡[26]。天然沸石已成功运用到废水中取出重金属,平衡吸附时间需要达到3 h以上[13]。硅藻土是一种良好的吸附剂,但吸附时间需要8 h以上[27]。
2.4 溶液pH对蓝藻多糖吸附Pb2+和Cd2+的影响
溶液的pH是影响金属性质的重要因素,同时,pH能影响多糖基团的解离,考察pH对蓝藻多糖吸附Pb2+和Cd2+的影响,结果如图4所示。
由图4可知:在pH为2~3时,蓝藻多糖对铅、镉的吸附量都较低。随着pH的增加,蓝藻多糖对铅、镉的吸附量明显增加,铅的吸附量从pH为3时的平衡吸附量38.4 mg/g上升到pH为7时的67.9 mg/g,而镉的吸附量从25.0 mg/g上升到35.7 mg/g。可能是多糖结构上H+从官能团解吸,因此吸附剂表面带更多负电荷,从而增加金属离子对多糖自由部位的吸引力,导致高吸附能力[23]。当pH为8时,蓝藻多糖对Pb2+的吸附量为55.0 mg/g,下降了12.9 mg/g,是因为在碱性条件下,产生了Pb(OH)2沉淀,使蓝藻多糖的吸附位点减少。蓝藻多糖结构上含有羧基和羟基基团,在酸性条件下,溶液中的H+与金属离子存在排斥力,使得蓝藻多糖吸附Pb2+和Cd2+的吸附量减少[22]。
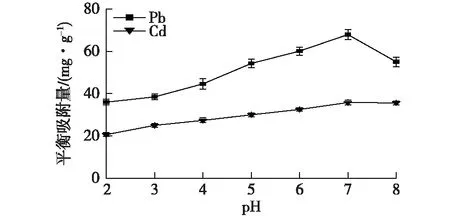
图4 pH对多糖吸附Pb2+、Cd2+的影响Fig.4 Effects of pH on adsorption of Pb2+ and Cd2+ by Cyanobacteria polysaccharide
2.5 温度对蓝藻多糖吸附Pb2+和Cd2+的影响
随着温度的变化,蓝藻多糖的平衡吸附量也逐渐变化,进一步考察温度对蓝藻多糖吸附Pb2+和Cd2+的影响,pH 7.0、多糖投加量80 mg、吸附时间3 h,结果如图5所示。
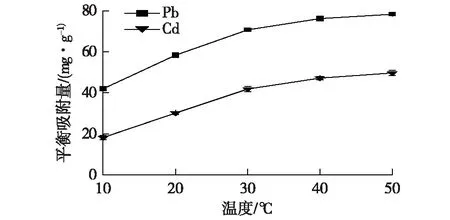
图5 温度对蓝藻多糖吸附Pb2+、Cd2+的影响Fig.5 Effects of temperature on adsorption of Pb2+ and Cd2+ by Cyanobacteria polysaccharide
由图5可知:随着温度的升高,Pb2+和Cd2+的吸附速率增大,温度从10 ℃上升到50 ℃,Pb2+的吸附量从42.0 mg/g上升到78.3 mg/g,而Cd2+的吸附量从18.3 mg/g上升到49.7 mg/g。其中,从10 ℃上升到30 ℃,吸附速率快,Pb2+的吸附速率提高了28.8 mg/g,Cd2+的吸附速率提高了23.7 mg/g;从30 ℃上升到50 ℃时,吸附速率变慢,Pb2+的吸附速率仅增加7.5 mg/g,Cd2+的吸附速率也仅增加了7.8 mg/g。这是因为随着温度的升高,分子间运动加快,加速蓝藻多糖与Pb2+和Cd2+吸附位点的接触,Pb2+和Cd2+的吸附效率变高;当温度过高时,吸附效率并没有明显的增加[23]。从节约能源角度考虑,重金属吸附适合于25 ℃下操作。
2.6 蓝藻多糖对重金属Pb2+和Cd2+的等温吸附模型
对蓝藻多糖吸附Pb2+和Cd2+的吸附等温线进行Langmuir模型和Freundlich模型线性拟合,相关参数及线性拟合方程结果如表1和表2所示。
由表1和表2可知:在不同温度下,Langmuir模型和Freundlich模型拟合方程R2均大于0.95,表明两种模型均适用于描述蓝藻多糖吸附Pb2+和Cd2+动力学过程。Langmuir模型所示的最大吸附量Qm与实际实验所得吸附量基本相近,Freundlich模型的参数n>1,表明该吸附过程为可行型吸附[28]。
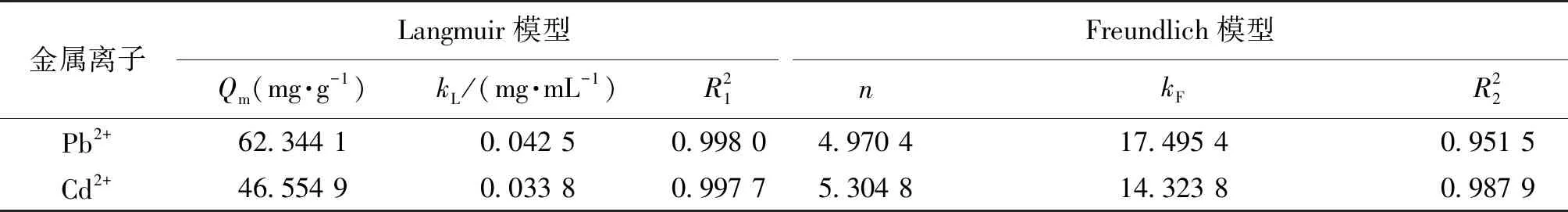
表1 在不同吸附热力学模型下的相关参数

表2 在不同吸附热力学模型下线性拟合方程式
2.7 蓝藻多糖吸附重金属Pb2+和Cd2+的机制
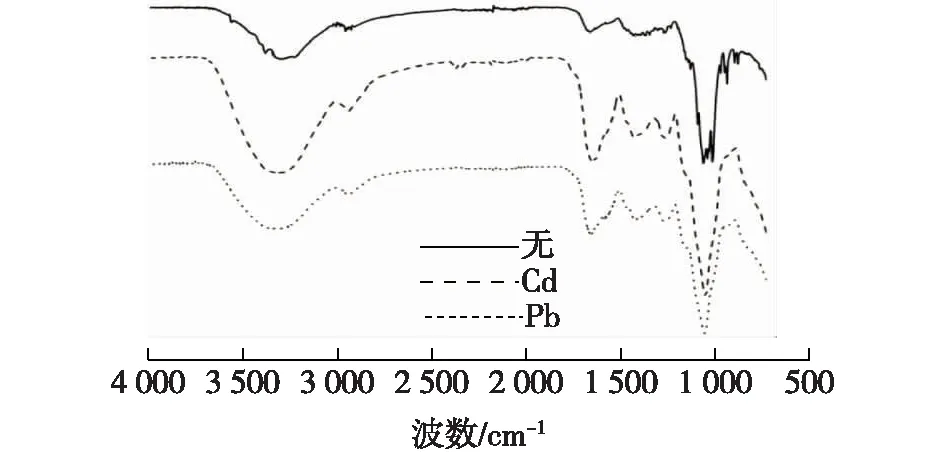
图6 蓝藻多糖原样和吸附Pb2+、Cd2+后蓝藻多糖的红外光谱图Fig.6 Infrared spectra of polysaccharides and that loaded with Pb2+and Cd2+
3 结论
在本文的研究中,建立并优化了蓝藻多糖的热水浸提方法,最终蓝藻多糖的最高得率达到25.1%,该提取方法的建立,为高效获得成本低廉的多糖产品提供了可靠方法和途径。
为了解蓝藻多糖的应用价值,本研究主要关注蓝藻多糖作为重金属离子吸附剂,应用于含有重金属离子污水的处理。因此考察并优化蓝藻多糖对Pb2+和Cd2+两种重金属离子的吸附条件。最终,经优化多糖投放量、吸附温度、吸附pH和吸附时间等条件,发现蓝藻多糖对Pb2+和Cd2+的最高吸附量分别达到62.34 mg/g和46.55 mg/g。相比目前应用较多的活性炭、壳聚糖等吸附剂,蓝藻多糖的吸附能力更强且受吸附条件的影响较小,显示了蓝藻多糖作为重金属吸附剂的应用价值和潜力。本文研究的结果,为实现综合处理太湖蓝藻及其他湖泊蓝藻并最终提高蓝藻的经济价值提供了有益的思路。

