子宫动脉化疗栓塞治疗剖宫产瘢痕妊娠的临床价值
谢志江 吕维富 胡汉金 戴家应 慈 靖
(安徽医科大学附属安庆医院放射科,安庆 246003)
剖宫产瘢痕妊娠(cesarean scar pregnancy,CSP)是剖宫产术后的远期严重并发症之一,受精卵在子宫切口处着床和发育,是临床上较少见的一种特殊的异位妊娠,占异位妊娠的6.1%[1,2]。2010年2月世界卫生组织发布报告,2007年8月~2008年5月中国剖宫产率高达46.2%[3]。随着剖宫产的增加,CSP发生率也逐年在上升,发生率为1∶2216~1∶1800[4,5]。因受精卵着床于子宫切口瘢痕处,该处局部组织血管和肌层无法适应胚胎发育需要,导致胚胎发育延缓或死亡,孕早期可出现不规则阴道流血等先兆流产现象,如不能明确诊断为CSP而盲目行刮宫治疗,可能导致流产不全、大出血甚至危及生命。子宫动脉栓塞(uterine arterial embolization,UAE)可以迅速有效控制血管损伤所致的大量子宫出血,与控制子宫大出血时常用的子宫动脉结扎术、骼内动脉结扎术或子宫切除术相比,具有微创、副作用少、术后并发症少等优点,更重要的是能够保留生育功能。2012年2月~2017年9月我院收治CSP 34例,其中16例行子宫动脉化疗栓塞(uterine arterial chemoembolization,UACE),术后联合清宫术或宫腔镜治疗,取得良好的疗效,现报道如下。
1 临床资料与方法
1.1 一般资料
本组16例,年龄26~39岁,(32.8±4.2)岁。15例因阴道出血就诊,1例因停经行妇科彩超诊断为CSP。停经时间34~81 d,(52.6±16.6)d。清宫术后大出血2例,药流后阴道流血不止1例。CSP妊娠距最近一次剖宫产时间为9个月~15 年,中位数5.5年。血清β-hCG 674.0~63 887.0 U/L,中位数18 163 U/L。术前彩超提示子宫切口处可见孕囊声像,孕囊周边见明显环状血流,孕囊最大径(5.77±3.39)cm。根据瘢痕处受精卵的深浅,CSP分为2种类型:Ⅰ型,受精卵种植于瘢痕处宫腔侧,妊娠囊向宫腔方向生长,本组8例;Ⅱ型,受精卵种植于瘢痕处深肌层,妊娠囊向膀胱、腹腔侧生长[6],本组8例。
病例选择标准:①有停经史,有(无)阴道出血和(或)腹痛等;②β-hCG阳性;③妇科腹部彩超或阴道B超提示宫腔内、宫颈内、附件区未见孕囊,子宫下段切口处有孕囊声像,孕囊周边有明显环状血流信号,回声紊乱,切口与肌层分界不清。排除标准:①严重心、肝、肾功能损伤;②过敏体质;③有严重凝血功能障碍。
1.2 方法
1.2.1 UACE 术前常规行凝血功能、血常规、血β-hCG、肝肾功能、妇科彩超检查,大出血病人备血并开通静脉通道,心电监护、吸氧、输血等。仰卧位,取右侧股动脉为穿刺点,常规消毒铺巾。采用改良Seldinger技术穿刺右侧股动脉,置入F5动脉鞘,插入F5COBRA(COOK)或F5子宫动脉(COOK)导管于两侧髂内动脉、子宫动脉造影,根据子宫内病灶血管染色及造影剂外溢情况,判断瘢痕妊娠位置、供血血管及有无血管破裂出血。无血管破裂时,表现为局部呈圆形或类圆形浓染,先于两侧子宫动脉灌注甲氨蝶呤80 mg,再用甲氨蝶呤20 mg浸泡的560~710 μm明胶海绵颗粒栓塞子宫动脉,待子宫末梢血管基本消失,子宫动脉血流明显减缓时,追加1~2条(1 mm×2 cm)明胶海绵细条栓塞子宫动脉主干,以子宫染色消失,子宫动脉呈残根样,髂内动脉其他分支通畅为栓塞满意。如果造影发现有子宫动脉血管破裂,表现为局部造影剂外溢,造影剂滞留,先超选择插管至出血子宫动脉分支行栓塞治疗后,确定无造影剂外溢时再进行上述操作。术毕穿刺点压迫15 min后加压包扎。术后给予水化、预防感染、营养支持、预防出血等治疗,失血性休克患者继续输血、补液扩容等抗休克治疗。
1.2.2 终止妊娠 UACE术后1~3 d B超引导下行宫腔镜妊娠组织切除术(CSP Ⅱ型)或清宫术(CSP Ⅰ型),妊娠组织残留者选择二次清宫或宫腔镜妊娠组织切除术,若宫腔镜妊娠组织切除术或清宫术操作困难改行腹腔镜或开腹妊娠组织切除术,出血难以控制危及生命行子宫切除术。
1.3 观察指标
UACE操作时间(手术开始到结束时间),曝光时间(实际射线使用时间),终止妊娠方式(宫腔镜妊娠组织切除/清宫术),UACE术后β-hCG恢复正常时间,月经恢复时间,终止妊娠时子宫出血量,栓塞术后不良反应及并发症(皮疹、发热、腹痛、异位栓塞、穿刺部位血肿、胃肠道反应、骨髓抑制、邻近器官缺血坏死),住院费用,住院时间。
2 结果
16例造影后提示子宫体积增大,子宫动脉增粗、扭曲,两侧子宫动脉均参与供血,且均以一侧子宫动脉供血为主,见胚囊着床位置团状造影剂浓聚,宫体上移。2例清宫大出血者造影均可见对比剂外溢,局部造影剂浓聚(图1)。UACE术后造影子宫动脉闭塞、血供完全阻断、子宫染色消失(图2)。2例清宫大出血、1例药流后阴道流血不止行UACE术后子宫出血停止。UACE操作时间15~45 min,(26.8±9.0) min;曝光时间5~15 min,(8.1±2.8)min。UACE术后清宫8例,出血量10~200 ml,中位出血量50 ml;宫腔镜切除妊娠组织7例,出血量5~150 ml,中位出血量20 ml;1例因清宫大出血行急诊UACE,二次清宫时出血较多终止清宫,MR检查提示胎盘植入,全麻下行开腹子宫切口瘢痕妊娠组织切除,胎盘穿透浆膜侵犯膀胱,术中出血1000 ml。UACE后清宫术前血β-hCG下降(20 472.1±17 076.4)U/L,下降(89.1±12.6)%。
UACE术后第1天4例轻微下腹部疼痛,2例恶心、呕吐,术后第2天2例低热,给予对症处理后均好转,无皮疹、异位栓塞、穿刺部位血肿、骨髓抑制、邻近器官缺血坏死、盆腔感染、子宫缺血坏死等并发症。住院6~28 d,(14.1±6.5)d。住院费用(15 750±5305)元。β-hCG恢复至正常时间(37.6±4.3)d。16例随访3~6个月,1~2个月后[(44.8±5.7) d]月经均恢复正常,2个月后复查性激素均正常,未出现卵巢早衰或继发性闭经等情况,2例半年后再次妊娠。
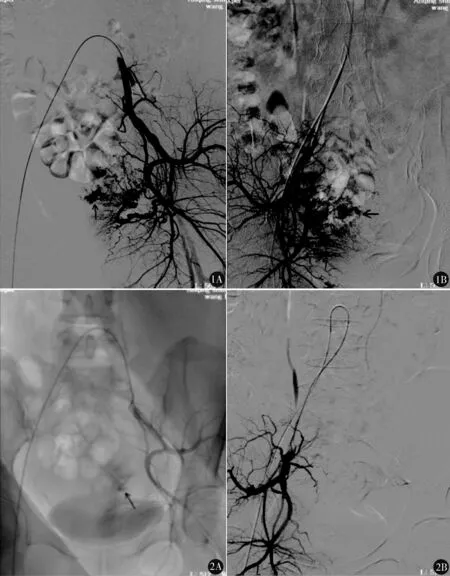
图1 UAE术前DSA A.左侧子宫动脉造影,CSP病灶显影,箭头所示子宫动脉分支破裂出血,造影剂外溢;B.右侧子宫动脉造影,箭头所示右侧子宫动脉亦参与供血 图2 UAE术后DSA:CSP病灶不显影,左侧子宫动脉远端造影剂滞留(A),近端子宫动脉呈残根样,右侧子宫动脉完全闭塞(B)
3 讨论
CSP因患病率低,常常难以引起临床的重视,往往导致误诊、误治,诊断主要根据临床表现及妇科彩超检查。临床表现:①剖宫产史;②停经史;③血/尿β-hCG升高;④阴道出血;⑤腹痛等。超声诊断标准:①子宫腔中上段位置无孕囊,宫腔下端前壁出现混合回声区;②子宫腔内无胎囊:③滋养层在膀胱和子宫前壁之间[4,7]。CSP的早期诊断很重要,在明确诊断下再行治疗,既可以减少病人痛苦,降低风险,也可以降低医疗不良事件、医疗事故的发生。
CSP是剖宫产的远期并发症,降低剖宫产率是预防其发生的重要环节。CSP可引起子宫破裂、大出血甚至危及生命,随着孕龄增加,胎盘植入、前置胎盘等相关并发症发生率也增高。目前,CSP尚无规范化统一的治疗指南,治疗目的是尽快终止妊娠,预防大出血,尽量保留子宫生育功能[8],临床治疗方法主要为保守治疗、手术治疗、介入治疗等。保守治疗是利用药物治疗来杀死胚胎组织、减少出血、保留子宫、保留生育功能等,但并不是所用保守治疗都能达到上述目的,有少数病例因保守治疗效果不佳导致子宫破裂大出血,出血难以控制而导致切除子宫[9]。手术主要方式有妊娠组织清除、双侧髂内动脉结扎及全子宫切除。患者病情较重,出血量较大,一般以急诊为主,因子宫动脉血供丰富,常伴有其他侧支供血,单纯行病灶清除或双髂内动脉结扎不能控制出血,往往需要切除子宫。切除子宫对患者损伤大,且对于那些有生育要求的患者是一个沉重的打击。经过多年的临床实践,UAE已成为妇产科急诊出血的主要治疗方法之一。CSP作为特殊的异位妊娠同样也有大出血的可能,UAE逐渐被临床认可。
UACE治疗CSP常见并发症有恶心、呕吐、发热、腹痛、神经损伤等,一般不需要特殊处理,可根据症状轻重给予适当对症处理即可;子宫缺血坏死、盆腔感染及异位栓塞极少发生[10]。本组4例出现轻微下腹疼痛,系栓塞后子宫血供减少,不能继续支持内膜生长,内膜缺血、坏死、剥脱所致,镇痛对症治疗即可[7]。2例出现低热,2例出现恶心、呕吐症状,术后无一例出现子宫坏死、盆腔感染、继发性闭经、神经损伤等严重并发症。
UACE灌注MTX最佳有效剂量为100 mg,这一剂量既可保证局部有效血药浓度,又可尽量减少MTX的不良反应。UACE的优势:①提高局部药物浓度。双侧子宫动脉MTX灌注时,药物能直接进入妊娠组织血管内,提高药物效价[11]。栓塞用明胶海绵经MTX浸泡,可以延长药物作用局部组织时间,从而提高药物效价[4,5,12]。②超选择栓塞子宫动脉可迅速控制阴道大出血、阻断胚胎血供,达到止血和提高疗效的双重作用。③栓塞后再行清宫术,出血少且避免大出血风险。④对于有生育要求的女性,可避免子宫切除,保留生育功能[13]。⑤缩短住院时间,成功率高。⑥UACE术后并发症少,恢复快。

