少见宫腔镜图像的宫腔粘连的处理
付凤仙 段 华 汪 沙 汤一群 甘 露 徐 倩
(首都医科大学附属北京妇产医院妇科微创中心,北京 100006)
宫腔粘连(intrauterine adhesion, IUA)是由各种因素导致子宫内膜基底层受损后,子宫肌壁间相互粘连,引起宫腔部分或全部闭塞的一类疾病[1],可导致不孕、反复流产、异常子宫出血、闭经、痛经或胎盘异常等。近年来,随着宫腔手术的增多,IUA的患病率不断增加,严重影响女性的生殖功能、月经生理及身心健康等。宫腔镜检查是IUA诊断的金标准,对于IUA的分类、程度、部位以及治疗方式的选择和预后评估具有重要意义。2012年3月~2016年3月我们在腹部超声监护下宫腔镜处理中、重度IUA 241例,其中12例(5.0%)宫腔镜图像较为少见,即单纯宫腔镜下IUA图像不能完整被识别,单纯宫腔镜手术处理困难,容易出现宫腔假道形成、子宫穿孔、错误识别IUA图像,报道如下,旨在为临床医师在宫腔镜手术时对于IUA少见图像的识别及处理提供帮助。
1 临床资料与方法
1.1 一般资料
本组12例,年龄25~40岁,平均31.2岁。孕产次G1~7P0~2。5例闭经,其中人工流产术后4例,外院宫腔粘连分离术后1例;月经量减少7例,月经量依据 WHO 月经失血图(pictorial blood loss assessment chart,PBAC)[2]进行量化评分,8~65分,其中胎停育清宫术后2例,人工流产术后4例,中期妊娠引产清宫术后1例。超声提示:7例重度IUA,子宫内膜厚度3~6 mm;5例中度IUA,子宫内膜厚度6~12 mm。4例外院宫腔镜检查诊断为重度IUA,其中3例临床表现为闭经,1例月经量减少。IUA的诊断和分类依据1988年美国生育协会(The American Fertility Society,AFS)分类系统[3],根据所涉及的宫腔范围,粘连类型和月经情况,将IUA分为:轻度1~4分,中度5~8分,重度9~12分。12例一般资料见表1。
病例选择标准:①20~40岁;②宫腔镜检查诊断为中度或重度IUA(AFS评分5~12分);③具有以下一种或多种临床症状,如月经量减少、反复发作的腹痛、闭经;④签署研究知情同意书并同意接受有条件随访。排除标准:①1988年版AFS IUA分类系统评分不超过4分;②其他疾病引起的月经稀发或闭经,如卵巢储备减少和多囊卵巢综合征;③有盆腔或子宫内膜异位症等急性/慢性炎症;④未提供知情同意或随访依从性差,无法进行定期随访;⑤有严重疾病,如心血管、肝脏、肾脏和不能耐受手术的血液疾病。
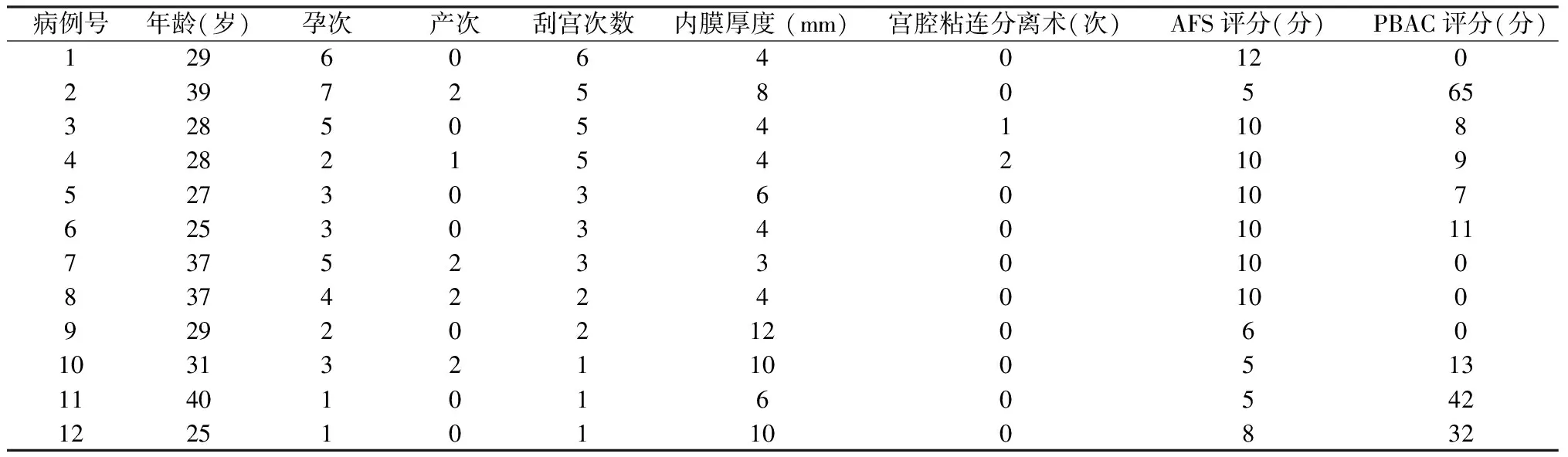
表1 12例中、重度IUA的一般资料
1.2 方法
1.2.1 手术器械 Olympus 公司4.5、5.5、6.5、8.5 mm F27被动式可旋转连续灌流宫腔检查镜和宫腔电切镜。超声诊断仪T2600实时线阵超声仪及RT3000扇扫超声仪(中国通用电气医疗系统有限公司,探头频率7.5 Hz)。
1.2.2 术前准备 完善术前化验检查,对患者进行全面的术前评估和准备,排除宫腔镜检查及手术禁忌证,膀胱适度充盈。
1.2.3 手术方法 取膀胱截石位,腹部超声检查了解膀胱适度充盈后常规消毒铺巾。设置膨宫压力80~100 mm Hg,灌流液为0.9%氯化钠,流速260 ml/min。双极电极输出功率切割280~320 W,凝固160 W。对于少见宫腔镜图像的IUA手术治疗,需要在腹部超声监护下完成,宫腔检查镜镜体在膨宫液的冲注引导直视下从子宫颈外口插入,全面观察宫颈管,若宫颈管内口和(或)宫腔中下段膜状粘连,在腹部超声监护下沿内膜线方向,采用宫腔检查镜镜体喙部推压钝性分离粘连后镜体插入宫腔,进入到宫腔底部,完全分离膜状粘连恢复宫腔正常形态后观察宫腔及双侧输卵管开口,退出镜体过程中再次观察宫颈管及宫腔情况;若宫腔镜检查显示IUA致密,宫腔检查镜镜体难以进入宫腔,则经宫颈置入宫腔电切镜,观察粘连的部位、范围与粘连性质。对于宫腔中下段致密粘连封闭的情况,在腹部超声监护下,引导探针沿内膜线方向进入宫腔后,逐渐扩张宫颈管至11号扩宫棒,先以针状电极/冷刀分离宫腔中央粘连带,随后采用电刀或冷刀切开或分离致密粘连组织,直至子宫腔恢复正常形态。手术完成的标志是在宫腔镜直视下,宫腔形态基本恢复正常,无明显粘连组织,双侧子宫角显示,输卵管开口可见和(或)不可见。宫腔粘连分离术后,5例宫腔内放置宫型节育器防止IUA,术后3个月宫腔镜二次探查+取环了解宫腔形态,2例宫腔内放置宫腔球囊(球囊内注入生理盐水分别为3.5、4 ml),术后7 d取出;5例IUA呈膜状,宫腔粘连分离后宫腔形态恢复正常,未采取预防IUA措施。
1.3 统计学处理
采用SPSS23.0进行数据分析。不符合正态分布的计量资料用中位数(最小值~最大值)表示。手术前后PBAC、AFS评分比较采用Wilcoxon Signed Ranks检验。P<0.05差异有统计学意义。
2 结果
2.1 宫腔镜检查和腹部超声监护所见及处理
7例重度IUA的粘连组织较为致密且封闭宫腔(图1、2),5例中度IUA组织呈膜状且存在数量不等的孔隙(图3、4),其中2例腹部超声监护显示宫腔中下段强回声带(图5)。在腹部超声监护下,7例宫腔镜检查提示宫腔中下段致密粘连封闭,采用电刀或冷刀切开或分离粘连组织后,宫腔形态完全恢复正常;5例采用宫腔检查镜镜体喙部推压钝性分离粘连后宫腔形态恢复正常,其中1例在腹部超声监护下宫腔检查镜镜体难以钝性推压分离粘连组织,在腹部超声监护下探针沿内膜线方向进入宫腔后宫腔检查镜镜体才得以进入宫腔底部。宫腔镜手术均顺利完成。手术时间(20±3)min,术中均未出现宫腔假道形成、子宫穿孔、TURP综合征、出血、感染等并发症。
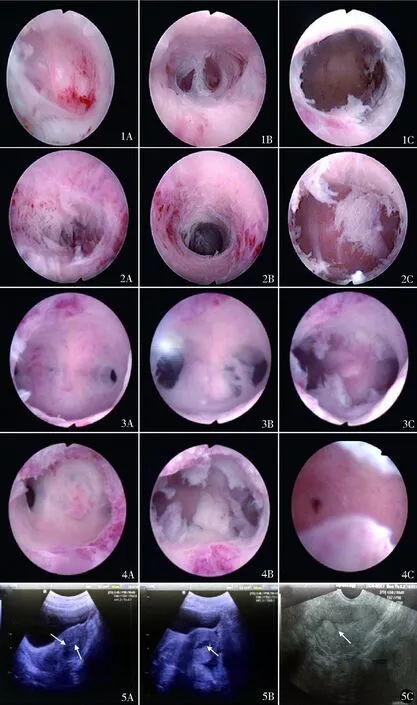
图1 A.宫腔中段粘连封闭;B.划开部分粘连后宫腔;C.完全划开粘连后宫腔图2 A.宫腔中下段粘连封闭;B.划开部分粘连后宫腔;C.完全划开粘连后宫腔图3 A.宫腔“幕样”粘连及孔隙;B.划开部分粘连后宫腔;C.完全划开粘连后宫腔 图4 A.宫腔“幕样”粘连及孔隙;B.完全划开粘连后宫腔;C.右侧输卵管开口 图5 A.宫腔镜检查前超声;B.完全划开粘连后超声;C.宫腔中段粘连带
2.2 宫腔镜术后PBAC、AFS评分比较
宫腔镜手术后PBAC、AFS评分与术前比较差异有显著性,见表2。
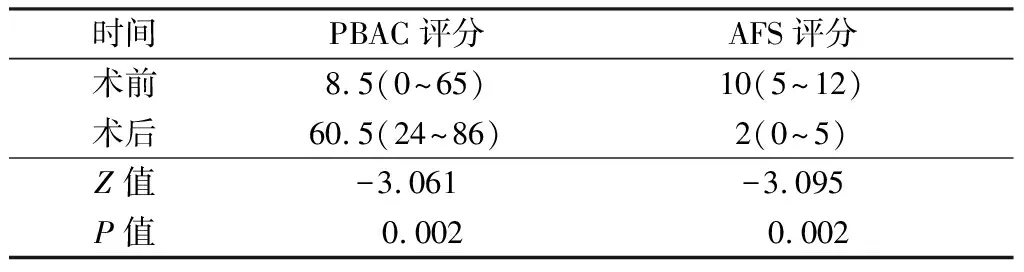
表2 12例手术前后PBAC、AFS评分比较(n=12)分
2.3 随访
12例随访3~12个月,8例有生育要求者术后妊娠5例,其中1例辅助生育,另4例无生育要求。
3 讨论
3.1 中、重度IUA宫腔镜特殊图像的特点、识别和临床意义
12例IUA既往宫腔操作史为IUA的主要病因,刮宫1~6次,就诊的主要原因为月经量减少或闭经。12例中、重IUA部分纤维性或膜状粘连把宫腔部分或完全封闭,宫腔镜下只能看到宫腔的一部分,如果无腹部超声监护宫腔检查镜镜体难以进入宫腔底部,不能完全识别宫腔的整体形态。IUA封闭7例,其中3例在外院行宫腔镜检查,均诊断重度IUA(图1、2);粘连处有孔隙4例,其中1例在外院行宫腔镜检查,诊断重度IUA(图3、4)。复读4例诊断重度IUA的镜下图像,3例IUA封闭,镜体只是到达IUA封闭处,未能进入到宫腔底部;1例IUA封闭处有孔隙,镜体几乎到达宫腔底部,但镜体全部进入到子宫内膜下方误诊为重度IUA。
中度IUA 5例,粘连处组织呈膜状且存在数量不等的孔隙,镜下图像易将孔隙误诊为输卵管开口(图3、4)。如何区分粘连处孔隙及输卵管开口,粘连处孔隙腹部超声监护显示镜体仅到达宫腔中段“幕样”粘连带处,而正常输卵管开口位于宫腔底部;同时,在膨宫压力产生变化时,双侧正常的输卵管开口对称且可见收缩呈缝隙状,而粘连处的孔隙不会产生变化;正常的输卵管开口多呈圆形或椭圆形,偶成星状或月牙状,有时可见收缩,而这种孔隙多不规则且固定。本组1例的孔隙位于粘连的两侧,4例的孔隙位于粘连一侧,似输卵管开口难以区分,但通过腹部超声监护显示粘连的位置位于宫腔中段,超声监护下当镜体划开粘连组织,完全暴露了宫腔形态,因此,排除输卵管开口的可能。
单纯宫腔镜检查或手术由于有中央型IUA的存在,阻止或障碍镜体进入到宫腔底部,不能正确反映出宫腔的整体形态,联合腹部超声监护能够有效地监护或引导镜体进入宫腔底部,从而准确而全面地反映宫腔形态,准确判断IUA的程度和范围。
3.2 腹部超声监护在宫腔中下段粘连诊断中的重要性
腹部超声监护对中、重度IUA的诊治极为重要,可帮助确定IUA程度及部位,有助于制定合理的治疗方案[4,5]。对于IUA导致的部分宫腔封闭,腹部超声监护可帮助区分出“幕样”粘连带及宫腔中下段完全粘连封闭的特殊类型。5例术前超声提示带状回声,腹部超声监护下宫腔镜检查显示宫腔中段“幕样”粘连带,镜体喙部钝性划开后宫腔形态恢复正常,术后月经恢复正常;7例粘连组织较为致密且封闭部分宫腔,在腹部超声监护下,探针沿内膜线方向进入宫腔,随后针状电极或冷刀划开粘连组织,暴露出宫腔形态。因此,对于某些少见宫腔镜图像的IUA,如宫腔中下段致密粘连和(或)部分封闭的患者,应联合腹部超声监护进行个体化诊断,单纯宫腔镜检查诊断此少见宫腔镜图像的IUA具有一定的局限性,应避免IUA程度的误诊。
术中腹部超声监护能够起到引导宫腔镜镜体进入宫腔的方向和深度,减少和(或)避免少见IUA镜下图像进行宫腔镜检查时的视野盲区,进行准确的手术定位。宫腔镜检查在腹部超声监护引导下沿宫腔内膜线方向置入镜体,超声探头在耻骨联合上方做横切与纵切,以宫腔内的膨宫液为参考,进行全方位的观察。超声监护的优越性有助于手术的定位、导向,同时可引导宫腔镜镜体喙部、电极分离或切割粘连组织的方向及深度,有效防止术中子宫穿孔、宫腔假道形成及子宫出血等并发症的发生,提高手术安全性,保障手术疗效,将复杂的手术变得容易实施[6]。Kresowik等[7]对159例宫腔镜手术进行研究,认为腹部超声监护对宫腔镜手术是一种理想的辅助措施,可有效减少子宫穿孔的发生,且降低手术费用。
腹部超声监护宫腔镜手术时,如粘连组织中含有大量纤维肌性成分和结缔组织成分,可采用电刀或冷刀切开或切除。若粘连组织呈现膜状,甚至出现一个或多个孔隙的时候,通过镜体的喙部逐渐划开粘连组织后完全暴露宫腔形态。Coccia等[8]研究显示超声监护下宫腔灌注可仅依靠机械力分离轻度或中度的中央型粘连组织,效果良好。本组7例采用电刀或冷刀切开或切除致密粘连组织,5例膜状/纤维性粘连处有孔隙,通过镜体的喙部钝性划开孔隙,恢复宫腔正常或大致正常形态。
3.3 子宫内膜厚度在IUA程度形态判定中的重要性
测量子宫内膜厚度对IUA程度的评估具有一定指导意义,通常重度IUA患者的子宫内膜基底层破坏严重,子宫内膜厚度3~4 mm,甚至更薄。7例重度IUA子宫内膜厚度3~6 mm,5例中度IUA子宫内膜厚度6~12 mm。Schlaff等[9]报道术前超声测量重度IUA患者子宫内膜厚度可预测其治疗预后,提出子宫内膜厚度越厚,术后患者越有可能恢复正常宫腔形态及月经量。12例子宫内膜厚度平均6.2 mm,4例外院宫腔镜检查提示重度IUA,子宫内膜厚度平均6.5 mm,其中1例子宫内膜厚度达到12 mm,分析本例第1次宫腔镜检查诊断为重度IUA的镜下图像,考虑镜体未能穿过宫腔中段的粘连带,进入宫腔底部,但误入子宫内膜下方,镜体在子宫内膜下方进入到宫腔底部;第2次腹部超声监护宫腔镜检查,超声监护显示镜体进入到宫腔中段,并观察到粘连处左侧有一小孔隙,镜体沿孔隙划开粘连后进入宫腔底部,见到宫底及双侧输卵管开口,宫腔形态恢复正常。6例子宫内膜厚度6~12 mm,宫腔镜检查均提示宫腔中央型纤维性和(或)膜状粘连,宫腔检查镜镜体推压钝性分离粘连后宫腔形态恢复正常或大致正常;6例超声提示子宫内膜厚度3~4 mm,宫腔镜检查提示宫腔中下段致密粘连封闭,其中1例在腹部超声监护下宫腔检查镜镜体难以钝性推压分离致密粘连,在腹部超声监护下探针探查进入宫腔后宫腔检查镜镜体才进入宫腔。12例AFS评分中位数从术前从10分(4~12分)下降至术后2分(0~5分)(Z=-3.095,P=0.002),术后月经量评分由术前中位数8.5分(0~65分)增加至60.5分(24~86分)(Z=-3.061,P=0.002)。此外,超声不仅可测量子宫内膜厚度,还可观察到子宫内膜的完整性,包括内膜下肌层与宫腔内粘连带的相互关系[10]。因此,术前超声测量子宫内膜厚度可预测IUA的程度,对于指导后续治疗及预后评估具有一定意义。
宫腔镜手术是IUA的标准诊治方法,医生需要结合个人经验、IUA程度和类型为每一位患者选择个体化的治疗方案。虽然宫腔镜检查是IUA诊断的金标准,但仅用宫腔镜检查对于某些少见镜下图像表现的IUA程度的判断具有一定局限性。对IUA的诊治,联合腹部超声监护更能准确判断IUA的程度和范围,进而能够选择恰当的治疗方式。此外,术中腹部超声监护可以进行准确的手术定位,提高宫腔镜手术治疗的安全性和成功率,能够较好地保证手术疗效。本研究病例少,需要扩大样本量,进一步总结临床数据并提供更好的临床经验。

