改良式抵钉座绑线反穿法在结直肠经自然腔道取标本手术消化道重建中的应用
段吉清 张路遥 孙东辉
(吉林大学白求恩第一医院胃肠外科,长春 130021)
经自然腔道取标本手术(natural orifice specimen extraction surgery,NOSES)是使用腹腔镜器械或经肛门内镜显微手术(transanal endoscopic microsurgery,TEM)器械以及软质内镜等设备完成腹腔内操作,经自然腔道(直肠或阴道)取出标本的腹壁无辅助切口手术,术后腹壁仅留几处trocar瘢痕[1]。与自然腔道内镜手术(natural orifice translumenal endoscopic surgery,NOTES)相比,NOSES无须切开阴道、胃等器官,经过自然腔道将标本取出,增加手术的安全性。取标本外科医师在追求手术微创的同时,也在寻求一种更为简单、快速、安全可靠的方式。在结直肠NOSES消化道重建过程中,传统的荷包缝合抵钉座吻合是常用的方式,但腹腔镜下荷包缝合抵钉座较为困难,耗时较长,且术后发生吻合口漏的几率较大。为此,我们采用一种新的方式——改良式抵钉座绑线反穿吻合器吻合法,可以使消化道重建更简便快捷和安全。2016年10月~2018年2月我科行92例结直肠NOSES,在消化道重建过程中,56例采用抵钉座绑线反穿法,36例采用传统荷包缝合抵钉座吻合,我们对2种方法进行回顾性比较,探讨结直肠NOSES消化道重建更为方便、安全的方式。
1 临床资料与方法
1.1 一般资料
本研究92例,男43例,女49例。年龄48~76岁,平均64岁。临床表现为腹部不适、排便习惯及性状改变、大便带血。肿瘤直径2.2~5.2 cm,平均3.6 cm。肠镜活检病理诊断:结肠癌37例,直肠癌55例,均单发。结肠增强CT检查支持结直肠癌诊断,影像学上未发现远处转移及侵犯周围器官。根据医生经验选择术式分成2组:A组采用改良式抵钉座绑线反穿吻合器吻合,56例;B组采用传统荷包缝合抵钉座吻合,36例。2组患者手术均由同一组医师完成。2组患者一般资料无统计学差异(P>0.05),有可比性,见表1。
病例选择标准:①术前肠镜、病理检查诊断为结直肠癌,增强CT及MRI检查无远处转移和梗阻;②肿瘤直径<6 cm;③肿瘤距肛缘5~30 cm;④患者无心、肺、肝、肾等重要脏器疾病;⑤BMI<30.0。排除标准:①术前CT考虑肿瘤侵犯周围组织;②既往有腹部手术史导致腹腔粘连。
表1 2组患者一般资料比较
1.2 方法
全身麻醉,平卧分腿位。经脐1.0 cm切口建立气腹作为观察孔,腹腔镜监视下于双侧腹直肌旁与脐水平连线、右侧髂前上棘内两横指及左侧“麦氏点”置入相应trocar。探查未见肿瘤转移后取头低右倾位。超声刀将乙状结肠系膜根部的右侧叶切开,并进入Toldt间隙,游离肠系膜下动静脉后切断。游离左侧腹膜,向上游离至降结肠上段,向盆腔游离至直肠膀胱陷凹,并于内侧平面贯通。肿瘤下方5 cm裸化肠管,腹腔镜下闭合器切断肠管,距肿瘤近端10 cm处切开预定切除肠系膜并裸化肠管。超声刀切开残端肠管,将吻合器钉座准备送入腹腔,开始消化道重建。钉座反穿法操作如下。①将吻合器抵钉座绑线并送入腹腔:钉座送进腹腔之前,在其尾部捆绑丝线。对于尖头抵钉座,若抵钉座尖端有小孔,可以把线穿过此小孔后打结,尖端没有小孔的抵钉座,可把线绑在靠近尖端的较细的部位。对于平头抵钉座,可以在靠近尾部较细部位对称绑线2根,再把这2根线拉直后于靠近抵钉座尾部处绑在一起,这种方式在抵钉座尾部从肠管内穿出时用器械稍加辅助也可顺利出来。切开保留的直肠(乙状结肠)远侧残端,于肛门置入TEM内镜,通过TEM内镜将吻合器抵钉座送入腹腔。②将吻合器抵钉座送入近侧肠端:在拟切断结肠处开始向远侧切开,切口位于系膜对侧,与肠管纵轴平行,把钉座送入近端肠管,绑线预留于肠管外。③吻合器抵钉座反穿出近侧肠管:将预留线沿着肠壁纵轴向近侧轻拉,拉直远侧肠管并使肠壁切口成线状,让镜下切割器和系膜基本平行时紧靠预留线切断肠管,将带有预留线的钉座留在近侧结肠肠腔内,提拉预留线,通过预留线处小孔将吻合器钉座的钉针穿出。这样操作就确保钉座杆从系膜对侧肠壁穿出,在钉座砧板两侧就没有2个角(俗称“狗耳朵”)。④标本取出:肿物上下肠管切断后,通过TEM内镜在腹腔镜监视下将标本自肛门完整取出。⑤消化道重建:以镜下切割闭合器闭合远侧肠管残端,经肛门置入吻合器,完成端端吻合。手术过程见图1~8。传统荷包缝合法:将抵钉座送入腹腔,超声刀切开近端肠管,沿肠管切缘做荷包缝合后将抵钉座送入近端肠管,收紧结扎缝合线。通过TEM内镜在腹腔镜监视下将标本自肛门完整取出后,远端肠管以镜下闭合器闭合,经肛门置入吻合器完成直肠-结肠端端吻合。
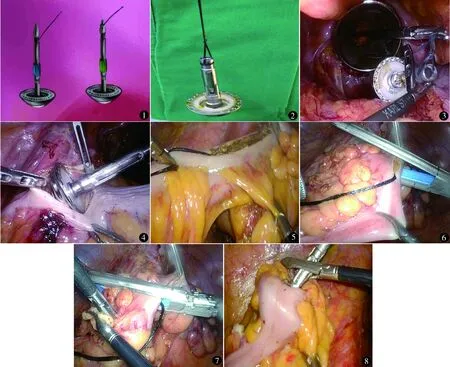
图1、2 3种不同吻合器钉簪的绑线部位及方法 图3 通过TEM内镜将吻合器抵钉送入腹腔 图4 把钉座送入近侧肠管并送到一定深度 图5 将肠壁切口拉直成线状 图6,7 将远侧肠管旋转90°,并使肠壁切口成线状,镜下切割器和系膜基本平行时紧靠预留线切断肠管 图8 吻合器钉座反穿出近侧肠管
1.3 观察指标
手术时间(建立气腹至完成直肠-结肠端端吻合)、术中出血量(吸引容器内液体量减去冲洗液体量)、首次排气时间、术后住院时间(患者排气、排便正常,无发热、进食后腹部无不适反应,腹部彩超未见异常)。
1.4 统计学处理
2 结果
92例顺利完成腹部无辅助切口手术,无中转开腹。2组术中出血量、首次排气时间、术后住院时间差异无显著性(P>0.05),A组手术时间明显短于B组(P<0.05),见表2。A组术后无吻合口漏,B组4例,经保守治疗愈合。术后病理TNM分期和肿瘤分化程度差异无显著性(P>0.05),见表3。92例随访4~8个月,中位数5个月,A组复发3例,分别在术后第3、5、8个月复发,B组1例术后第6个月复发。
表2 2组患者术中、术后情况比较
*Fisher精确检验
3 讨论
腹腔镜结直肠手术由于腹部切口明显缩小,所以无论是病人的躯体痛苦和心理压力都有所减轻,但腹部有一个5 cm左右的辅助切口来取标本[2],对于一些年轻患者及对美容要求较高的老年患者,这种手术方式已经不能满足其心理需求。NOSES成为微创外科新的浪潮,它的快速发展为腹腔镜直肠外科开辟广阔的空间[3,4]。在追求手术微创和安全性的同时,简化手术步骤,缩短手术时间也已成为外科医师的重要研究范畴。
既往NOSES中,结直肠切除后我们将抵钉座通过TEM内镜送入腹腔,在送入近端肠管时最常用的方法是近端肠管腹腔镜下荷包缝合,然后抵钉座置入,镜下收紧荷包打结,但此种操作难度大、耗时长,抵钉座置入效果完全依赖术者的技术水平,吻合效果及漏的风险也大相径庭,不适合广泛普及。本研究结果显示荷包缝合法手术时间明显长于钉座绑线反穿法,说明腹腔镜下荷包缝合比反穿难度大,对术者技术要求很高,程序也相对复杂,不如反穿法简单快捷,手术时间长加大术中损伤和麻醉药物用量以及心肺负担。钉座绑线反穿法早已被用于胃肠吻合[5,6],安全性较传统荷包缝合法高,因为钉座绑线反穿法操作简单由于杆部是从针孔样小缺损里穿出来,拉出钉座杆部后周围严密包围钉座杆,不会发生吻合不完全情况,荷包缝合后镜下打结时,一旦遇到肠腔很宽大,肠壁肥厚的病例,可能荷包收不紧或打结后不能让肠壁牢牢和钉座杆紧密系在一起,可能存在缝隙,加上收紧吻合器的挤压,吻合后可能造成吻合不完全,部分黏膜或浆膜层缺如。
传统钉座绑线反穿法在操作中钉座两侧经常出现2个角,俗称“狗耳朵”[7],能否增加吻合口漏的几率现无权威解释。我们采用改良式抵钉座绑线反穿法与传统反穿法有所不同:切割器在切割近端肠管时,传统方法是切割器与系膜呈垂直状态,我们在原来状态下把肠管旋转90°,使切割器与系膜呈平行关系,切割完后确定抵钉座从系膜对侧肠壁穿出,这样抵钉座穿出后,钉座砧板上覆盖的肠壁近乎没有系膜,两侧也没有“狗耳朵”。另外,除消除“狗耳朵”外,由于钉座砧板覆盖的肠壁几乎没有系膜脂肪组织或脂肪组织很少,使吻合时砧板和吻合器之间没有夹杂太多脂肪组织,不必过度用力收紧吻合器压榨,所以就不会因为吻合器过度收紧而造成吻合口狭窄或上切缘环不完整等情况,这样吻合会更加确切,减少吻合口漏的几率。荷包缝合受限于个人技术差异、肠管粗细和肠壁肥厚等因素。至于缝合钉被切断是否影响漏问题,已经有大量事实证明没有问题,因为常规腹腔镜直肠癌手术远侧直肠残端闭合都是缝合钉,无论是荷包缝合还是钉座反穿法,只要用吻合器吻合都是远侧缝合钉被切断形成新的吻合口,吻合后远侧肠管也有2个切缘位于吻合口两侧,并没有因此而提高吻合口漏的概率。
另外,传统荷包缝合并不是所有消化道重建都适合,比如结肠次全切除时保留的升结肠残端大都较宽,残端荷包缝合后打结难以把太多肠壁收紧牢牢固定在钉座杆周围,同时,因较多组织在吻合器的钉座和吻合器头之间,收紧吻合器就可能把组织挤压出去造成吻合不全或吻合后缝合过多组织而张力加大导致钉松动或脱落。
临床上亦有将吻合器抵钉座经拟切断的肠管处切开的切口送入近侧肠管,然后用镜下切割器在切口上方切断肠管,让抵钉座留在近侧肠管内,再用器械辅助让抵钉座尾部从肠壁穿出来直到抵钉座杆完全显露,抵钉座的圆形头部分紧贴肠管内侧壁的报道。这种方法和我们目前采用的方法有相似之处,这样可以保证抵钉座根部被肠管包围严密,吻合起来效果较好。但这样的操作难度依然很大,因为抵钉座进入肠管腔内后,再把它尾部穿出肠壁的操作属于全盲操作,特别是在结肠次全切除时,钉座送进回盲部闭合结肠残端后很难明确钉座尾部的位置。此外,因回盲部比较宽大,钉座在里面可以自由活动,不容易在肠壁外用器械控制,所以抵钉座的尖端能否顺利穿出也是个难题,如果经验不足就会造成穿出时间太长或者穿出的位置不满意给吻合带来难度和术后漏的风险。其他一些方法我们也尝试过,也都不太适合推广普及。吻合器抵钉座绑线反穿法与上述几种方式比,由于钉座的尾部从结肠系膜对侧肠壁的小孔穿出,钉座杆周围大都是裸化的肠壁,基本上钉座杆完全从肠腔内拉出后就可以吻合,省去修剪多余脂肪组织及镜下缝荷包时间,简化了操作步骤[8]。另外,由于抵钉座自预留小孔穿出的位置及大小准确无误,吻合比较精确,手术安全性也相应提高。
本研究结果显示改良式吻合器抵钉座绑线反穿法与传统方法相比,明显缩短手术时间,具有简单快捷和适合推广的优势,应用前景广阔。

