磷改性对K-Mo催化剂催化合成气制甲硫醇的影响
郭红彦,王 琪,王 静,赵 星,柴翠元
(1.合肥工业大学化学工程学院,安徽 合肥 230009,2.淮南联合大学化学工程系,安徽 淮南 232038,3.淮南师范学院化学材料学院,安徽 淮南 232038 )
甲硫醇(CH3SH)在工业中常用于合成染料、农药、医药等,可采用CH3OH和H2S合成或者通过含硫合成气在钼基催化剂上一步法制得[1]。文献[2-3]研究了合成气一步法制CH3SH的机理,提出CO先与H2S反应生成中间体COS,然后COS再进一步加氢得到CH3SH。近年来,MoP良好的加氢脱硫( HDS) 和加氢脱氮(HDN)性能引起了研究者的关注[4]。文献[5]通过模型化合物对NiMoP/Al2O3催化剂研究发现,加入适量的磷能够削弱NiMo活性组分与Al2O3载体之间的相互作用,增加Ⅱ型Ni-Mo-S活性相的含量,提高活性组分的分散度。文献[6]研究了在NiMo/Al2O3催化剂中引入磷元素, 发现P的添加利于MoS2晶体的进一步堆积, 促进活性相Mo物种的分散,从而提升催化剂加氢性能。最近,文献[7-8]研究了磷的添加对Al2O3上硫化氢和二甲硫醚制备甲硫醇的催化性能,结果表明,少量的磷添加可增加催化剂的比表面积、孔隙体积以及路易斯酸酸性位,尤其是路易斯酸性位的增加促进CH3SCH3和H2S的解离吸附,从而提高反应的催化性能。
本文采用等体积浸渍法分别制备了不同磷负载量的K-Mo-P/SiO2催化剂,并在固定床反应装置上考察了磷的添加对高硫合成气制甲硫醇的促进作用。通过H2-TPR和LRS表征研究磷添加前后催化剂中的Mo物种与载体间的相互作用变化,并对反应后的催化剂进行LRS以及ESR研究,探讨磷的加入对K-Mo-P/SiO2硫化态催化剂性能的影响。
1 实验
(1)样品制备
催化剂采用等体积共浸渍法制备。 首先将计量的四水合钼酸铵和KOH以摩尔比1∶2混合溶于适量蒸馏水中配制成均一溶液,然后,按钼源(以MoO3计量)负载量为20%称取SiO2(60~80目)载体,进行等体积浸渍,室温静置24h后110℃烘干,得K2MoO4/SiO2催化剂。
配制计量浓度的NH4H2PO4溶液,与K2MoO4/SiO2催化剂再次进行等体积浸渍,室温静置24h后110℃烘干,制得催化剂样品。记作K2-Mo1-Px/SiO2催化剂,其中x为P/Mo的摩尔比。
(2)催化剂表征
氢气程序升温还原(H2-TPR)测试在自制TPR装置上进行。称取50mg试样(60~80目),在氮气氛中升温至300℃吹扫40min以上去除表面吸附,降温冷却至100℃,改通5% H2-95%Ar混合气(流速为25mL·min-1),以10℃·min-1的速率升温至850℃。
激光拉曼光谱(LRS)测试在原位激光共聚焦拉曼光谱分析仪上进行。激光源:Ar+激光器的532nm线,扫描范围:200~1 200cm-1。
ESR测试在日本日本电子JES-FA200电子自旋共振谱仪上进行。
(3)催化剂性能评价
催化剂的活性评价在固定床微型反应器上进行,每次催化剂的装填量为0.5mL,反应温度为300℃,反应压力为0.2MPa,空速为3 000h-1。催化剂试样在300℃恒温下先通入H2活化8h,再切换通入原料气,保持此温度下充分硫化2h,采样,由气相色谱仪在线分析。 原料气组成:V(H2S) /V(H2) /V(CO) =2∶1∶1。热导检测器(TCD)分析CO,CO2;氢火焰离子化检测器(FID)分析烃类和甲硫醇含量;氢火焰分光光度检测器(FPD)用于分析含硫化合物。
2 结果与讨论
(1)催化剂H2-TPR表征
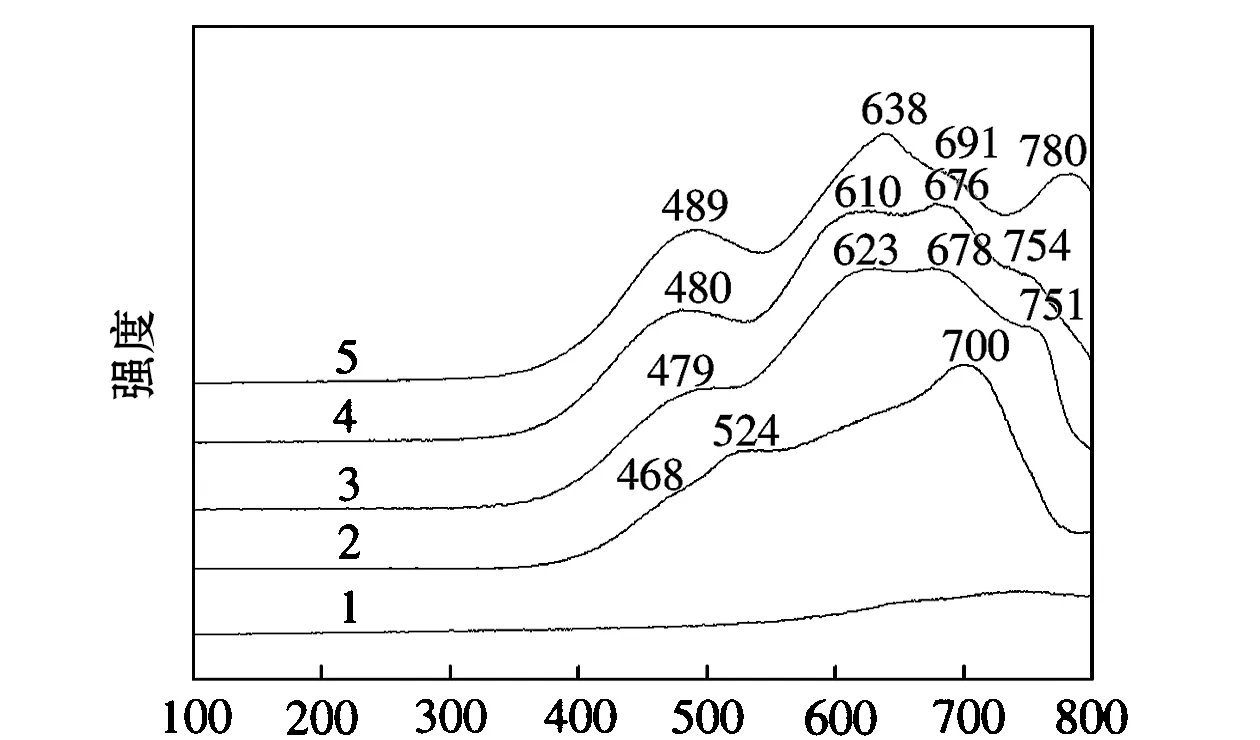
温度/℃1.P0.1/SiO2;2.K2MoO4/SiO2;3.K2-Mo1-P0.1/SiO2;4.K2-Mo1-P0.2/SiO2;5.K2-Mo1-P0.3/SiO2图1 催化剂的H2-TPR谱图
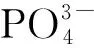
曲线3~5为不同P添加量的K2-Mo1-Px/SiO2催化剂的H2-TPR表征结果,数据表明,磷的添加对催化剂表面Mo物种的还原性能具有显著影响。对比曲线2,磷修饰改性的K2-Mo1-P0.1/SiO2(曲线3)、K2-Mo1-P0.2/SiO2(曲线4)和K2-Mo1-P0.3/SiO2(曲线5)催化剂的还原峰明显向低温方向移动,同时还原峰面积显著增加。结果表明,磷的添加可以减弱催化剂表面Mo物种与SiO2间的相互作用[14]。同时还可以看出,磷的添加量增大会导致催化剂的还原温度略有升高。而磷添加后出现在750~780℃附近的还原峰,可能与磷被还原密切相关。
(2)催化剂LRS表征
图2为不同磷的添加量的氧化态和硫化态催化剂的LRS谱图。从图2(a)中曲线1可以看出,K2MoO4/SiO2催化剂在217,362,900cm-1附近出现了三组特征峰。文献[15]等研究指出四面配位“Mo6+(Td)”的单钼化合物在317,843和896cm-1有明显的特征峰,而八面配位“Mo6+(Td)”的多钼化合物在219,360,474,896 和941 cm-1有LRS 特征峰。文献[16] 指认200~250cm-1为Mo-O-Mo的变形振动,310~370cm-1为Mo=O的弯曲振动,500~650cm-1为Mo-O-Mo的对称伸缩振动,700~850cm-1为Mo-O-Mo的反对称伸缩振动,和900~1 000cm-1端基Mo=O伸缩振动,同时,指认~900cm-1处出现为端基Mo=O伸缩振动峰,且与Mo的聚集程度成正比。
因此可知,K2MoO4/SiO2氧化态催化剂上217,362,894~939cm-1位置处主要是高聚集态八面体结构的Mo7O246-物种Mo-O-Mo的变形振动和反对称伸缩振动,以及Mo=O的弯曲振动和端基Mo=O伸缩振动。曲线2~4显示添加磷后217cm-1处特征峰消失,710cm-1处出现了新的特征峰,说明磷破坏了Mo-O-Mo的变形振动模式而转变为聚钼物种的桥式Mo-O-Mo的反对称伸缩振动峰[17]。随着磷的添加,高波数特征峰前移至843,857,906,927cm-1处,从而得出,添加磷会导致催化剂表面Mo的聚集程度降低[18]。结合H2-TPR的还原数据结果,磷添加可以提高催化剂的低温还原性能,提升活性组分的分散程度。同时还可以看出,K2MoO4-P0.3/SiO2(曲线4)催化剂同时存在低聚集态八面体结构的Mo7O246-物种和四面体结构的MoO42-物种,这可以归因于部分Mo与四面体的PO43-结合从而产生四配位的Mo-O-P结构。
图2(b)为硫化态催化剂ESR图谱,374cm-1和405cm-1处的振动散射峰被指认为硫化钼造成的[19],~900cm-1处的振动散射峰归属于硫钼氧物种。另外,在200~450cm-1处的散射峰分别被指对应Mo-O或Mo-S 变形振动和桥硫的振动。对比曲线1~4,MoS2的衍射峰随着磷含量的添加显著增强,由此表明了磷元素的引入有利于钼向MoS2物种转化,有趣的是,工作态催化剂出现了更多的S-Mo-O物种,该物种与甲硫醇的生成密切相关。
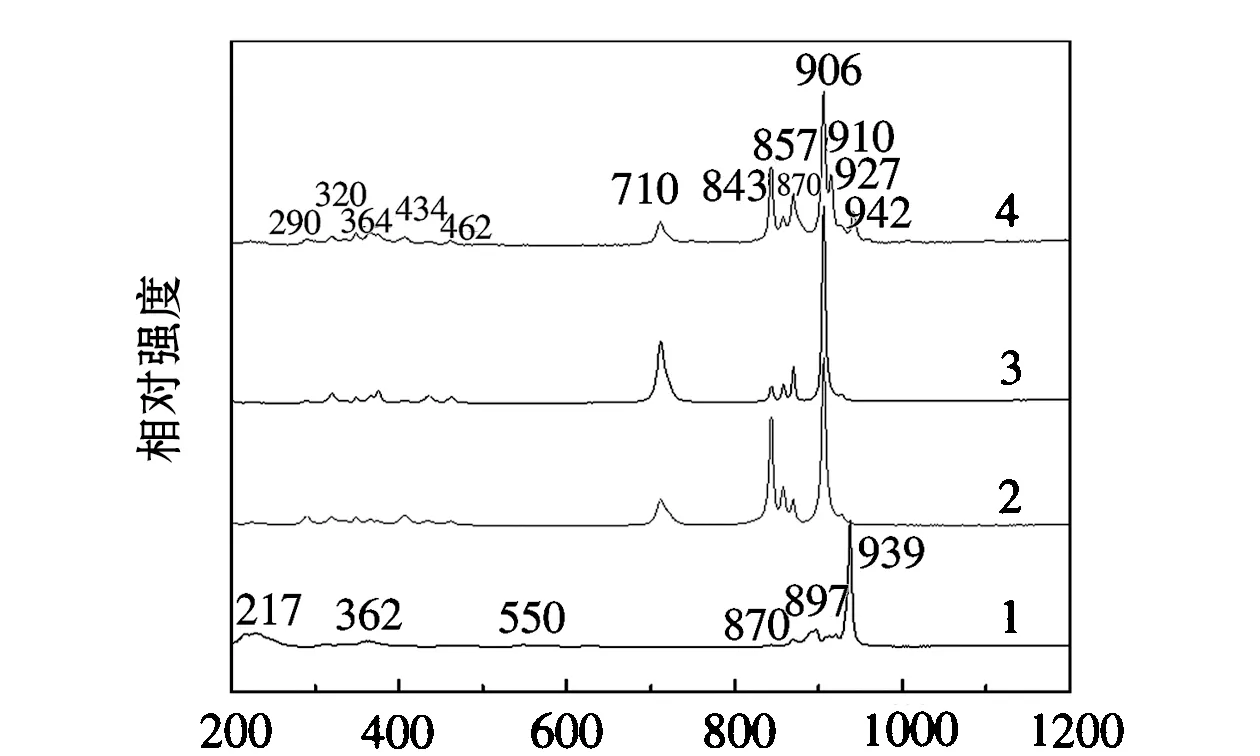
位移/cm-1(a)氧化态催化剂光谱
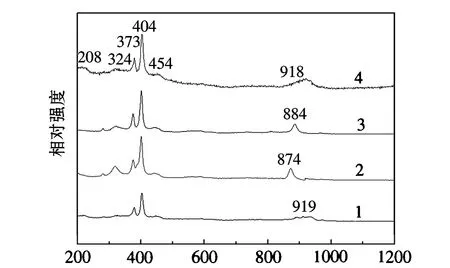
位移/cm-1(b)硫化态催化剂光谱1.K2MoO4/SiO2;2.K2-Mo1-P0.1/SiO2;3.K2-Mo1-P0.2/SiO2; 4.K2-Mo1-P0.3/SiO2图2 氧化态(a)和硫化态(b)催化剂的LRS光谱
(3)催化剂ESR表征
图3为硫化态催化剂ESR谱图。文献[3] 指出信号g=1.899处的峰值是由氧包围的Mo5+活性钼与载体的相互作用产生的。信号g=1.998处的峰值可归属于氧硫包围的Mo5+活性钼,这是因为催化剂经过硫化,部分O原子被S原子替代,形成“O-Mo-S”复合体,使得信号峰值移动。如图所示,引入磷后的催化剂,g=1.899处的信号峰值显著增强,说明磷的引入会降低活性组分与载体的相互作用,O原子增容易被S原子替代。这个结论与前面H2-TPR的表征结果一致。

能量/eV1.K2MoO4/SiO2;2.K2-Mo1-P0.1/SiO2;3.K2-Mo1-P0.2/SiO2;4.K2-Mo1-P0.3/SiO2图3 硫化态催化剂的ESR谱图
(4)催化剂活性评价
将催化剂用于高硫合成气制备甲硫醇反应,其活性数据结果如图4所示。磷引入后CO转化率及CH3SH和COS的选择性都得以大大提升,副产物CO2的选择性有明显降低趋势,同时随着磷元素含量的增加,CO转化率和CH3SH的选择性先增加后降低,K2-Mo1-P0.2/SiO2催化效果最好。

图4 K2MoO4/SiO2催化剂上高硫合成气制备甲硫醇的活性
文献[17]指出,在钼基催化剂上催化合成气制醇过程中,低价态配位未饱和的Mo与CO的吸附密切相关。由H2-TPR、ESR谱图数据并结合催化性能表征结果可知,往K-Mo催化剂中添加磷后,低价态钼物种的浓度显著增大,工作态的催化剂存在更多的低价态配位不饱和Mo位。但是随着磷添加量的增多,部分八面体配位“Mo6+(Oh)”物种向四面配位 “Mo6+(Td)”物种转化,活性位反而减少。因此导致CO的转化率随磷添加量的增多,呈现了先增大后减小的趋势。
3 结论
(1)非金属P元素对高硫合成气制甲硫醇的K2MoO4/SiO2催化剂具有促进作用,当P/Mo的摩尔比为0.2时,催化剂的活性最高;
(2)H2-TPR和氧化态催化剂LRS表征显示P元素的加入增加了八面不饱和配位的Mo物种的含量以及低分散度,增强了Mo的可还原性;硫化态催化剂LRS表征显示P的加入,提高了低价硫物种的浓度;
(3)ESR表征进一步证明了P元素的加入降低了载体与活性组分之间的作用力,促进钼氧物种上硫的取代,增加了“oxysulfo-Mo5+”物种的含量。
总之,P的促进作用被认为是促进了催化剂的活性组份的还原和硫化,对其促进效应的研究进一步证实了低价硫和低价钼的存在对高硫合成气制甲硫醇反应的重要性。

