氧弹燃烧-离子色谱法测定茶叶中的氟
(天津海关(原天津出入境检验检疫局)动植物与食品检测中心,天津300461)
氟是自然界中常见的元素,也是人体必须的微量元素,人体缺氟易出现佝偻、骨质疏松和龋齿等病症。但若摄入过多的氟,也会导致急性或慢性氟中毒,主要表现为牙斑釉和氟骨症[1]。研究表明,茶树是富集氟能力很强的植物,含量高达每千克几百至上千毫克[2-3]。农业部标准NY 659-2003《茶叶中铬、镉、汞、砷及氟化物限量》中规定,茶叶的氟化物限量值为200 mg/kg[4]。因此,建立茶叶中氟含量的检测方法具有重要的意义。
离子色谱因其较高的灵敏度,较好的选择性,快速简便等优点,是检测氟离子的理想方法。检测茶叶中的氟主要的前处理方法有灰化碱熔法、浸泡法和氧弹燃烧法等[5-10]。灰化碱熔法在开放的容器内进行,氟易挥发至空气中,造成回收率偏低;文献表明茶叶中42%~86%的氟可被溶解到茶水中[11],而采用浸泡法,植物细胞内的氟也难以被完全提取;氧弹燃烧法将样品放在富氧的密闭环境下进行燃烧,燃烧完全,样品内的氟元素全部被转化为无机态的氟离子,可满足茶叶中氟的检测要求。本试验利用氧弹燃烧的前处理技术,结合离子色谱分析方法测定茶叶中氟离子的含量,提高了方法的准确性和重现性。
1 材料与方法
1.1 材料与仪器
氟离子标准溶液:国家标准物质中心,1 000 mg/L;50%NaOH溶液:阿法埃莎(天津)化学有限公司;所有试验用水均为去离子水(经Millipore纯水系统纯化,电阻>18.2 MΩ);绿茶、黑茶、普洱茶、花茶:超市。
ICS-3000离子色谱仪(配电导检测器、紫外检测器、KOH淋洗液发生装置、ASRS 500(4 mm)阴离子抑制器)、ICS-3000色谱工作站数据处理系统、AS自动进样器:DIONEX公司,美国;IonPac AS11-HC型阴离子分离柱(4 mm×250 mm)、IonPac AG11-HC型保护柱(4 mm×50 mm):Thermofisher公司,美国;0.22 μm 水系微孔滤膜:博纳艾杰尔公司,天津;Parr-1911型氧弹燃烧仪(包括氧弹、坩埚、石英内衬、铂金点火丝、冷却水浴和气体吸收装置):Parr公司,美国;Mili-Q型纯水仪:Millipore公司,美国;2mL注射器:华福医械公司,浙江。
1.2 分析条件
淋洗液:浓度为10 mmol/L~60 mmol/L;洗脱梯度:10 mmol/L 保持 10 min,10 min~35 min升至 60 mmol/L,保持 10 min,45 min~50 min 10 mmol/L;抑制器:ASRS 500型抑制器(4 mm);抑制电流:149 mA;紫外检测波长:223 nm;进样量:100 μL;柱温:30 ℃;电导池温度:35℃。
1.3 试验方法
将茶叶样品,经食品粉碎机粉碎后,过40目筛,于80℃下烘干至恒重。称取0.500 0 g茶叶试样于压片机中压成茶饼,放入氧弹坩埚中,石英内衬中加入20 mL 10 mmol/L的NaOH溶液作为吸收液,向气体吸收瓶中加入20 mL10 mmol/L的NaOH溶液。小心拧紧氧弹盖,向氧弹中慢慢充入氧气至3.0 MPa,将氧弹置于水浴中,连接点火电极,点火,燃烧。静置吸收20 min。将氧弹从水中取出,缓慢开启放气阀,进入气体吸收装置经吸收液吸收。用纯水洗涤弹体、气体吸收管及石英内衬,与气体吸收液合并定容至100 mL。经0.22 μm滤膜过滤后上离子色谱仪分析。
2 结果与讨论
2.1 样品制备方法的研究
常规样品可直接放入氧弹的坩埚中,但由于茶叶样品质量较轻,称样量较大时易在坩埚内溢出。松散的样品在点燃的瞬间产生剧烈燃烧,部分茶叶会飞溅至弹体内,造成燃烧不完全。散落在吸收液中的茶叶还会引入有机杂质,影响检测结果。因此,需对茶叶试样进行粉碎处理。粉碎后的试样在压片机中压制成茶饼,再放入坩埚中燃烧,可使燃烧完全。
2.2 吸收时间对测定的影响
依照1.3的试验步骤,将同一样品进行多次氧弹燃烧,以20 mL 10 mmol/LNaOH作为吸收液,进行吸收时间条件试验,结果如图1所示。

图1 吸收时间对回收率的影响Fig.1 Effect of absorption time
从图1可知,随着吸收时间的延长,回收率逐渐增大,15 min后回收率基本不变。所以,本试验确定吸收时间为20 min。
2.3 淋洗条件的选择
以KOH为淋洗液,其浓度越高洗脱强度越大,保留时间相近的物质易出现共洗脱,影响分离度,当淋洗液浓度大于20 mmol/L时F-与其后面的干扰峰难以分离,而淋洗液浓度较低时被测物洗脱较慢,分析时间随之延长。因此最终选择10 mmol/L的KOH作为初始浓度,10 min后梯度升至60 mmol/L,加快其他离子的洗脱,缩短整个分析时间,并有利于杂质离子的排出。F-及其他离子的标准色谱图见图2。

图2 F-及其他离子的标准色谱图Fig.2 Chromatogram of F-and other anions
2.4 氧弹燃烧法与浸泡法的比较
将绿茶样品用20 mL10 mmol/LNaOH浸泡30 min,与氧弹燃烧后石英内衬中的吸收液直接进样后进行对比。直接浸泡的茶叶的提取液中存在大量的有机酸、色素及其他有机物质,特别是小分子有机酸与氟离子的出峰时间非常接近,而且含量较高,影响氟离子峰的峰型,干扰氟离子的测定,难以对氟离子进行准确的定量,见图3、图4。再通过紫外检测器的色谱图进行对比,可发现浸泡法的色谱图较为杂乱,而氧弹燃烧法的紫外色谱图则仅有亚硝酸盐和硝酸盐的色谱峰,说明样品燃烧完全,有机物都被转化为无机物,见图5、图6。
2.5 方法精密度
对绿茶、黑茶、普洱茶、花茶进行6次平行处理进样,结果见表1。绿茶样品色谱图见图7。
2.6 方法回收率
采用标准加入法对每份茶叶样品进行加标回收试验(各做6次平行),统计结果见表2。
2.7 方法的线性范围和检出限

图3 直接浸泡法后绿茶的电导色谱图Fig.3 Conductivity chromatogram of soaked green tea
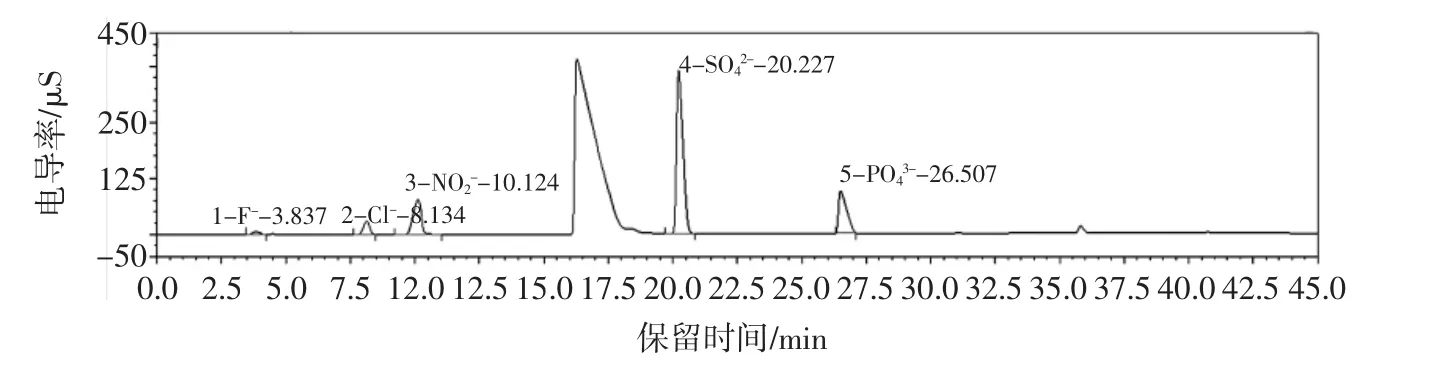
图4 经氧弹燃烧后绿茶的电导色谱图Fig.4 Conductivity chromatogram of green tea by oxygen bomb combustion

图5 直接浸泡法后绿茶的紫外色谱图Fig.5 UV chromatogram of soaked green tea

图6 经氧弹燃烧后绿茶的紫外色谱图Fig.6 UV chromatogram of green tea by oxygen bomb combustion

表1 样品精密度试验Table 1 Analytical precision of fluoride

图7 绿茶样品色谱图Fig.7 Chromatogram of green tea
氟离子标准品经纯水稀释,配制成标准系列,按色谱条件进行测定。结果表明,氟离子的质量浓度在0.05 mg/L~2 mg/L范围内与其峰面积呈线性关系,线性回归方程为y=1.736x+0.017 3,相关系数为0.999 9。氟离子校准曲线见图8。以峰面积为基线噪声的3倍浓度推算方法的检出限,氟离子的检出限为2.3 μg/L。

表2 回收率试验结果Table 2 Recovery of fluoride

图8 氟离子校准曲线Fig.8 Calibration curve of F-
3 结论
用充氧压力为3.0 MPa的氧弹燃烧分解茶叶样品,用10 mmol/LNaOH作为吸收液,吸收作用时间为20 min,离子色谱法测定氟含量;平均回收率为90.8%~93.7%,相对标准偏差为1.2%~3.1%。结果表明,氧弹燃烧-离子色谱法将茶叶中的氟转化为无机氟离子,燃烧去除了试样中的有机干扰物,其精密度和准确度符合茶叶中氟的测定要求,可应用于茶叶中氟的测定。

