慢性主观性耳鸣认知障碍特征分析
张剑平, 曹婷婷, 任冰焱, 王 涛, 余 欣, 王 艺, 李在望
主观性耳鸣是指在无外部刺激的情况下,患者自觉耳内或颅内有异常声音的一种常见的临床疾患[1,2]。同时,主观性耳鸣患者还常伴有失眠、焦虑等非听觉症状[3,4]。不仅如此,临床医生早已发现慢性主观性耳鸣不仅是一种异常的听觉感知,还常常伴有一定程度的认知缺陷[5]。然而,关于慢性主观性耳鸣认知功能的相关研究极少,因此慢性耳鸣患者的认知障碍的临床特点尚不清楚。同时,慢性主观性耳鸣患者的认知缺陷是耳鸣继发的临床表现还是该病固有的主要特征也未明了。为此,我们应用认知能力筛查测验(中文2.0版)(Cognitive Abilities Screening Instrument,Chinese Version 2.0,CASI C-2.0)[6,7]和听觉诱发电位P300来研究慢性主观性耳鸣患者与健康对照人群认知能力的差异,从而探讨慢性主观性耳鸣患者认知障碍的临床特征。
1 资料与方法
1.1 临床资料 选择2015年4月-2016年3月就诊于无锡市人民医院神经内科和耳鼻喉科的慢性主观性耳鸣患者和同期健康体检者。慢性主观性耳鸣的诊断均符合Shulman A和Farhadi M确立的诊断标准[8,9]。
1.2 纳入及排除标准 慢性主观性耳鸣组的纳入标准:(1)确诊为慢性主观性耳鸣的18~80岁患者;(2)单侧或双侧耳鸣病程至少6个月。排除标准:(1)因外耳和中耳解剖结构异常导致的客观性耳鸣;(2)患有其他的可能影响听力的相关疾病;(3)合并痴呆。其中,痴呆的诊疗步骤为:首先详细询问病史,然后通过CASI量表进行认知评估(CASI量表的痴呆诊断评分标准为:教育年限为0 y的患者<50分;教育年限为1~5 y的患者<68分;教育年限为>6 y的患者<80分)[6],最后按照精神障碍诊断与统计手册第4 版修订版(DSM-IV-R)[10]标准来明确痴呆的诊断。对照组纳入标准为18~80岁健康者。
1.3 研究方法 采用耳鸣残疾评估量表(THI)[11]评估耳鸣严重程度,CASI C-2.0量表评估认知功能。其中,CASI量表是美国南加州大学李眉等编制的一套筛查痴呆的神经心理测试量表,有英文、中文及日文3个版本[6]。而CASI C-2.0量表为中文第二修订版,由9个子项目组成:长期记忆(LTM)、短期记忆(STM)、注意能力(Att)、数字计算(Conc)、定向能力(Ori)、抽象思维及判断(AJ)、语言能力(Lang)、构图能力(VC)和思维流畅度(Flu)。CASI C-2.0分值在0~100之间,分数越高代表认知能力越好。目前,CASI量表在痴呆及认知功能障碍等临床领域的应用得到广泛的认可,其不仅适用人群广,而且在效度方面也有优势[7]。CASI量表敏感性与简易精神状态检查表(MMSE)相当,特异性高于MMSE[7,12]。同时,本研究采用听觉诱发电位P300客观评估耳鸣患者认知功能[13]。我们按照国际电极系统10/20标准,将电极置于Fz、Cz和Pz等电极点记录大脑活动,将A1和A2参考电极分别置于受试者左右耳垂,采用经典的OB刺激序列模式诱发听觉电位。OB刺激序列模式包括靶刺激和非靶刺激。本研究采用的靶刺激频率、概率、强度分别为2000Hz、20%、85 dB HL;非靶刺激频率、概率、强度分别为1000 Hz、80%、60 dB HL,两者间隔1~3 s。测试结束,相关技术人员分析听觉诱发电位P300成分特征(P300 潜伏期和波幅)。另外,所有参与者均应用听力计(AC40,Interacoustics,丹麦)检测听阈。听力检查频率为150~8000 Hz,正常听力范围为0~25分贝。
1.4 统计学分析 使用SSPS 16.0统计软件进行数据分析。统计方法为t检验、卡方(χ2)检验、Mann-Whitney U检验、相关分析等。P<0.05视为有统计学意义,P<0.01视为有显著统计学意义。
2 结 果
2.1 一般资料 本研究成功招募到201例耳鸣患者,其中82例患有可能影响听力相关疾病的患者和16例合并痴呆的患者被剔除。最后,103例慢性主观性耳鸣患者和52例健康对照者纳入该研究。
2.2 两组研究对象的基线资料比较 耳鸣组在年龄、性别构成、教育程度等方面与对照组相比无显著差异,但两组研究对象听力具有显著差异(P<0.01)。Pearson相关分析显示:双耳纯音听阈值与CASI评分呈负相关(r=-0.168,r=-0.122,均P<0.05),与P300潜伏期呈正相关(r= 0.122,r=0.255,均P<0.05),表明听力减退与认知之间有很强的相关性(见表1)。
2.3 两组CASI量表各子项目评分及总分的比较 由于听力减退与认知能力之间有很强的相关性,故在该研究中以双耳纯音听阈值为协变量,应用协方差分析法对两组CASI各子项目评分进行分析,从而评估两组间认知能力的差异。耳鸣患者组与对照组相比,在“短期记忆(STM)”,“注意能力(Att)”和 “定向能力(Ori)”等方面具有差异,但两组间CASI总评分无显著差异(见表2)。
2.4 两组P300潜伏期与振幅的比较 耳鸣组较对照组潜伏期延长(P<0.001),但振幅无显著性差异(P>0.05)(见表3)。
2.5 两组CASI总分及各子项目评分与THI评分及P300 潜伏期之间的相关性分析 CASI总分与THI评分和P300潜伏期呈负相关。耳鸣患者组CASI各子项目评分和THI评分之间均呈负相关,CASI各子项目评分与P300潜伏期呈负相关(除“长期记忆”)。THI评分与P300潜伏期呈正相关(r=0.345,P<0.001)(见表4)。
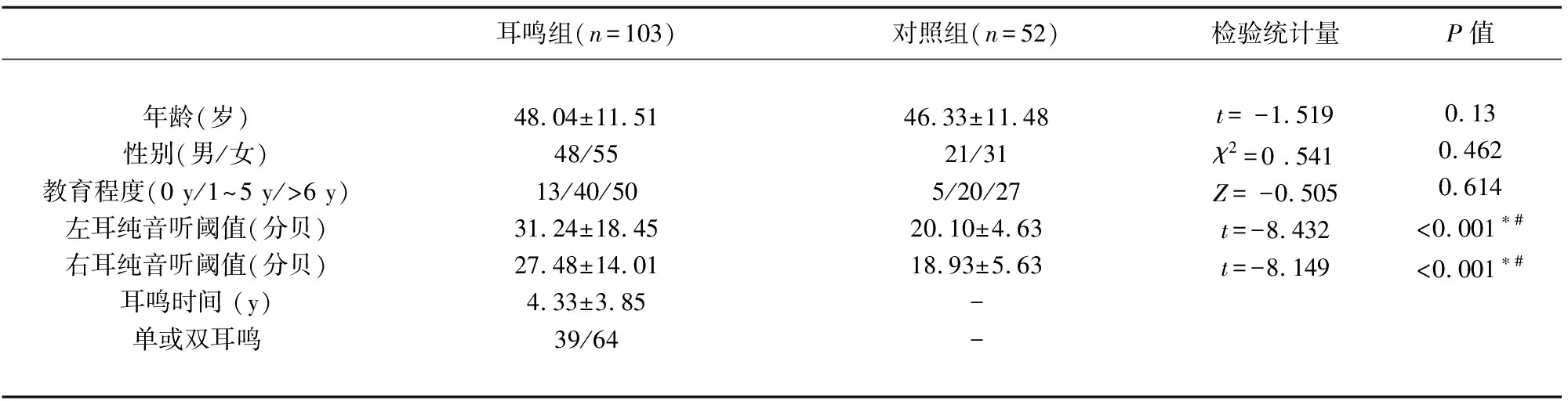
表1 耳鸣组及对照组一般资料比较
注:*#P<0.01,*P<0.05

表2 耳鸣组与对照组CASI各项目得分及总分比较
注:*#P<0. 01,*P<0.05

表3 耳鸣组与对照组P300听觉诱发电位参数比较
注:*#P<0.01,*P<0.05

表4 CASI总分、各子项目评分与THI评分、P300潜伏期的相关性分析
注:*#P<0.01,*P<0.05
3 讨 论
在本研究中,我们采用认知能力筛查测验量表(CASI)和听觉诱发电位P300结合的研究方法来比较慢性主观性耳鸣患者与健康人群认知能力的差异。结果显示,耳鸣组在“短期记忆”、“注意能力”和“定向能力”等方面的得分明显低于对照组。而对于CASI量表而言,“短期记忆”和“定向能力”这两个子项目评分之和在对认知能力评估的效度方面甚至超过CASI量表总评分的效度[14]。这一结果表明慢性主观性耳鸣患者存在认知功能损害。进一步的相关性分析证实CASI总分及各子项目评分均与耳鸣严重程度(THI评分)呈负相关,表明认知障碍的严重程度可能与耳鸣严重程度密切相关。我们不仅使用CASI量表而且还采用了听觉诱发电位P300这一客观指标来分析慢性主观性耳鸣患者的认知功能。P300潜伏期与刺激评价过程(如编码、分类)密切有关,可客观评估认知能力[13]。本研究结果显示两组P300潜伏期存在显著差异,而P300振幅无显著差异。同时相关性分析结果还提示P300潜伏期与THI评分(耳鸣严重程度)呈正相关而与CASI评分(认知能力)负相关。这些结果证明认知障碍是慢性主观性耳鸣的一个非听觉方面的重要临床特征。
本研究中耳鸣组中不仅无痴呆患者而且其CASI总评分与对照组也无显著差异。然而慢性主观性耳鸣患者的部分认知功能(“短期记忆”、“注意能力”和 “定向能力”)却出现明显下降。不仅如此,其P300潜伏期较正常对照组也显著延长。这提示慢性主观性耳鸣患者不仅长期遭受耳内异响的困扰,而且还存在显著认知功能障碍。这是为什么呢?最近的关于慢性耳鸣患者脑结构异常改变的研究为解释这种临床现象提供了有力的依据。Leaver等人[15]发现慢性耳鸣患者前额叶腹内侧皮质结构明显减小于正常对照组人群。而前额叶腹内侧皮质在记忆力及注意力等方面发挥着重要的作用[16]。而Lee等人[17]采用扩散张量成像技术,证明慢性耳鸣患者脑内连接听觉和前额区的弓状纤维束受损。而此脑区的弓状纤维束通路与阅读、视觉空间功能密切有关[18]。简言之,慢性主观性耳鸣患者相关脑区结构的异常改变与认知功能障碍密切有关,这也证明“短期记忆”、“注意能力”和 “定向能力”等认知功能减退可能是慢性主观性耳鸣的一种固有的非听觉临床特征。
本研究具有一定的局限性。首先,耳鸣患者和健康对照者处于不同的健康状态,有些耳鸣患者可能会有一定程度的听力减退和抑郁。虽然本研究已将双耳纯音听阈值作为协变量来消除两组听力差异对认知评估的影响,但两组患者的不同健康状况仍可能会导致认知功能评估的偏差。此外,受试者均来自无锡市人民医院,而医院内人群的特征可能与总体人群存在差异,这也可能导致研究偏倚。
总之,慢性主观性耳鸣不仅是一种异常的听觉感知,还常常伴有认知功能障碍等非听觉症状,尤其在“短期记忆”、“注意能力”和 “定向能力”等认知水平方面下降得极为明显。这些认知功能障碍特征的发现有利于提高临床医师对耳鸣患者非听觉症状的认识。

