永久性心脏起搏器植入术后囊袋大量积液一例
林宪如 延荣强 王正忠 于忠祥 唐军卫
文献报道,起搏囊袋的远期并发症以感染居多[1],而表现为单纯非感染性积液者则极为罕见。笔者发现1例永久性双腔起搏器植入患者于术后1年余出现大量囊袋积液,现报道如下。
患者女性,78岁,8年前因患右侧乳腺癌行手术治疗,术后给予短暂化疗并定期随访,病情稳定。1年半前因“病窦综合征”行永久性双腔起搏治疗,起搏器埋置于左侧胸大肌浅筋膜下。6个月前患者起搏囊袋处略有胀感并出现微微隆起,无疼痛感,遂未在意。其后起搏囊袋逐渐胀大并明显隆起,经予中药“芒硝”外敷5天后肿胀不消失,遂于5个月前来诊。患者无发热、寒战、乏力等全身不适症状。体检可见起搏囊袋明显隆起,触之有波动感,囊袋处无红、肿及触痛(图1),右侧乳腺切除后可见胸壁局部疤痕组织。心电图示起搏器起搏、感知功能正常。实验室检查:血常规示轻度贫血(血红蛋白9.6 g/L),白细胞计数及分类正常,C-反应蛋白及血沉正常;B超检查于起搏囊袋处可探及约8.1×5.0×7.5 mm无回声区,内见起搏器及导线回声(图2);胸部CT可见起搏器植入部位明显隆起及高密度影(图3,白色箭头所指处)。初步诊断为囊袋血肿,继予芒硝外敷1周后不见好转,遂行穿刺抽液,抽出黄色乳状液体,其中一管穿刺液外观粉色系刺破囊袋壁小血管所致(图4),抽出液无异味,总计140 ml;穿刺液送检,常规及生化检测结果示:外观淡黄色,混浊,镜检:WBC(++++)/HP,RBC 3~8/HP,结晶(-)/HP,真菌孢子(-)/HP,上皮细胞(-)/HP;总蛋白57.50 g/L,葡萄糖3.90 mmol/L,氯102.0 mmol/L,乳酸脱氢酶4202.03 u/L,腺苷脱氢酶149.02 u/L。穿刺液涂片可见大量中性粒细胞,未见脓细胞及恶性瘤细胞;穿刺液未发现抗酸杆菌,革兰染色未找到细菌,培养无细菌生长。其后分别于第7天及第35天2次重复穿刺,分别抽出液体50 ml和40 ml,外观及送检结果与第一次抽出液体大致相似,穿刺液培养均为阴性。抽液后于囊袋上方放置厚层无菌纱布并采用自制类似“乳罩状”加压装置行持续加压包扎,定期随访5个月,未再出现囊袋隆起,患者囊袋处亦无任何不适。
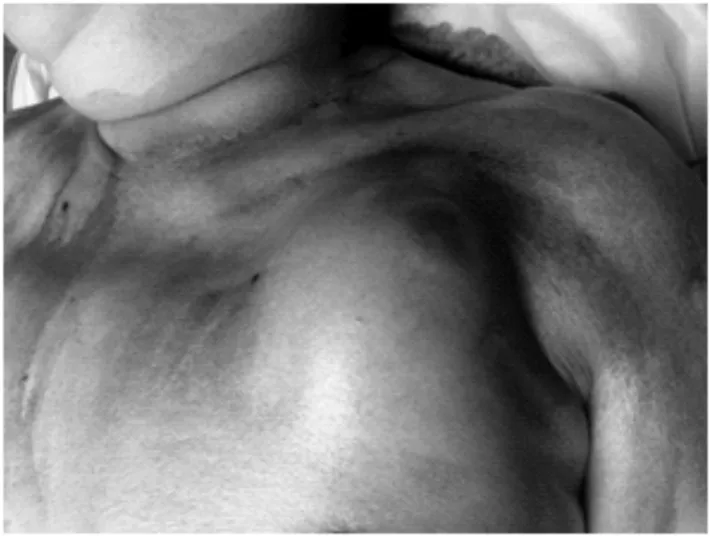
图1 起搏囊袋处明显肿胀、隆起
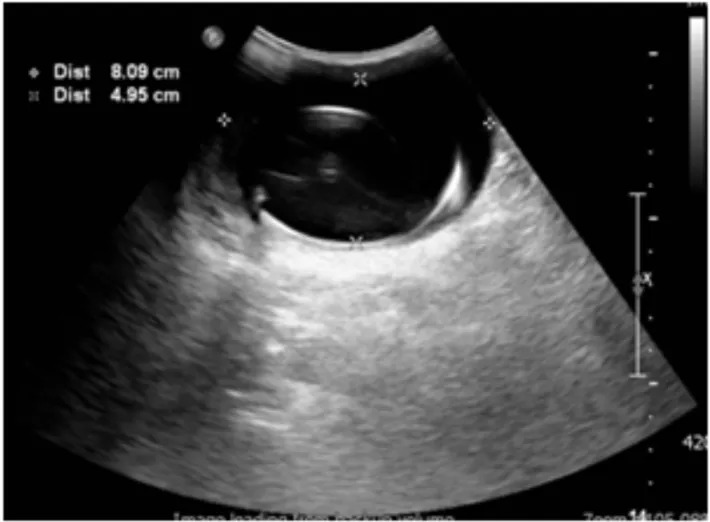
图2 起搏囊袋B型超声所见
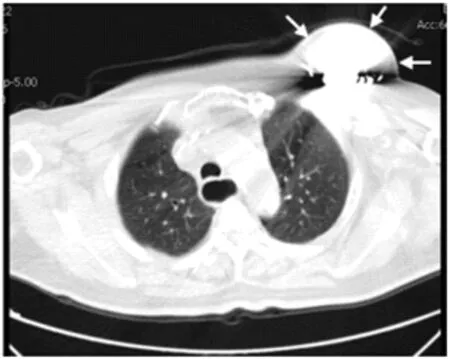
图3 胸部CT可见起搏囊袋明显凸起(白色箭头所指处)
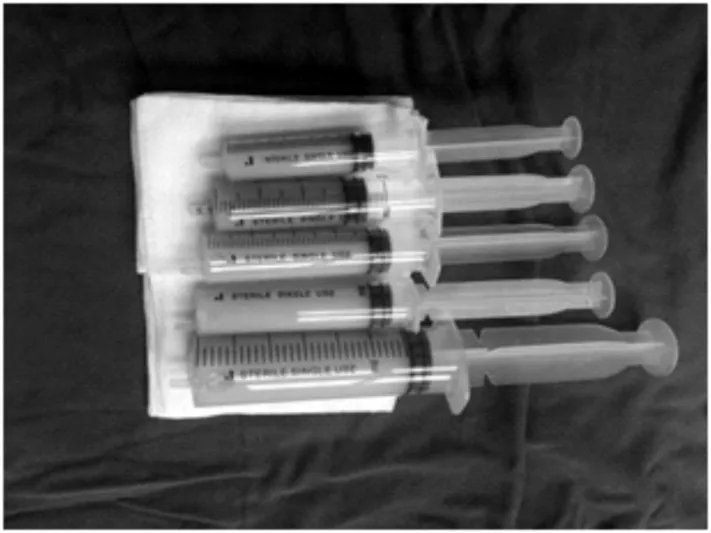
图4 起搏囊袋穿刺所抽出的黄色乳样液体,酷似乳糜液
讨论起搏器囊袋最常见的并发症为感染和血肿形成,前者可见于起搏治疗后的各个时期,而后者则以起搏术后围术期更为多见。起搏囊袋感染时,除囊袋部位出现肿胀外,局部皮肤可见典型的红、肿、热、痛等炎症特征,另外可有发热、白细胞增高等全身表现,显然,该病人的囊袋肿胀不符合上述特点,难以用囊袋感染来解释。图1中囊袋上方虽可见红色斑状皮疹,但亦并非感染征象,而是与此前芒硝外敷有关,停止芒硝外敷后红色皮疹很快消失。患者抽出液体为黄色液体,故也可排除囊袋血肿。患者在起搏治疗1年后何以出现如此之多的囊袋积液,其原因尚不明确,笔者认为可能系患者局部组织与起搏器表面相容性较差,逐渐导致起搏器周围组织受到刺激而液体渗出增加,而起搏器囊袋所形成的纤维膜则限制了液体的重吸收,久之在囊袋内形成大量积液,患者囊袋积液中含有大量白细胞,亦符合渗出液特点。部分患者起搏囊袋内出现反应性变化,亦可能与电极或起搏器放置的位置或形态以及囊袋的大小有关。此外,该患者因以往右侧乳腺癌根治术导致右胸淋巴引流系统完全破坏,其淋巴液回流主要经左侧淋巴引流系统,起搏器埋置于左侧胸大肌浅筋膜下,所穿刺抽出液体呈黄色乳样,酷似乳糜液,是否系术中导致胸导管损伤、以致组织间液引流障碍也未可知。起搏囊袋穿刺会增加日后感染的风险,宜谨慎使用。考虑到患者大量囊袋积液越来越多,且此前经芒硝外敷无明显吸收,给予穿刺抽液可减轻囊袋内压、促进液体吸收,同时亦可根据穿刺液进行特殊检查以尽早明确诊断、利于后续处理。笔者三次囊袋穿刺均在经严格消毒后的导管室内进行,也是为了尽可能避免穿刺所致继发性囊袋感染。在给患者抽取囊袋积液后局部采用持续加压包扎,随访5个月未见起搏囊袋再出现肿胀隆起。然而,本患者囊袋内发生积液或组织增生性改变的因素并未完全消除,仍应密切观察并延长随访时间,尤其要排除慢性囊袋感染的可能。

