瑞莱TZ-301型仪器对降钙素原检测能力的临床评价*
解宏杰,程歆琦,杨启文△,徐英春
(1.中国医学科学院北京协和医院检验科,北京 100730;2.北京市羊坊店医院检验科 100038)
脓毒血症是急性细菌感染最严重的表现形式,可引起多器官功能衰竭,病死率达30%~50%[1]。目前,诊断细菌感染的金标准是细菌培养,但是由于常规培养时间较长,往往不能及时给予临床指导而导致病情延误。降钙素原(PCT)是由甲状腺细胞分泌的,当脓毒血症发生时其在血浆中水平升高[2],目前已广泛应用于临床。瑞莱TZ-301型仪器(简称TZ-301)是由瑞莱公司(ReLIA)研发生产,基于免疫荧光的方法定量检测PCT水平的新型仪器,8 min即可完成1份标本的检测,在检测时间上有明显优势。为了验证其结果是否准确,本文以临床常用的基于酶联荧光免疫方法的VIDAS30型仪器(简称VIDAS30)作为比较方法,对瑞莱TZ-301的检测能力进行评估,现报道如下。
1 资料与方法
1.1一般资料 收集自2016年5-11月北京协和医院门诊及住院患者静脉血清标本共305例,其中4例处于不同医学决定水平的标本用于精密度验证;40例覆盖检测范围的标本用于正确度验证;结合VIDAS30的检测结果及临床意义将剩余261例标本根据PCT水平划分为5个区间,其中PCT<0.05 ng/mL 57例,0.05~0.50 ng/mL 86例,0.50~2.00 ng/mL 55例,2.00~10.00 ng/mL 44例,>10.00 ng/mL 19例,用于相关性、医学决定处偏倚、检测能力及区间一致性分析。
1.2仪器与设备 采用瑞莱生物工程(深圳)有限公司生产的瑞莱TZ-301及其配套PCT检测试剂,孵育器;法国梅里埃公司生产的VIDAS30及其配套PCT检测试剂。
1.3方法
1.3.1检测原理 将待测标本加入到检测试剂盒的加样口中,随着液体的流动,待检测标本先经过标本过滤垫片,然后再与荧光偶合物垫片上的PCT标记抗体发生特异免疫结合,形成荧光复合物。荧光复合物先经过测试带,复合物中的抗原与测试带中预包被的PCT抗体发生特异免疫结合,从而被固定在测试带中。免疫夹心复合物中的抗原水平与测试带的荧光强度呈正比,游离的复合物经过内控带时,复合物中的亲和素与内控带中已包被的羊抗亲和素抗体发生特异免疫结合,从而被固定在对照带中,其中内控带与测试带的荧光强度呈反比,从而可以校正标本个体差异。采用ReLIA荧光仪检测出2条带的荧光强度,并计算RI值(RI=测试带荧光强度/内控带荧光强度),拟合至校正曲线,仪器自动换算出相应标本中的PCT水平(ng/mL)。

1.4方法学比较
1.4.1正确度评价 采用VIDAS30和TZ-301同时检测40例水平覆盖检测范围的临床患者标本,5 d内完成检测。按照VIDAS30检测结果将所有结果分为≤10 ng/mL及>10 ng/mL 2个区间,分别计算TZ-301测定值均值与VIDAS30测定值均值间的偏倚,并计算置信区间,判断两种方法的偏倚是否小于厂家声明的偏倚。
1.4.2相关性分析及医学决定水平处的偏倚 由于VIDAS30对于<0.05 ng/mL及>200.00 ng/mL的PCT结果无法报告具体数值,因此,在做相关性分析时排除了<0.05 ng/mL的57例数据及200 ng/mL左右的2例数据,剩余202例标本参与相关性分析。采用Excel及Med Calc软件对总体数据的相关性及两种方法检测结果的偏差进行分析,拟合线性回归方程,计算相关系数及P值、斜率、截距及95%置信区间(95%CI),同时绘制两种方法的相关图及Bland-Altman图。再根据线性回归方程计算医学决定水平处的预期偏倚及95%CI。
1.5检测能力分析 将收集的所有标本作为标本总体,根据不同医学决定水平将检测结果分为几个不同区间,若瑞莱TZ-301检测结果与VIDAS检测结果位于相同区间即为符合。以VIDAS30作为比较方法,瑞莱TZ-301作为试验方法,以PCT水平0.05 ng/mL作为临界点,绘制受试者工作特征曲线(ROC曲线),计算曲线下面积,判断实验方法对感染的诊断效能。此外再分别对每个区间内的数据绘制四格表(真阳性、真阴性、假阳性、假阴性),计算每个区间内瑞莱TZ-301检测结果的敏感度(也称真阳性率)=真阳性例数/(真阳性例数+假阴性例数)×100%,指正确判断患者的程度,即实际有病而被正确诊断的百分比;特异度(也称真阴性率)=真阴性例数/(真阴性例数+假阳性例数)×100%,指正确判断非患者的程度,即实际无病而被正确诊断为无病的百分比。
1.6区间一致性分析 将收集的所有标本作为标本总体,若两种方法检测结果在相同区间即为符合。以VIDAS30检测结果作为参考方法,统计各区间瑞莱TZ-301检测结果不一致的标本例数及差异区间数,并统计不一致数据的偏倚属性。

2 结 果
2.1精密度验证 瑞莱TZ-301 PCT检测系统的CV均小于厂家说明书标示的相应接近水平的CV,其中厂家声明的CV<10.0%,结果能符合要求,见表1。

表1 瑞莱TZ-301 PCT检测系统的精密度
2.2方法学比较
2.2.1正确度评价 瑞莱TZ-301检测与VIDAS30检测PCT结果在0.00~10.00 ng/mL区间的偏倚为-0.11,95%CI为-0.75~0.27,厂家声明的偏倚为-0.20,在>10.00 ng/mL的区间偏移为-3.20,95%CI为-8.99~2.59,厂家声明的偏倚为-5.00,置信PCT覆盖厂家声明,见表2。
2.2.2相关性分析及医学决定水平处的预期偏倚 两种方法检测总体及各区间内数据在P<0.01水平上明显相关。此外,根据Bland-Altman图两种检测方法总体差异超过差异均值95%CI的数据为11个。拟合的线性回归方程及各参数见表3及图1,医学决定水平处的预期偏倚为-1.38~0.05,见表4。

表2 配对t检验结果
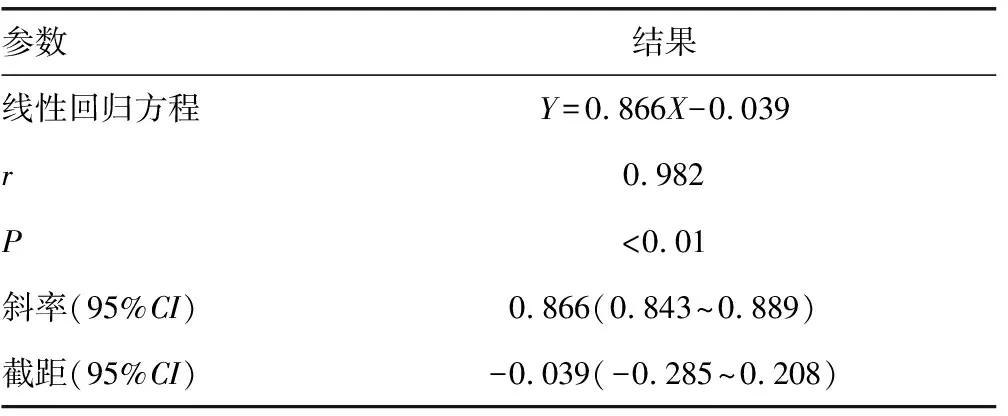
表3 总体数据的相关性分析
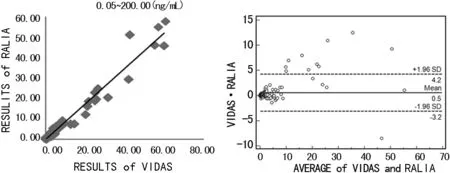
图1 总体标本检测结果的相关图及Bland-Altman图

表4 医学决定水平处的偏倚
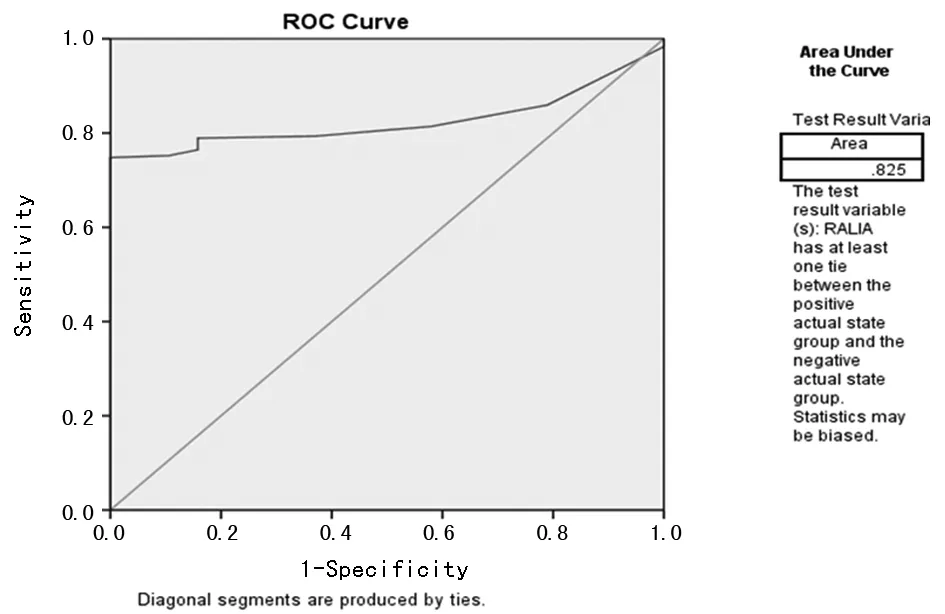
图2 瑞莱TZ-301对感染的诊断效能图
2.2.3检测能力分析 以VIDAS 30检测结果作为标准,ROC曲线下面积为0.825,具有一定的准确性,见图2。在PCT<0.05、0.05~0.50、0.50~2.00、2.00~10.00 ng/mL及>10.00 ng/mL的区间内敏感度、特异度分别见表5。

表5 瑞莱TZ-301对PCT的检测能力分析
2.2.4区间一致性分析 在0.05~0.50 ng/mL及0.50~2.00 ng/mL范围内二者比较区间不一致的例数最多,均为15例,>10.00 ng/mL范围内最为稳定,不一致标本个数为3例,见表6。各个区间不一致标本的结果均相差1个区间。比较各区间内不一致结果的偏倚属性,在<0.05 ng/mL的低值区间内,均为正偏倚,其余4个区间正偏倚逐渐减少,且为负偏倚居多。
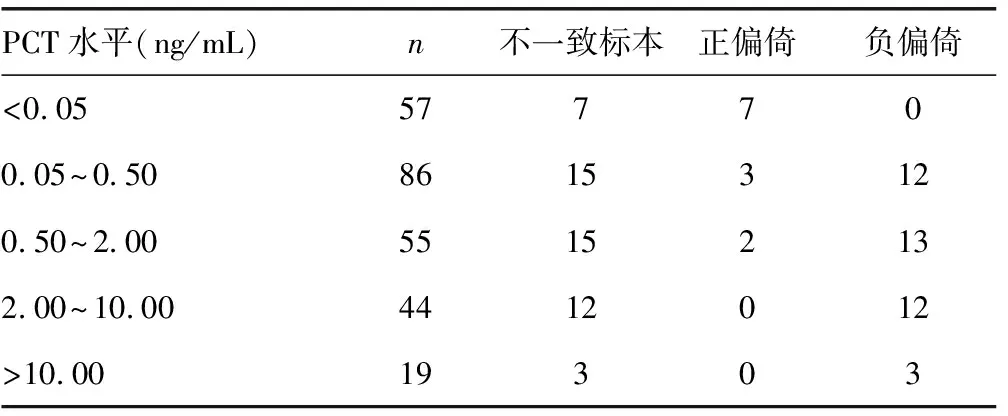
表6 瑞莱TZ-301检测PCT与VIDAS 30的不一致情况分析(n)
3 讨 论
脓毒血症表现为全身性炎性反应,是一类病程进展快,且可危及患者生命的细菌感染性疾病。有研究显示,脓毒血症细菌感染患者病情严重程度与血液炎性指标水平呈正相关,可作为临床上评估患者病情、预后的可靠指标[3]。血液炎症因子包括PCT、C反应蛋白(CRP)、白细胞介素-6(IL-6)、血清淀粉样蛋白A等,其中PCT对脓毒血症患者的诊断效能优于其他免疫炎症因子[4]。PCT是检测细菌感染的敏感指标,与脓毒血症病情严重程度及病原菌感染类型有一定关系,可用于脓毒血症的早期诊断[5]。此外,PCT检测方法简便快速,目前已广泛应用于临床。PCT检测结果在不同区间范围具有不同的临床意义。除新生儿等特殊人群外,PCT检测结果在<0.05 ng/mL时为正常值;在0.05~0.50 ng/mL时为可疑局部炎性反应或局部感染,建议查找感染或其他导致PCT增高的原因;在0.50~2.00 ng/mL为中度全身炎性反应,建议6~24 h后复查;在2.00~10.00 ng/mL时很可能为脓毒血症、严重脓毒血症或脓毒性休克,建议每日复查;>10.00 ng/mL时几乎均为严重脓毒血症或脓毒性休克,建议每日检测PCT以评价治疗效果[6]。本文正是以这些具有临床意义的检测区间为依据,将整体标本划分为5个不同的检测区间后选择标本,再对总体标本及各个区间内的结果进行分析,同时对于落在临界值的数据均统一向数值较高的区间划分。由于目前行业内对PCT检测结果的评价并无明确标准,从溯源来看,瑞莱TZ-301溯源到罗氏的仪器,罗氏仪器溯源到BRAHMS,目前PCT普遍认可的标准正是BRAHMS115抗原决定簇。梅里埃公司生产的VIDAS30是公认的检测PCT较为准确的仪器,其溯源也是BRAHMS,如此看来,瑞莱TZ-301与VIDAS30有共同的溯源,只是瑞莱TZ-301的溯源较VIDAS30低一级。因此,本研究选择梅里埃公司生产的VIDAS30作为比对的比较方法,瑞莱TZ-301作为试验方法,将标本按区间分类后再分析。通过比较,达到掌握瑞莱TZ-301检测PCT整体水平的目的,并了解其对不同区间结果的检测能力。
在本试验中首先对仪器进行了精密度验证,在保证仪器基本性能稳定后再进行其他性能验证。在进行正确度验证时,依据CLSI EP9A2指导方案,按照不同水平梯度分布选择了40例标本参与试验,结果能够更加全面地体现仪器的整体偏倚。
对于相关性分析,在部分低值区间内,因为检测数值较小,从而导致此类区间的相关系数偏低。此外,VIDAS30的检测范围为0.05~200.00 ng/mL,瑞莱检测范围为0.02~150.00 ng/mL。因此,对于相关性分析,本研究排除了检测限以外的数据,仅比较了均在两种方法检测范围内数据的相关性。经比较,对于总体及各区间内的数据,两种方法的检测结果r2>0.95,可认为二者明显相关,且根据线性回归方程计算了医学决定水平处的预期偏倚,更进一步评价了瑞莱TZ-301在医学决定水平处检测结果的正确性。
对于检测能力分析,因为根据PCT的临床意义,当PCT>0.05 ng/mL时即可疑局部炎性反应或局部感染,因此,在分析检测能力时,选择0.05 ng/mL作为诊断的临界点绘制ROC曲线,结果显示,瑞莱TZ-301对诊断炎性反应及感染具有一定的准确性。而在区间分析时,相对于其他区间,瑞莱TZ-301在PCT<0.05 ng/mL及>10.00 ng/mL区间内的敏感度及特异度均较高。在各个区间内,特异度较高而灵敏度相对较低,可能与两种仪器的检测方法及溯源不同有关。此外患者感染的时间不同,也可能会造成检测结果在区间的临界点上下浮动。有研究显示,PCT与IL-8联合检测诊断早期细菌感染的敏感度可达100.0%。尤其在细菌感染24~48 h后,PCT明显升高,并且诊断价值明显优于CRP、IL-8等其他炎症因子[7]。因此,对于PCT的检测应结合临床对患者进行连续检测,不应以单次检测结果作为细菌感染的排除因素,以免造成漏诊,延误病情。
在进行区间一致性分析时,针对每个区间范围内的数据可发现,区间不一致的数据主要体现在区间的临界值,不一致的数据在0.05 ng/mL及0.50 ng/mL的位置较为集中,可能与PCT升高的时限有关。不一致的数据大部分为负偏倚,说明瑞莱TZ-301检测较VIDAS30有偏低趋势。
本研究也有不足之处,对于检测结果所属区间不一致的标本并未寻找第三方仪器进行验证。但是由于目前对PCT的检测并无统一标准,因此,这项试验并不影响对瑞莱TZ-301的总体评价,对于结果不符的标本,可能与仪器溯源不同及标本自身对试验方法的干扰有关。
瑞莱TZ-301检测PCT与VIDAS有较好的相关性,各检测区间的特异度较高,区间分类不一致的标本主要以负偏倚为主。

