肺腺癌恶性胸腔积液EGFR突变检测及其临床意义*
陈轩 李真斌 邹斌 易向军
肺癌是我国最常见的恶性肿瘤之一,近年来发病率呈上升趋势,临床确诊病例70%已为晚期,失去手术机会,尽管不断有新的化疗药物问世,但仍然未突破化疗的瓶颈,患者的预后仍较差,5年生存率不足20%。伴随着分子靶向药物的成功研发,诸如进口的吉非替尼(Gefitinib)、厄洛替尼(Eriotinib)及我国自主生产的埃克替尼(aiketinib)相继被批准上市用于治疗晚期肺癌。靶向治疗是目前肿瘤治疗的新策略之一,也给肺癌患者带来了巨大的希望。2004年,Lynch等[1]和Paez等[2]最先报道肺癌组织中EGFR酪氨酸激酶编码区基因突变是靶向药物治疗有效的一个重要因素。研究证明EGFR基因突变状态与靶向药物的临床疗效密切相关,且EGFR敏感突变阳性者对EGFR-TKI疗效好[3-4]。因此,通过EGFR基因诊断可以筛选出合适的患者进行有针对性的靶向治疗,从而显著提高药物疗效。但是肺癌在确诊时超过70%患者已为Ⅲ、Ⅳ期,肿瘤组织难以获取。鉴于此,能否利用肿瘤患者恶性胸腔积液DNA进行晚期肺腺癌肿瘤细胞基因突变检测[5-6],从而用于EGFR-TKI靶向药物疗效预测将成为研究热点。笔者于2015-2017年采用ARMS法检测肺腺癌患者恶性胸腔积液EGFR突变状态,突变者给予EGFR-TKI治疗,取得较好效果,现报道如下。
1 资料与方法
1.1 一般资料 选取2015年1月-2017年10月江西省胸科医院收治的50例肺腺癌患者的恶性胸腔积液样本50例,其中男23例,女27例,年龄46~80岁,平均年龄63岁。胸腔积液均中找到腺癌细胞。(1)纳入标准:①经胸腔积液细胞学诊断为肺腺癌;②均接受EGFR基因检测;③临床分期为Ⅳ期;④30~70岁,PS 0~2分;⑤无重要脏器功能不全;⑥有至少一个可测量的病灶。(2)排除标准:有严重心脑血管疾病、肝肾功能障碍、肺部感染、既往接受过化疗、合并其他部位原发瘤。该研究已经论理委员会批准,患者知情同意。
1.2 方法 采用Qiagen 51304 QIAamp DNA Mini Kit人类DNA提取试剂盒提取标本胸腔积液DNA,然后使用AmoyDx EGFR ADx-EG0X基因突变检测试剂盒检测EGFR基因的突变情况。胸腔积液有EGFR基因突变的患者口服吉非替尼(生产厂家:AstraZeneca UK Limited,批号:国药准字J20070047)250 mg/次,每日一次;或厄洛替尼(生产厂家:上海罗氏制药有限公司,批号:国药准字J20070031)150 mg/次,每日一次;或埃克替尼(生产厂家:贝达药业股份有限公司,批号:国药准字H20110061)125 mg/次,每日三次,直到病情进展或者因不良反应不能耐受,患者用药时均停用全身化疗1个月。
1.3 疗效评价标准 入组患者于服药前及服药后每4周复查胸CT及转移病灶CT检查。按照实体瘤疗效评价标准,疗效分为完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD)。客观缓解(ORR)=CR+PR,疾病控制(DCR)=CR+PR+SD。无进展生存期(PFS)是指患者从首次用药至观察到疾病进展或因任何原因死亡的时间间隔(以发生在先的事件计算),在数据截止时尚未进展或死亡的患者,及研究中失访的患者将以其最后1次肿瘤评价的时期计算。总生存期(OS)指患者首次用药到由于任何原因死亡,在数据截止日尚生存的患者或在研究中失访的患者将以其最后1次联络的日期作为截尾数值进行分析。
1.4 随访 采用电话方式随访,36例患者均有随访资料,末次随访时间2018年6月30日。
1.5 统计学处理 使用SPSS 19.0统计学进行分析,计数资料采用率(%)表示,比较采用字2检验,使用乘积极限法又称Kaplan-Meier法及Logrank法比较生存时间及生存率,以P<0.05为差异有统计学意义。
2 结果
2.1 恶性胸腔积液EGFR基因突变的检出结果 在50例肺腺癌患者恶性胸腔积液中检测到EGFR基因突变36例,突变检出率为72.0%,在这些突变的样本中,外显子19和21突变分别占80.5%(29/36)和 19.5%(7/36)。
2.2 EGFR基因突变与患者临床特点之间的关系 36例EGFR基因突变患者中,1例患者服药1周后症状缓解,5例患者服药2周后症状缓解,26例患者服药1个月后症状缓解,4例患者无效,临床有效率88.9%(32/36)。口服靶向药物1个月后复查CT肺部及转移灶疗效评价,CR 0例,PR 24例,SD8例,PD 4例,客观缓解率为66.7%,疾病控制率为88.9%。整组中位无进展生存期(PFS)为10.0个月(8.6~11.3个月),EGFR 19外显子突变和21外显子突变患者的中位PFS分别为10.0、9.0个月,比较差异无统计学意义(字2=1.548,P=0.213),见图1、2。整组总生存期(OS)为26个月(23.4~28.5个月),1年生存率57.1%,2年生存率21.4%。EGFR19外显子突变和21外显子突变患者的中位OS分别为28.0、21.0个月,比较差异有统计学意义( 字2=7.585,P=0.006),见图 3、4。

图1 36例EGFR19外显子和21外显子突变患者无进展生存时间曲线

图2 36例EGFR突变患者无进展生存时间曲线

图3 36例EGFR19外显子和21外显子突变患者总生存时间曲线
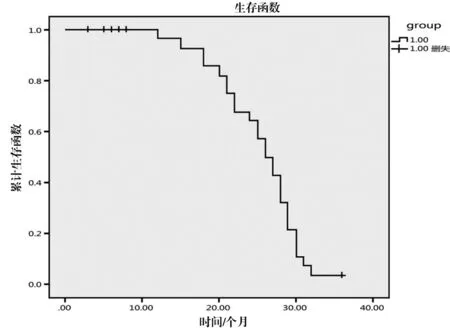
图4 36例EGFR突变患者总生存时间曲线
2.3 靶向治疗的不良反应 对36例胸腔积液EGFR基因突变患者治疗中出现的不良反应进行统计,皮疹最为常见44.4%(16/36),其次为腹泻27.8%(10/36),其他少见的不良反应包括:消化道黏膜炎 11.1%(4/36),食欲减退 8.3%(3/36),乏力5.6%(2/36),咳嗽 2.8%(1/36)等,多数为Ⅰ~Ⅱ度86.1%(31/36),极少数可见Ⅲ度13.9%(5/36),未见Ⅳ度不良反应。见表1。

表1 靶向治疗的不良反应 例
3 讨论
非小细胞肺癌靶向治疗的疗效与EGFR的突变状态密切相关,而且突变基因不同的治疗效果也不尽相同[7-9]。因此明确EGFR基因是否突变及突变类型对指导靶向治疗有很大的帮助。晚期肺癌患者的诊断主要依据病理活检和影像学检查,但晚期肺癌患者已无手术适应证,难以获取病理组织。尽管可通过经皮肺穿刺术、支气管镜等方法获取到组织,但有时癌组织少,难以用于病理免疫组化及基因检测。由此可见,尽快找到方便、快捷而又准确的途径来评价肺癌患者EGFR突变状态显得尤为关键。恶性胸水是晚期肺癌常见并发症之一,而且胸腔闭式引流术或胸膜腔穿刺术是行之有效获取胸腔积液的方法。国外研究报道胸腔积液中肿瘤细胞块DNA可以检测到一些癌基因突变,与原发肿瘤组织的基因突变高度相符[6]。国内也有文献[10]报道在癌性胸水中提取肿瘤细胞DNA,能有效检出EGFR突变,胸腔积液细胞块与组织样本在EGFR基因突变上具有较高的一致性。万莉娟等[11]发现胸腔积液与肿瘤组织EGFR基因突变的符合率达到80%以上,这两种标本来源对EGFR检测的突变比较,差异无统计学意义(P>0.05)。
吉非替尼、厄洛替尼和埃克替尼均是高效、选择性的EGFR酪氨酸激酶抑制剂,抑制肺癌细胞的游走、黏附、侵袭和血管新生,促使肺癌细胞凋亡。这三种EGFR-TKI类药物均可用于EGFR突变敏感型的非小细胞肺癌的靶向治疗,且疗效和不良相好似[12]。国内易涵等[13]研究显示吉非替尼、厄洛替尼和埃克替尼三组药物治疗晚期非小细胞肺癌的客观有效率分别为66.7%、70.0%和63.3%,比较差异均无统计学意义(P>0.05);无进展生存期分别为0.934、1.079和1.063年,生存曲线比较差异无统计学意义(F=0.001,P=0.999 0),不良反应主要为皮疹、腹泻。该研究结果与本研究结果相仿(客观缓解率66.6%,中位无进展生存期为10.0个月,中位总生存期为26个月),值得注意的是:本研究是采用恶性胸腔积液检测EGFR基因突变状态,虽然与易涵等[13]采用的组织标本不同,但研究结果却高度相似,而且本研究还发现EGFR19外显子突变的患者比21外显子突变患者在中位生存期上获益更大,中位OS:28.0个月 vs 21.0个月,比较差异有统计学意义(字2=7.585,P=0.006)。文献[14]得出更好的结果(中位PFS 14.3个月,中位OS 30.8个月)。EGFR-TKI治疗EGFR突变敏感型的非小细胞肺癌患者,不仅疗效确切,而且不良反应多可为患者耐受,未见严重不良反应发生。在本研究中仅观察到轻至中度的不良反应,例如皮疹、腹泻、黏膜炎等,与国内外相关文献[15-16]报道结果相似。综上分析初步认为恶性胸腔积液可以作为肺腺癌患者进行EGFR基因突变的检测标本,进而可预测靶向治疗的疗效,但仍然需要大样本的循证医学证据进一步证实。
以前临床上EGFR突变最常用的检测方法是直接测序法,被称为检测基因突变的“金标准”,能明确目的片段中每一个碱基状态,但也有不足之处,其测序图谱有时令研究者很难做出准确判断。伴随着基因测序技术的发展,诸如突变扩增阻滞技术(ARMS法)等更先进技术运用于临床基因测序。有研究证明,ARMS法操作简单,突变检出率高于直接测序法[17]。而且上海市肺科医院的任睿欣等[18]研究显示:ARMS法检测NSCLC微小标本(CT引导下经皮肺穿刺活检标本,支气管内超声引导下针吸活检标本,淋巴结针吸活检活检标本,支气管镜活检标本以及胸腔积液等)也能获得较高的EGFR突变检出率,对于晚期肺癌难以取得大标本的患者,微小标本可代替大标本用于临床EGFR突变检测,丰富了晚期肺癌患者基因检测的取材途径及方法。本研究采用ARMS法对50例肺腺癌恶性胸腔积液进行了EGFR基因突变检测,突变者36例,突变检出率为72.0%,更好地指导了临床靶向用药,减轻了患者的痛苦,取得了较好的疗效。现今二代基因测序技术高通量测序技术(NGS法)已经逐渐运用于临床,具有更高效的灵敏度,使得可以抽取静脉血用于检测基因突变,且检测率与运用胸腔积液的检出率相当[19],文献[20]显示外周血与病理组织切片EGFR基因检测结果一致性较好,使得外周血基因检测有可能成为临床无法取得病理组织标本患者的替代选择,方便了基因检测的取材,更好地造福了患者。

