西达本胺治疗外周T细胞淋巴瘤的效果和安全性分析
王杰松,何鸿鸣,杨 瑜,林剑扬,郑艳彬,吴 晖,陈道光,陈 英,陈宁斌,邹思平,陈秀容,王 畅
外周T细胞淋巴瘤(PTCL)是一种高度异质性的淋巴细胞恶性增殖性疾病,是非霍奇金淋巴瘤(NHL)的常见类型,约占NHL的7%[1-2]。PTCL病情进展迅速,易侵袭,预后较差,有研究显示,PTCL患者的5年生存率仅为30%[3]。目前,PTCL治疗仍以化疗为主,常见化疗方案为CHOP或类CHOP方案等,这些方案虽有一定疗效,但总体效果欠佳,并不能显著延长患者生存期[4-5]。西达本胺是一种组蛋白去乙酰化酶(HDAC)抑制剂,是由我国自主研发的治疗复发或难治性PTCL的新型药物。临床研究显示,西达本胺在体内、体外实验中均具有显著抗肿瘤作用且安全性良好[6-7],目前国内缺乏其临床应用的相关报道。本研究旨在评价西达本胺对PTCL的疗效和安全性。现报告如下。
1 资料与方法
1.1一般资料 选取2015年4月—2017年9月福建省肿瘤医院淋巴瘤头颈部肿瘤内科收治的PTCL 25例。①纳入标准:经组织病理学检查确诊为PTCL;年龄≥18岁;入组前4周内未接受抗肿瘤治疗;对研究知情并签署知情同意书。②排除标准:合并严重心、肝、肾功能不全者;合并其他血液疾病者;伴其他类型恶性肿瘤者;妊娠期或哺乳期女性。本组男8例,女17例;年龄33~81(56.84 13.45)岁;病理类型:非特异性外周T细胞淋巴瘤(PTCL-NOS)8例,血管免疫母细胞性T细胞淋巴瘤(AITL)9例,间变性大细胞淋巴瘤(ALCL)8例;临床分期:Ⅱ期15例,Ⅲ~Ⅳ期10例;B症状:无10例,有15例;结外浸润:无13例,有12例;骨髓浸润:无21例,有4例。
1.2治疗方法 给予西达本胺片(深圳微芯生物科技股份有限公司,国药准字:20150224)30 mg口服,2/周,连续服用4周,停2周,以6周为1个周期。共治疗4个周期。本组16例采取西达本胺单药治疗,9例采取西达本胺联合治疗(沙利度胺、泼尼松)。治疗过程中给予对症支持治疗。
1.3效果评价 参照淋巴瘤疗效评价标准进行疗效评价[8]:完全缓解(CR)、部分缓解(PR)、病情稳定(SD)及疾病进展(PD)。近期疗效指标为客观有效率(ORR),ORR=(CR+PR)/总例数×100%;远期疗效指标为无进展生存期(PFS),是指患者从开始化疗到疾病进展或死亡时间。统计治疗期间不良反应发生情况,评价标准参照NCI CTC3.0版标准[9],以定期复查或电话访问对患者进行随访,随访截止时间为2018年3月。
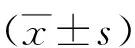
2 结果
2.1近期疗效 本组16例单药治疗患者中,CR 6例、PR 4例、SD 3例、PD 3例,ORR为62.50%(10/16)。9例联合治疗患者中,CR 3例、PR 2例、SD 1例、PD 3例,ORR为55.56%(5/9)。
2.2近期疗效与临床病理参数的关系 经分析显示,西达本胺单药治疗及联合治疗PTCL的近期效果与性别、年龄、病理类型、临床分期、治疗前乳酸脱氢酶、治疗前EB病毒-DNA、结外侵润、骨髓侵润等临床病理参数均无相关性(P>0.05)。见表1和2。
2.3远期疗效 单药治疗患者的1年无进展生存率为56.25%(9/16),2年无进展生存率为43.75%(7/16),中位PFS为11个月(2~23个月);联合治疗患者的1年无进展生存率为77.78%(7/9),2年无进展生存率为66.67%(6/9),中位PFS为15个月(3~28个月)。
2.4不同近期疗效者无进展生存率及无进展中位PFS比较 单药治疗有效患者2年无进展生存率为60.00%,中位PFS为16个月(7~23个月);单药治疗无效患者2年无进展生存率为16.67%,中位PFS为4个月(2~7个月);单药治疗有效患者2年无进展生成率及中位PFS优于无效患者(P<0.05)。联合治疗有效患者2年无进展生存率为80.00%,中位PFS为21个月(10~28个月);联合治疗无效患者2年无进展生存率为50.00%,中位PFS为5个月(3~9个月);联合治疗有效患者2年无进展生成率及中位PFS优于无效患者(P<0.05)。
2.5不良反应 本组共发生45例次不良事件,其中单药治疗患者24例次、联合治疗患者21例次,常见不良反应为乏力、厌食、白细胞或中性粒细胞降低、头晕,且均可耐受。不良反应程度及发生系统见表3和4。

表1 西达本胺单药治疗外周T细胞淋巴瘤的近期疗效与临床病理参数的关系(例)

表2 西达本胺联合治疗外周T细胞淋巴瘤的近期疗效与临床病理参数的关系
3 讨论
PTCL包括PTCL-NOS、AITL、ALCL等病理类型,其中以PTCL-NOS最为常见。PTCL虽发病率较低,但异质性较高,易侵袭,故预后较差[10]。目前,对PTCL尚缺乏理想的治疗方案,临床主要参照B细胞淋巴瘤标准,予以CHOP或类CHOP方案治疗,但疗效差,ORR偏低且易出现复发[11]。大强度的蒽环类化疗亦未能明显提高PTCL的治疗效果,反而增加了药物毒副反应[12]。近年文献报道,吉西他滨治疗PTCL取得较好疗效,且包含吉西他滨的GDP方案被认为优于CHOP方案,有望成为治疗PTCL的一线方案[13]。然而,对于复发或难治性PTCL,至今缺乏有效治疗方案,自体干细胞移植对治疗该类患者有效,但其确切效果还有待观察[14]。因此,靶向药物的开发应用成为医学界研究的热点。

表3 16例单药治疗外周T细胞淋巴瘤患者的不良反应发生情况(例)

表4 9例联合治疗外周T细胞淋巴瘤患者的不良反应发生情况(例)
近年研究发现,表观遗传学与肿瘤发生、发展密切相关,有望成为治疗新思路[15]。表观遗传学是指DNA序列未发生改变的情况下,基因出现了异常表达。组蛋白乙酰化和去乙酰化是基因调控过程中的重要环节[16]。研究显示,HDAC活性异常增强与肿瘤发生、进展紧密相关,而通过HDAC抑制剂抑制其活性,能够抑制血管形成、诱导细胞凋亡、促进细胞分化,从而发挥抗肿瘤作用[17]。罗米地辛、贝利司他是国外针对PTCL治疗而研究的HDAC抑制剂,目前仍处于临床研究阶段。
西达本胺则是我国自主研发的HDAC抑制剂,已成功获取Ⅰ类新药,于2014年开始在国内应用于复发及难治性PTCL的治疗。本组25例PTCL的ORR为60.00%,这与相关报道接近[18],表明西达本胺治疗复发或难治性PTCL有较好近期疗效。国外研究显示,西达本胺对血液系统肿瘤疗效确切,尤以PTCL获益最大[19]。而该药至今在国内仍处于初步临床研究阶段,相关报道极为缺乏。陈聪杰等[20]报道结果显示,经过西达本胺6个月治疗,PTCL患者血常规恢复,脾脏及淋巴结明显缩小,亦支持了西达本胺治疗PTCL的有疗效。 本研究结果显示,西达本胺单药和联合治疗PTCL的近期疗效与性别、年龄、病理类型、临床分期、治疗前乳酸脱氢酶、治疗前EB病毒-DNA、结外浸润、骨髓浸润等临床病理参数无关。但本研究纳入病例较少,其结果还有待进一步探讨。本组单药治疗患者的1年和2年无进展生存率分别为56.25%和43.75%,中位FPS为11个月,联合治疗患者的1年和2年无进展生存率分别为77.78%和66.67%,中位FPS为15个月。提示西达本胺治疗复发或难治性PTCL可取得较好远期疗效。一项纳入79例难治性PTCL的西达本胺Ⅱ期临床试验显示[21],患者中位生存时间为21.4个月,高于本研究,可能与纳入对象、用药方法存在差异有关。曹利红等[22]报道,采用西达本胺治疗急性髓系白血病的生存时间超过12个月,亦体现了西达本胺的应用价值。本研究结果显示,近期有效患者2年无进展生存率及中位PFS均明显优于无效患者,提示近期疗效好的患者预后更好。
本组治疗过程中不良反应以乏力、厌食、血白细胞或中性粒细胞降低、头晕较为常见,但以Ⅰ度反应为主,均未出现Ⅳ度不良反应,提示西达本胺耐受性较好。Marquard等[23]开展的西达本胺Ⅰ期临床试验亦证实患者对西达本胺耐受性较好,安全事件可控,单药可使PTCL患者获益。
综上所述,西达本胺单药及联合治疗PTCL疗效较好,安全性较高,为复发及难治性PTCL患者的治疗提供了新的选择,但其疗效的优越性仍需更多循证医学证据支撑。

