基于食品液态体系的功能因子靶向传输系统的构建及其释放研究
徐捍山 ,郑波 ,李琳 ,3,陈玲 ,3
(1.东莞理工学院化学工程与能源技术学院,广东东莞 523000)(2.华南理工大学食品科学与工程学院,广东广州 510640)(3.广东省天然产物绿色加工与产品安全重点实验室,广东广州 510640)
功能食品除了具有一般食品皆具备的营养功能和感官功能(色、香、味)外,还具有一般食品所没有或不强调的调节人体生理活性的功能[1,2]。而功能因子是功能食品的物质基础,主要包括多肽及蛋白质、益生菌、抗氧化剂、多不饱和脂肪酸、膳食纤维、低聚糖、糖醇等[3,4]。要实现功能因子的生理功能,需要依靠一定的载体材料加工成功能食品,被人体服用后能在相应的部位被吸收利用。对于食品功能因子传输体系,其载体材料不仅要抵御食品加工储藏过程中的各种侵扰,又要避免活性功能物质在上消化道中失活[5,6]。
目前,前人的研究对功能因子的储藏稳定性和生物利用性均有涉及,但研究仅仅涉及其中一个方面,还未能将两者进行综合考虑。功能因子的储藏稳定性和控制释放是通过一定的微囊化控释传输系统来实现的。微丸微囊化控释传输系统由于其独特的优点,已成为一种很有潜力的倍受关注的控释传输系统。淀粉作为一种天然多糖高分子化合物,具有来源丰富、价廉、可再生不枯竭、可生物降解和生物相容性好等优点,常被改性后用来作为微囊载体材料。根据淀粉的消化速率和程度,淀粉通常被分为快消化淀粉(RDS)、慢消化淀粉(SDS)和抗消化淀粉(RS)三部分[7]。其中,抗消化淀粉在上消化道中不被消化,而在结肠中能被微生物菌群降解,产生短链脂肪酸,维持肠道健康[8]。醋酸酯淀粉是利用化学改性得到的一种具有糊化温度低、粘度高、不易凝沉和储存稳定等优点的抗消化淀粉,是一种理想的用作活性功能物质传输的载体材料[9]。
因此,本研究以醋酸酯抗消化淀粉作为薄膜包衣载体材料,以5-氨基水杨酸作为模型功能因子,通过对薄膜包衣工艺的调整,构建醋酸酯抗消化淀粉薄膜包衣微丸,考察醋酸酯抗消化淀粉成膜工艺对功能因子在液态食品储藏过程及模拟人体消化道环境中的控释行为的影响规律及微丸表面醋酸酯抗消化淀粉薄膜包衣膜层的形貌变化,为筛选适合液态食品体系的功能因子控释传输载体材料及控释传输系统的构建奠定基础。
1 材料与方法
1.1 原料与试剂
醋酸酯淀粉,实验室自制,取代度DS=1.9;药用淀粉,药用级,佛山市华昊华丰淀粉有限公司;微晶纤维素,药用级,佛山市华昊华丰淀粉有限公司;5-氨基水杨酸,药用级,武汉远城科技发展有限公司;全脂灭菌纯牛乳,食品级,内蒙古伊利实业集团股份有限公司;其他试剂均为分析纯。
1.2 主要仪器设备
挤出-滚圆制粒机(Mini-250),深圳信宜特科技有限公司;流化包衣机(Mini-XYT),深圳信宜特科技有限公司;电子分析天平(BS210S),德国Sartorius公司;智能药物溶出仪(RCZ-8B),天津天大天发科技有限公司;溶出仪自动取样器(RCZ-8C),天津天大天发科技有限公司;紫外可见分光光度计(UV-2102PC),尤尼柯(上海)仪器公司;扫描电子显微镜(EVO18),德国Zeiss公司;恒温磁力搅拌器(85-2),常州澳华仪器有限公司。
1.3 醋酸酯抗消化淀粉薄膜包衣微丸液态食品传输体系的构建
1.3.1 荷载功能因子丸芯的制备
以5-氨基水杨酸为模型功能因子,称取一定量的5-氨基水杨酸、微晶纤维素和药用淀粉(其中,微晶纤维素和药用淀粉的比例为3:1),混合均匀。加入物料重量1.7倍的蒸馏水,使物料粘合,具有一定的可塑性。选择孔径为0.7 mm的孔板,物料放入到挤出圆筒,在50 r/min的转速下将物料挤出推进并通过孔板,获得圆柱状条形物,然后放入滚圆装置,在500~700 r/min的转速下将条形物打断,并在300 r/min的转速下滚成圆球。在挤出滚圆过程中,开启冷却装置,保持系统温度在 5~10 ℃下,最大限度的保持功能因子的活性。制备好的丸芯,置于 45 ℃烘箱中,烘干24 h后,按实验要求过筛,得到一定大小的丸芯。
1.3.2 醋酸酯抗消化淀粉薄膜包衣微丸液态食品传输体系的构建
将一定量的醋酸酯抗消化淀粉溶于适合的有机溶剂中,配制成醋酸酯抗消化淀粉浓度为 4%的溶液,添加占醋酸酯抗消化淀粉干基重量20%的三乙酸甘油酯,磁力搅拌8 h。在风机转速为1500~1800 r/min、物料温度25~29 ℃、进风温度40~4 ℃、流化压力和雾化压力为 0.01~0.1 MPa和包衣液进样流速为 5~7 r/min的条件下,对上述制备好的丸芯进行包衣制备微丸。然后称取1.000 g制备好的微丸投入100 g新鲜发酵的酸奶中,搅拌均匀,置于4 ℃下储藏。
1.4 醋酸酯抗消化淀粉薄膜包衣微丸的性质测定
1.4.1 5-氨基水杨酸测定方法的建立
1.4.1.1 最大吸收波长的确定
采用紫外分光光度法,称取适量的5-氨基水杨酸(5-ASA),分别用pH=1.2的盐酸溶液、pH=6.8的磷酸盐缓冲液和 pH=7.0的磷酸缓冲液溶解,然后定容至50 mL,摇匀后分别进行紫外扫描,得到5-ASA在pH=1.2的盐酸溶液、pH=6.8的磷酸盐缓冲液和pH=7.0的磷酸缓冲液中的最大吸收波长分别为302 nm、330 nm和329 nm。
1.4.1.2 标准曲线的绘制
分别用pH=1.2的盐酸溶液、pH=6.8的磷酸盐缓冲液和 pH=7.0的磷酸缓冲液配制系列浓度为:0.000015 g/mL、0.00002 g/mL、0.000025 g/mL、0.00003 g/mL、0.000035 g/mL、0.00004 g/mL和0.000045 g/mL的5-ASA标准溶液。以pH=1.2的盐酸溶液、pH=6.8的磷酸盐缓冲液和pH=7.0的磷酸缓冲液为空白对照,分别在波长为302 nm、330 nm和329 nm波长处测定不同浓度的5-ASA标准溶液的吸光度A,以5-ASA的浓度C与吸光度A的关系曲线,用最小二乘法进行线性回归,得到人工胃液、人工小肠液和人工结肠液中5-ASA的浓度C与吸光度A的关系:
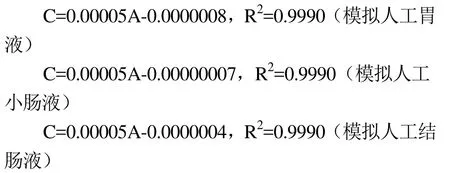
1.4.2 在酸奶储藏期间的释放行为
将储藏一定时间的酸奶中的醋酸酯淀粉薄膜包衣微丸取出,用蒸馏水洗净。用一定量的 pH=1.2的盐酸溶液浸泡、研磨、充分溶解和过滤,将滤液定容至100 mL的容量瓶中,稀释50倍,测定5-ASA在302 nm波长下的吸光度A,并通过标准曲线计算得到微丸中功能因子的残留量。累积释放率计算如下:

1.4.3 在酸奶储藏期间表面形貌的变化
将储藏一定时间的酸奶中的醋酸酯抗消化淀粉薄膜包衣微丸取出,用蒸馏水洗净,在45 ℃下干燥12 h。将微丸固定于样品台上喷金处理,并在真空条件(10-5kPa)下利用SEM进行观察,拍摄具有代表性的醋酸酯抗消化淀粉薄膜包衣微丸的表面形貌照片。
1.4.4 在体外模拟消化道环境中的释放行为
将储藏一定时间的酸奶中的醋酸酯抗消化淀粉薄膜包衣微丸取出,用蒸馏水洗净,置于200 mL溶出介质中,在水浴温度为37 ℃,搅拌转速100 r/min的条件下进行模拟。依据人体胃肠道中食物转运时间,微丸在模拟人体消化道中活性物质释放的考察时间分别设置为:人工胃液2 h,人工小肠液6 h,人工结肠液40 h,每次更换溶出介质在5 min中内完成。并在设定时间1 h、2 h、4 h、6 h、8 h、10 h、12 h、16 h、20 h、24 h、30 h、36 h、42 h和48 h进行取样,取样体积为5 mL,测定其在相应波长下的吸光度A。
1.4.5 在体外模拟消化道环境中表面形貌变化
将储藏一定时间的酸奶中的醋酸酯抗消化淀粉薄膜包衣微丸取出,用蒸馏水洗净。放入溶出仪的溶出杯中,加入200 mL模拟人工胃液,2 h后更换溶出介质为模拟人工小肠液,再过6 h后更换溶出介质为模拟人工结肠液,水浴温度为37 ℃,搅拌桨转速为100 r/min。根据食物在人体消化道中的运转时间,分别在2 h、8 h、24 h和48 h对醋酸酯淀粉膜包衣微丸进行取样。取样后的微丸,用蒸馏水冲洗干净,吸去表面的水分,在45 ℃下烘干12 h。
将上述的醋酸酯抗消化淀粉薄膜包衣微丸经喷金处理,固定于样品台上,在真空条件下利用 SEM 进行观察,拍摄具有代表性的薄膜包衣微丸的表面形貌照片。
1.5 数据统计分析
采用Excel 2013软件建立数据库,通过SPSS19.0统计软件进行数据处理,检验水准取p=0.05,所有数据均以±sd表示,并采用origin 8.5作图。
2 结果与讨论
2.1 酸奶储藏期间醋酸酯抗消化淀粉薄膜包衣微丸的稳定性
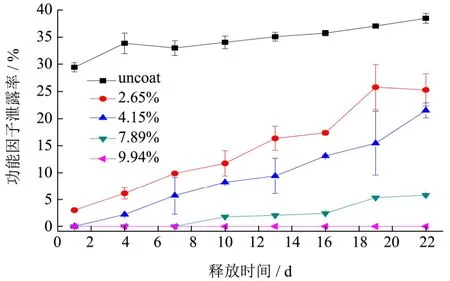
图1 醋酸酯抗消化淀粉包衣增重对功能因子在酸奶储藏期间泄漏量的影响Fig.1 Effect of coating thickness on the 5-ASA release from RSA coated microparticles during yoghourt storage
由图1中数据对比可知,随着储藏时间的增加,功能因子的泄漏量逐渐增加。在相同的储藏时间下,醋酸酯抗消化淀粉薄膜包衣增重越大,功能因子的泄漏量越低。这是由于酸奶中的乳酸菌、酸、水与醋酸酯抗消化淀粉薄膜中淀粉分子相互作用引起的。且随着储藏时间的延长,醋酸酯抗消化淀粉薄膜的降解程度逐渐增大,淀粉分子链发生重排,导致醋酸酯抗消化淀粉薄膜刚性增大,容易发生脆化[10,11]。当包衣厚度为9.94%,其第22 d泄漏量几乎为0。因此对包衣厚度为9.94%微丸通过扫描电镜进行表面形貌观察。
2.2 酸奶储藏期间醋酸酯抗消化淀粉薄膜包衣微丸表面形貌的变化

图2 包衣增重为9.94%醋酸酯抗消化淀粉薄膜包衣微丸经过不同储藏时间后表面形貌变化Fig.2 The surface of RSA coated microparticles with coating thickness of 9.94% during yoghourt storage
由图2可知,酸奶储藏1 d后,包衣厚度为9.94%的醋酸酯抗消化淀粉薄膜包衣微丸表面仍然完整,与未储藏的微丸表面形貌相似。
由于包衣增重为9.94%,丸芯外的醋酸酯抗消化淀粉包衣厚且致密,在后续的酸奶浸泡储藏过程中,薄膜包衣微丸的表面形貌并无变化,微丸浸泡7 d后也没有裂痕或破损出现,与未浸泡的微丸表面相似。当储藏时间延长到13 d后,微丸表面仅有少量裂痕出现。储藏19 d后,微丸表面形貌与储藏13 d后的相近。因此,包衣厚度为9.94%的醋酸酯抗消化淀粉薄膜包衣微丸在酸奶储藏过程中,功能因子基本不泄漏。
2.3 醋酸酯抗消化淀粉薄膜包衣微丸在体外模拟消化道环境中的释放行为
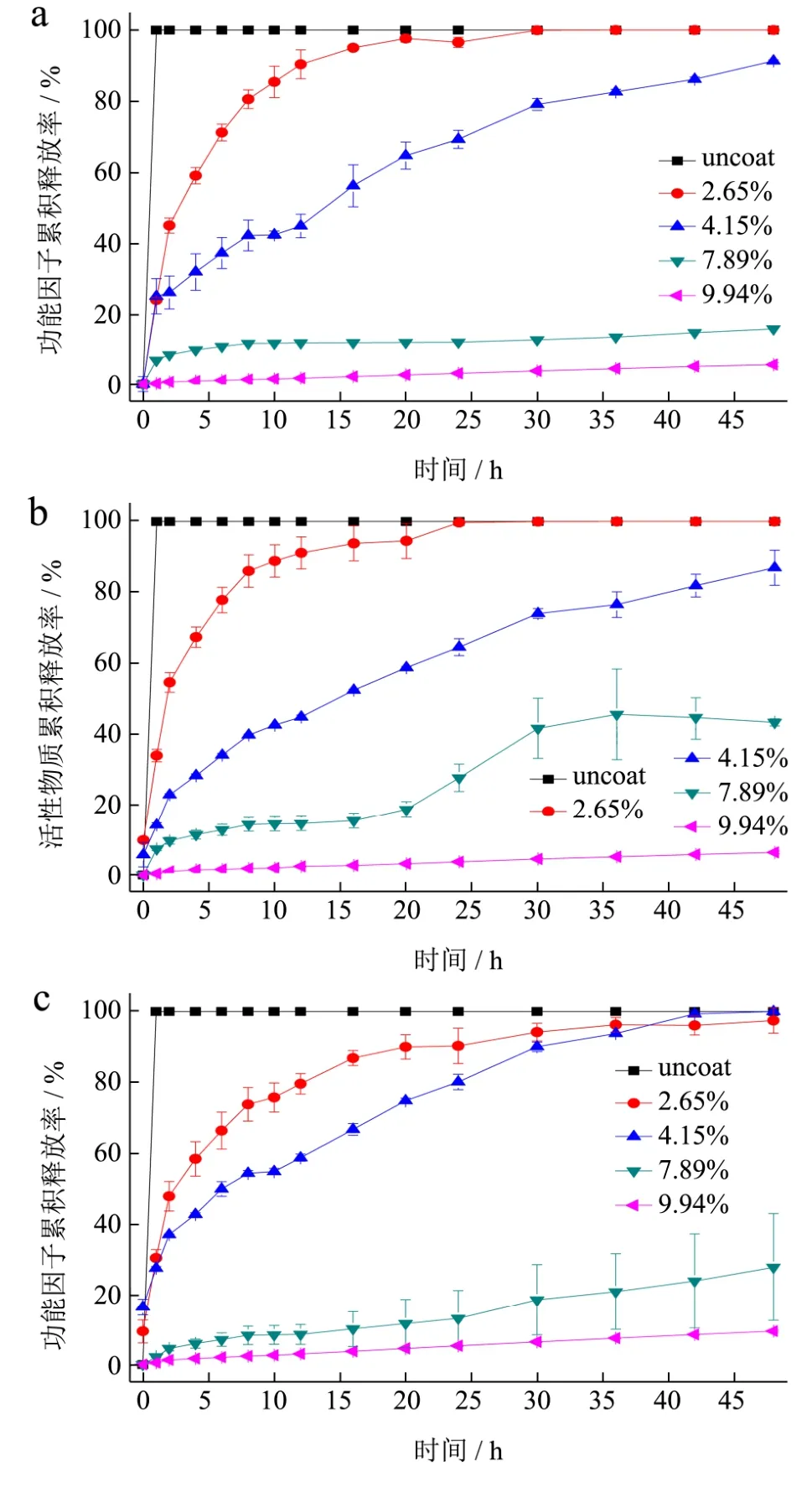
图3为酸奶储藏不同时间后,不同包衣厚度的醋酸酯抗消化淀粉薄膜包衣微丸在模拟人体消化道中的释放情况。
由图3结果可知,酸奶储藏时间越久,相同包衣厚度的醋酸酯抗消化淀粉薄膜包衣微丸在进入人体消化道环境中,功能因子的释放量越大。在相同的储藏时间下,功能因子在胃肠道中的累积释放率,随着包衣厚度的增加而逐渐下降。
2.4 醋酸酯抗消化淀粉薄膜包衣微丸在体外模拟消化道环境中表面形貌的变化

图5 酸奶储藏7 d后包衣增重为9.94%醋酸酯抗消化薄膜包衣微丸在模拟人体消化道环境中形貌变化Fig.5 The surface of RSA film coated microparticles in GI tract after storing in yoghourt for seven days (with coating thickness of 9.94%)

图6 酸奶储藏13 d后包衣增重为9.94%醋酸酯抗消化薄膜包衣微丸在模拟人体消化道环境中形貌变化Fig.6 The surface of RSA film coated microparticles in GI tract after storing in yoghourt for thirteen days (with coating thickness of 9.94%)

图7 酸奶储藏19 d后包衣增重为9.94%醋酸酯抗消化薄膜包衣微丸在模拟人体消化道环境中形貌变化Fig.7 The surface of RSA film coated microparticles in GI tract after storing in yoghourt for nineteen days (with coating thickness of 9.94%)
图4至图7为酸奶储藏不同时间后,包衣增重为9.94%的醋酸酯抗消化淀粉薄膜包衣微丸在模拟人体消化道环境中浸泡不同时间的表面形貌。由于包衣膜层较厚,酸奶储藏1 d后,包衣增重为9.94%的醋酸酯抗消化薄膜包衣微丸在模拟胃液中浸泡2 h后,微丸表面并无破损,当微丸继续在模拟小肠液中浸泡6 h后,微丸表面的包衣膜层仍然完整。随着运转时间的增加,微丸的表面形貌逐渐出现孔洞,因此,功能因子的释放较小。在酸奶中浸泡储藏了7 d后,包衣增重为9.94%的醋酸酯抗消化薄膜包衣微丸在后续模拟消化道环境中的运转过程中,微丸的表面形貌变化与储藏1 d的相似。当酸奶储藏13 d后,包衣增重为9.94%的醋酸酯抗消化薄膜包衣微丸在模拟胃液中浸泡2 h后,其表面有细小的裂痕,随着运转时间的增加,微丸表面的裂痕变大,但表面的包衣膜层并没有出现松脱,丸芯与周围的模拟消化液接触程度有限,功能因子释放量不大。酸奶储藏19 d后,包衣增重为9.94%的醋酸酯抗消化薄膜包衣微丸在模拟胃液中浸泡2 h后,其表面已有破损。当微丸继续在模拟小肠液和人工结肠液中浸泡后,微丸表面的破损程度增大,丸芯中的功能因子得以均匀地释放出来。
3 结论
本研究探讨了不同包衣厚度的醋酸酯淀粉薄膜包衣微丸在酸奶中储藏过程以及后续的体外模拟人体消化道运转过程中功能因子的释放规律及微丸表面包衣膜层的微观形貌变化。在相同的储藏时间下,包衣厚度越大,微丸表面包衣膜层越完好,越能有效阻止功能因子的释放;当醋酸酯抗消化淀粉包衣增重达到9.94%时,其中的功能因子在储藏22 d不释放;加大包衣厚度,醋酸酯抗消化淀粉薄膜包衣微丸能有效抵御液态食品体系的侵蚀;同时,在酸奶中储藏不同时间后,不同包衣厚度的微丸在模拟消化道中运转时的表面形貌变化与其释放情况相符;醋酸酯淀粉薄膜在酸奶储藏过程和体外模拟人体消化道环境中展现了良好的储藏稳定性和结肠靶向性。本研究的结果为液态食品体系中功能因子生理功能的提高提供了新途径,也为淀粉的高附加值利用提供了新思路。

