17例获得性反应性穿通性胶原病临床分析
韩毓梅 胡东艳 李 明 王 强 申 晨 辛崇美
获得性反应性穿通性胶原病(acquired reactive perforating collagenosis,ARPC)是一种变性胶原经表皮排出的穿通性疾病。表现为黄豆大红色丘疹,中央凹陷,内见角质栓,伴有剧烈瘙痒。临床上可与湿疹、结节性痒疹等疾病混淆。本文旨在加强临床医生对本病的认识,早期诊断、早期干预,避免病情加重,提高患者生活质量。现汇总本科经临床及病理确诊的17例ARPC病例进行分析讨论。
1 资料与方法
17例ARPC患者为2016年1月至2018年7月来我院就诊,4例住院病人分别来自心内科、肾内科、皮肤科,其余来自我科门诊。其中男8例,女9例,年龄19~81岁,平均(51.06±16.82)岁。病程1周~5年,平均(9.54±0.56)个月。所有患者皆记录皮损形态、伴发疾病、家族史等资料,查血常规、肝肾功能、糖代谢、血脂、自身抗体、电解质、离子浓度,并予病理活检、HE、Masson、胶原蛋白染色明确诊断。治疗1个月后随访疗效。见表1。
2 结果
2.1 临床表现 皮疹可分布全身,躯干(14例,82.35%)、双下肢(13例,76.47%)是好发部位,头部未见皮疹。10例(58.82%)患者累及2个部位以上。一般对称发生,2例见于单侧(11.76%)。初为针尖大小淡红色丘疹、斑丘疹,可有明显瘙痒,后逐渐增大,中央凹陷,呈脐凹状或杯状,内含黄色、褐色角栓物质,质硬,不易抠除,周围绕以红晕。呈对称性散在分布(图1a、1b),部分患者(8例,47.06%)因剧烈搔抓见同形反应(图1c)。本病未经治疗可自愈,愈后遗留色素沉着或瘢痕,也可反复发作。搔抓剧烈可进一步破溃感染,表面见糜烂、渗液、溃疡。
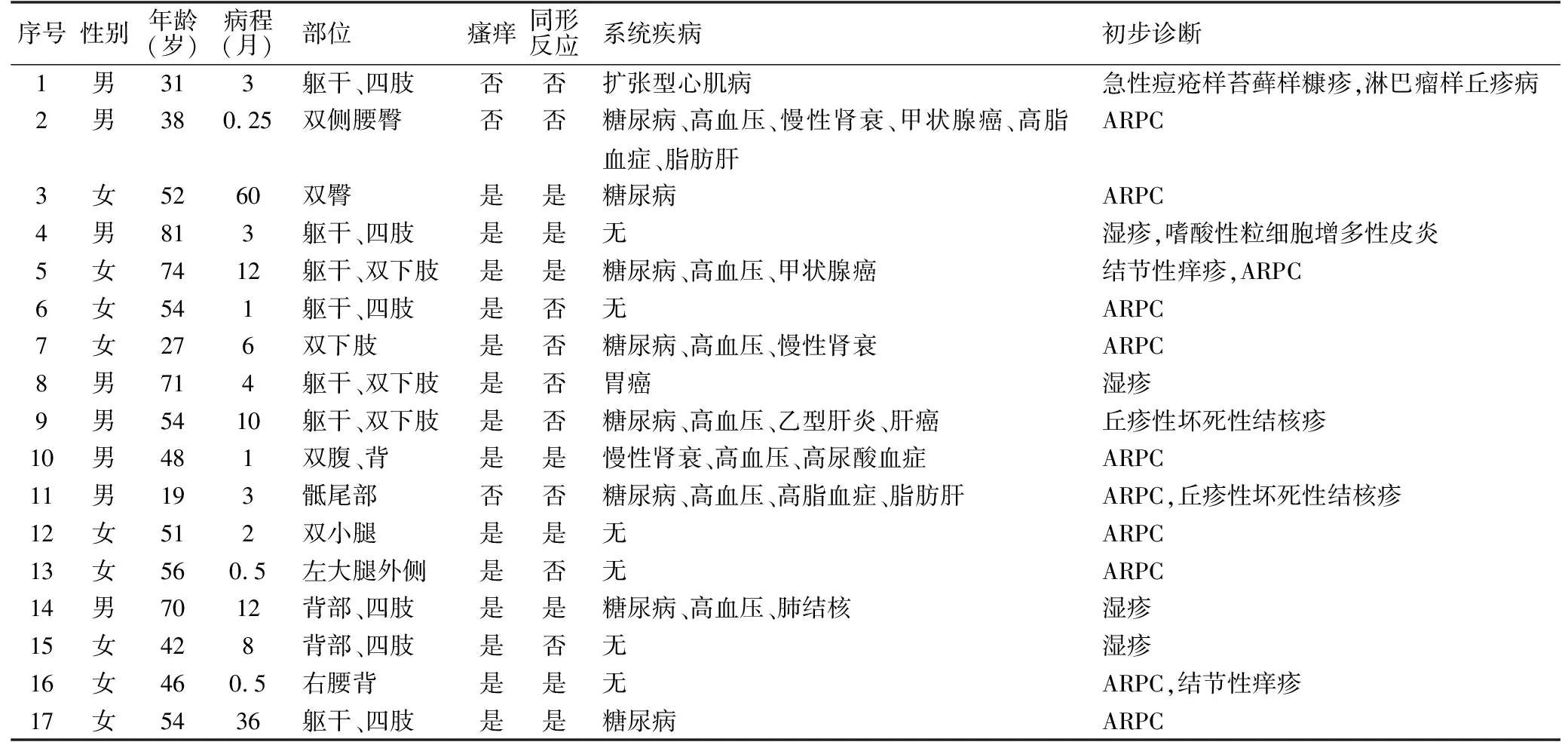
表1 17例获得性反应性穿通性胶原病患者临床资料

图1 获得性反应性穿通性胶原病患者下肢皮损 1a:双下肢散在分布大小不等暗红色丘疹、结节 ;1b:暗红色丘疹中心可见脐凹,内含黄色角栓 ;1c:见明显同形反应图2 获得性反应性穿通性胶原病皮损组织病理学检查 2a:表皮杯状凹陷,内含大量破碎角质、角化不全角质形成细胞碎片、中性粒细胞及嗜碱性胶原纤维(HE,×40);2b:嗜碱性、卷曲、断裂的胶原纤维垂直穿出表皮(HE,×100);2c:蓝染的胶原纤维穿出表皮(Masson,×40);2d:胶原纤维破碎、断裂、变性(Masson,×100)
我科临床误诊率35.29%(6例),最常误诊为湿疹(4例,23.53%)或结节性痒疹、丘疹性坏死性结核疹、淋巴瘤样丘疹病、急性痘疮样苔藓样糠疹等。见表1。
大部分患者(12例,70.59%)伴随其他系统疾病,常见糖尿病(8例,47.06%)、高血压(7例,41.18%)、慢性肾衰(5例,29.41%)(表1)。糖尿病病程在2~20年,平均10年,肾衰病史1~5年。或伴恶性肿瘤(5例,29.41%)、肝脏疾病(3例,17.65%)、高脂血症(2例,11.76%)、心脏疾病。也有29.41%患者(5例)无基础疾病。实验室检查自身抗体皆阴性,基础疾病的相关化验指标有异常,如血糖、糖化血红蛋白、胆红素、肝酶、血脂、肌酐、尿素、血磷。合并感染时血常规可有白细胞、中性粒细胞升高。
2.2 病理特征 皮损病理检查HE染色可见杯状或盘状下陷的表皮,内含大量破碎角质、角化不全角质形成细胞碎片、中性粒细胞及嗜碱性胶原纤维,可见断裂、卷曲的胶原纤维束垂直表皮穿出;真皮浅层见大量中性粒、少量淋巴细胞浸润(图2a、2b)。Masson染色可见蓝染破碎、断裂、变性的胶原纤维穿出表皮(图2c、2d)。
2.3 治疗与随访 积极控制基础疾病,皮疹治疗以口服止痒药物与外用乳膏为主,合并感染加用系统或局部抗生素。口服常应用抗组胺药物,效果不佳时可予雷公藤或沙利度胺,辅以活血、凉血中药。糖皮质激素乳膏有一定的止痒效果,角栓明显时加用维A酸乳膏。其中8例(47.06%)患者自觉瘙痒缓解,皮疹好转,4例(23.53%)患者病情无明显变化,另外4例(23.53%)有明显新发皮疹。1例在确诊ARPC后1周因心力衰竭死亡。
3 讨论
反应性穿通性胶原病根据病因可分为遗传性和获得性两类,遗传性多见于婴幼儿,获得性则见于成人,常合并其他系统疾病,如糖尿病、慢性肾衰等。Faver[1]于1994年提出本病诊断标准:发病年龄在18岁之后,皮疹为中央见角化过度或杯状凹陷的丘疹,病理示嗜碱性胶原纤维束经表皮排除。
根据以上病例分析,ARPC常见于50岁左右中年人群,无明显性别差异,平均病程9个月余。典型皮损为中央角栓的红色丘疹,一般对称发生,躯干、双下肢是好发部位,头面部少见。多数患者有剧烈瘙痒感,常见同形反应,少数无自觉症状。
本病容易误诊,既往文献误诊率可达47%~77%[2,3]。最常误诊为湿疹,其次结节性痒疹,或是丘疹性坏死性结核疹、急性痘疮样苔藓样糠疹、淋巴瘤样丘疹病、嗜酸性粒细胞增多性皮炎等[3,4]。鉴别要点:1.湿疹,皮疹多形,急性期见丘疹、丘疱疹、水疱,搔抓渗液;慢性期皮疹表面苔藓化。2.结节性痒疹,黄豆至花生米大丘疹、结节,触之坚实感,如搔抓表面可有痂皮,痂皮干燥后较易抠除;组织病理示表皮棘层增厚为主,无变性胶原穿出。3.急性痘疮样苔藓样糠疹,起病急,好发于青少年,皮疹为红斑、丘疹、丘疱疹、水疱、坏死、结痂等多形损害,表面鳞屑,自觉症状不明显。疾病有自限性,愈后留下痘疮样瘢痕。4.丘疹性坏死性结核疹,四肢对称分布散在丘疹,以伸侧为主,顶端可有脓疱,周围红晕,脓疱干涸后形成黏着性褐色厚痂,去除痂皮,中心见凹陷性坏死、溃疡、瘢痕。病理可见血管炎表现及多核巨细胞。查T-spot可能阳性。5.淋巴瘤样丘疹病,表现为慢性、复发性红棕色丘疹、结节,中央出血、坏死、结痂,可自行消退愈合,遗留色素沉着斑或萎缩性瘢痕。病理见异型淋巴细胞浸润。6.嗜酸性粒细胞增多性皮炎,表现为泛发的丘疹、结节,水肿性、浸润性红斑,瘙痒剧烈。可伴全身症状如发热、疲倦、体重下降、水肿、关节肿痛、肌肉疼痛。外周血嗜酸粒细胞增高达1.5×109/L。7.恶性萎缩性丘疹病,初为半球形丘疹,后变平、坏死,中心出现脐凹,有特征性瓷白色萎缩,周边留有线状边缘。伴有胃肠道、中枢神经系统损害。组织病理可见特征性的细小动脉闭塞、神经及皮肤附属器炎性细胞浸润。
本病病因、发病机制至今尚未阐明。糖尿病、高血压、慢性肾衰等基础疾病可能与本病有关。本研究中70%患者伴系统疾病,近半数患糖尿病,其次高血压、肾脏疾病,或肝脏疾病、高脂血症、恶性肿瘤等。既往文献报道伴发系统疾病的比例高,达75%~100%,伴发糖尿病者约在30%~80%、高血压40%~73%、慢性肾衰12%~53%、肝脏疾患12%~20%、高脂血症7%[2-4]。部分患者ARPC起病常在伴发疾病加重恶化后[5]。
研究发现ARPC杯状皮损周围TGF-β3(transforming growth factor-3)、matrix metalloproteinase-1(MMP-1)、tissue inhibitor of metalloproteinase-1(TIMP-1)表达升高,这些细胞因子在创面修复中具有重要作用,可延缓表皮再生和调节表皮重塑,改变细胞外基质蛋白的代谢[6]。目前认为最初可能与搔抓造成皮肤表面微小创伤有关,进而引起真皮乳头胶原纤维坏死;另外,糖尿病血管病变和缺氧引起的小血管供血不足可加重胶原坏死、变性,坏死的胶原经由表皮排出,同形反应可以支持此假说[7]。
治疗原则首先是止痒,积极控制系统疾病。本病反复发作,瘙痒明显,搔抓可加重病情。轻症患者可口服抗组胺药,局部外用润肤剂,角质剥脱剂,如5%水杨酸乳膏、10%~15%尿素乳膏,糖皮质激素制剂。顽固皮损可外用0.1%维A酸类乳膏,或皮损内注射糖皮质激素。病情较重者,可口服小剂量糖皮质激素、阿维A、沙利度胺、雷公藤等。皮损泛发者可用PUVA、308 nm激光、窄波中波紫外线(NBUVB)照射有一定的疗效[8-10]。除此之外,有病例报导别嘌呤醇对本病有治疗效果,具体机制未明。别嘌呤醇可以抑制黄嘌呤氧化酶生成氧自由基,氧自由基可破坏胶原纤维,引起胶原交联[11]。糖尿病、高脂血症、慢性肾衰的患者需合理控制血糖、血脂、肌酐,有助于本病的治疗。个案报道患者血糖调节稳定ARPC好转;控制不佳,病情加重[4],但目前缺乏大样本的相关研究。
本文共汇总17例ARPC病例,归纳疾病特点,有助于对本病进一步认识,达到早期诊断,治疗。ARPC临床上易与其他疾病混淆,应注意鉴别诊断,询问患者伴随系统疾病,如糖尿病、慢性肾衰、高血压、高脂血症等。如这些疾病的患者躯干、双下肢出现瘙痒性黄豆大红色丘疹,中央见角栓,不排除ARPC可能,可予皮肤活检明确诊断。治疗上以止痒为主,并控制基础疾病病情。

