“插空法”巧解气体参与制备类实验综合题
周学兴 杨 华
湖南
实验题是高考必考题型,实验综合题三大类型为物质制备分离型、性质原理探究型、定量分析型,其中制备类实验是最重要的一种基础综合实验,理解好如何制备物质,有助于培养对其他实验的认知。近五年与制备类相关的高考题情况见表1。

表1 近五年高考制备类实验题的考查情况
学生对实验或实验题有着一种复杂的感情“爱看实验,想做实验,又怕做实验”,文章着重介绍了插空法在突破有气体参与的制备类实验题和提高学生实验设计能力、学科素养等方面的应用,以期抛砖引玉。
在教学中鼓励学生尝试实验设计、实践,提高学生实验设计与实践能力。通过思维策略的技巧训练,帮助学生明确解决问题的核心,掌握解决问题的一般程序和方法,提高学生的实验分析能力。在学生完成设计的基础上,再配合学生亲自动手完成自行设计的实验,让学生亲身体验探究过程,这将能非常有效地起到培养科学素养的作用。
一、插空法介绍
插空法,根据实验目的和物质性质确定三大核心装置(供气装置、主要发生装置、尾端装置)为框架,框架间结合性质分析进行插空理解,可以高效解决气体制备类实验综合题,并为展开实验设计提供模型和思路。插空法解题思路,见图1。

图1 插空法解题思路
1.小试牛刀
例1.[2017·全国卷Ⅰ·10]实验室用H2还原WO3制备金属W的装置如图所示(Zn粒中往往含有硫等杂质,焦性没食子酸溶液用于吸收少量氧气)。下列说法正确的是
( )

A.①②③中依次盛装KMnO4溶液、浓H2SO4、焦性没食子酸溶液
B.管式炉加热前,用试管在④处收集气体并点燃,通过声音判断气体纯度
C.结束反应时,先关闭活塞K,再停止加热
D.装置Q(启普发生器)也可用于二氧化锰与浓盐酸反应制备氯气
【解析】插空法:框架插空

图2 制备W的解题模型
【评价】通过插空法,实验装置得以整体把握。诚然,此题难度不大,B项正确,但对于该题实验的严谨性,有待商榷,鼓励学生补充完整,为展开实验打下扎实的基础。
例2.磺酰氯(SO2Cl2)是一种重要的有机合成试剂,实验室可利用SO2与Cl2反应制取少量的SO2Cl2。装置如图(有些夹持装置省略)所示。已知SO2Cl2的熔点为—54.1℃,沸点为69.1℃,在潮湿空气中遇水能发生剧烈的水解反应,并产生白雾。

(1)仪器组装完毕后,检验甲装置气密性的方法是______________,表明装置气密性良好。
(2)仪器C的作用是吸收逸出的有毒气体Cl2、SO2,防止污染环境和__________。
(3)试剂X、Y的组合最好是 (填字母)。
a.18.4 mol/L H2SO4+Cu
b.4 mol/L HNO3+Na2SO3
c.60% H2SO4+K2SO3
(4)戊是贮气装置,则E中的试剂是__________。若缺少装置乙和丁,潮湿的氯气和二氧化硫之间发生反应的化学方程式是__________。
(5)反应结束后,将丙中的混合物分离开的实验操作是____________________。若反应中消耗的氯气的体积为896 mL(已转化为标准状况,SO2足量),最后得到纯净的磺酰氯3.3 g,则磺酰氯的产率为_______(保留三位有效数字)。
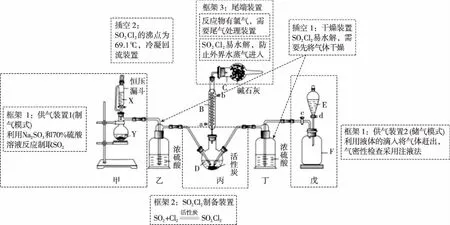
图3 制备SO2Cl2解题认知模型
【答案】

例3.[2018·全国卷Ⅰ·26]醋酸亚铬[(CH3COO)2Cr·2H2O]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价铬;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图所示。回答下列问题:
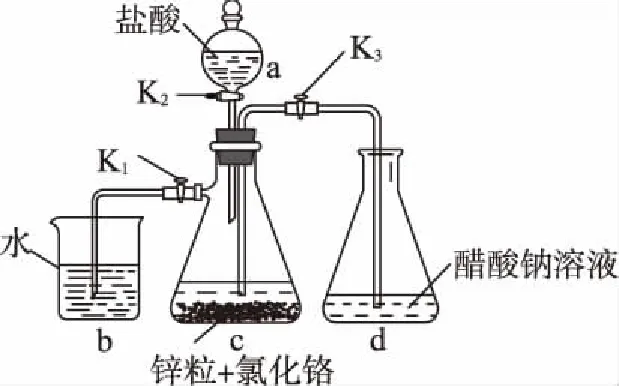
(1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是______________,仪器a的名称是__________。
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置,打开K1、K2,关闭K3。
①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为__________。
②同时c中有气体产生,该气体的作用是__________。
(3)打开K3,关闭K1和K2。c中亮蓝色溶液流入d,其原因是______________;d中析出砖红色沉淀,为使沉淀充分析出并分离,需采用的操作是_________、洗涤、干燥。
(4)指出装置d可能存在的缺点:__________。
【解析】根据题干信息可知,反应物溶液之间并未接触,没有采取分液漏斗加液混合的方式,氢气没有直接参与反应,而是利用氢气产生的压强差将其中一种反应液压入另一反应液混合达到制备目的。类似于氢氧化亚铁的制备。

图4 制备醋酸亚铬的解题模型
【答案】
(1)去除水中溶解氧 分液(或滴液)漏斗

(3)c中产生H2使压强大于大气压 (冰浴)冷却 过滤
(4)敞开体系,可能使醋酸亚铬与空气接触
【评价】诚然,插空法并不拘泥于形式,对该题亦有很好的诠释。同时插空法对于物质的性质探究也有指导意义,因为探究的对象是制备(物质发生反应)产生,框架装置是验证装置。
例4.[2011·课标全国Ⅰ·28(1)节选]氢化钙固体是登山运动员常用的能源提供剂,某兴趣小组拟选用如下装置
制备氢化钙。

请回答下列问题:
(1)请选择必要的装置,按气流方向连接顺序为 (填仪器、接口的字母编号)。
【解析】采用插空法可迅速解决装置连接问题。
插空法:框架→插空
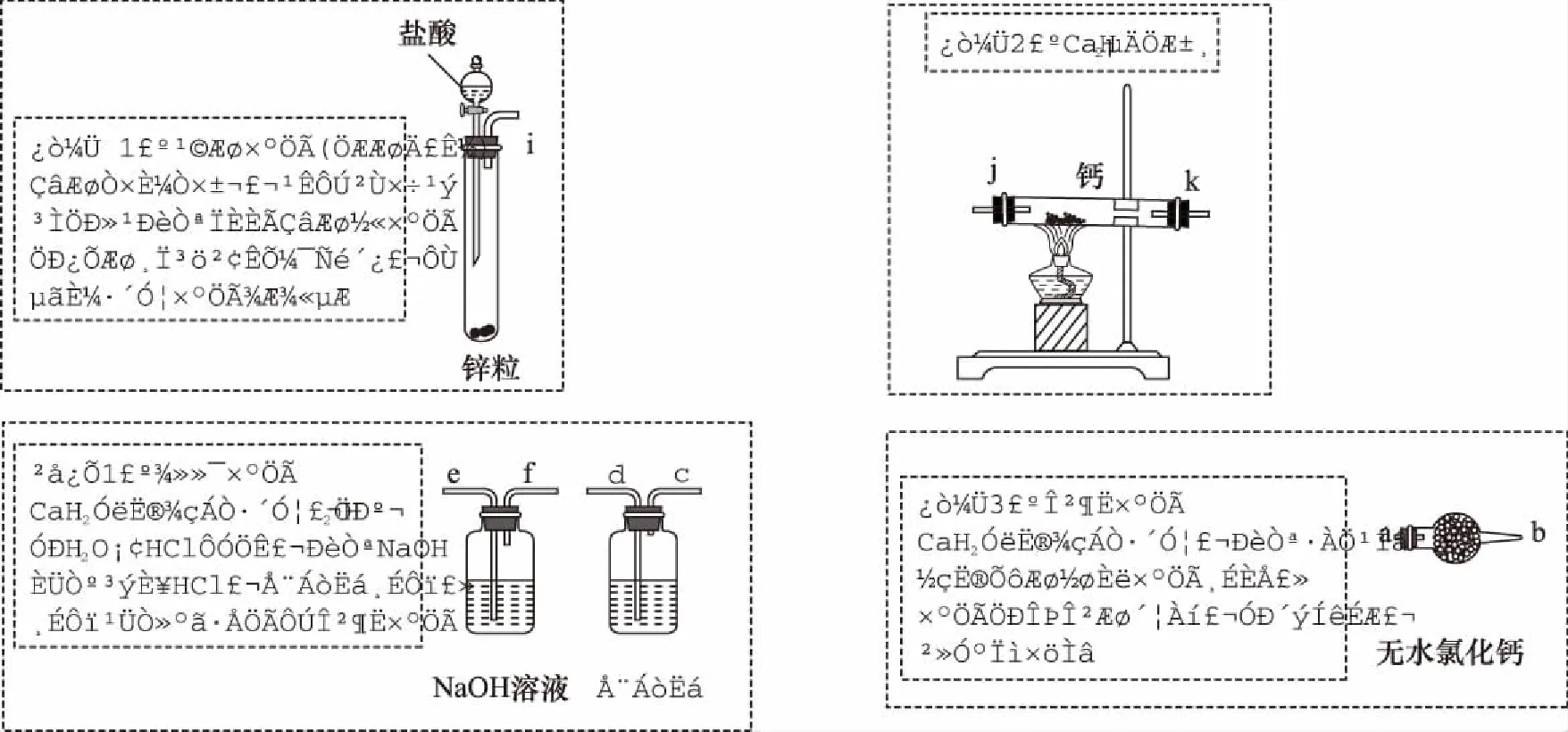
图5 制备CaH2的解题模型
【答案】
(1)i→e,f→d,c→j,k(或k,j)→a
【评价】诚然,装置连接顺序问题,利用插空法便可高效解决。
2.解题小结
(1)加热操作的要求
①使用可燃性气体(如:H2、CO、CH4等),先用原料气赶走系统内的空气,再点燃酒精灯加热,以防止爆炸。
②制备一些易与空气中的成分发生反应的物质(如H2还原CuO的实验),反应结束时,应先熄灭酒精灯,继续通原料气至试管冷却。
(2)尾气处理的方法
有毒气体常采用溶液(或固体)吸收或将之点燃的方法,不能直接排放。
(3)特殊实验装置
①制备在空气中易吸水、潮解以及水解的物质(如Mg3N2、Al2S3、AlCl3等),往往在装置的末端再接一个干燥或液封装置,以防止空气中水蒸气的进入。
②用液体吸收气体,若气体溶解度较大,要加防倒吸装置。
③若制备物易被空气中氧气氧化,应加赶气装置,称为反应前赶气。若是反应后赶气,往往是为了定量测定气体的质量,将残留在装置中的气体赶至吸收装置中吸收。也可能是将有毒气体赶至吸收装置吸收,以便拆卸装置无污染。
④“空瓶子”(空置洗气瓶)装置:可能是防倒吸、收集、气流缓冲、气体混合装置(有时候盛有浓硫酸等溶液)等。
(4)常见信息的处理:(要求相应特殊装置或操作)
①熔沸点:可能考查蒸馏、冷凝等分离操作。
②遇水水解:考查防水操作,一般需要在反应装置前后加防水装置。
③与空气反应:需要赶气,前面已描述。
④受热分解:控制反应速率不能过快、防止加热温度过高(反应温度,蒸发、烘干等温度)。
⑤溶解度与温度关系:涉及分离提纯操作。溶解度随温度变化程度大,一般采用的具体操作为蒸发浓缩、冷却结晶、过滤、洗涤、干燥。
二、实验设计与解题能力相关性的研究
经过插空法对气体参与实验原理的理解,尝试让学生展开结合信息的实验设计训练,并鼓励学生展开实验实践。实验设计习题如下:
例5.完成下列实验的初步设计(有必要请将反应装置图画出)
1.设计实验方案制备氯化铁固体
已知:FeCl3在300℃以上易升华,遇水易水解。
2.设计实验方案制备PCl3
已知:①实验室要用黄磷(即白磷)与干燥的Cl2模拟工业生产制取PCl3;②黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;③PCl3遇水会强烈水解生成H3PO3和HCl;④PCl3遇O2会生成POCl3,POCl3溶于PCl3;⑤PCl3、POCl3的熔沸点见表2:

表2 PCl3、POCl3的熔沸点
3.利用SO2与Na2S、Na2SO3混合溶液反应制备Na2S2O3·5H2O


②Na2S2O3遇酸易分解
经过插空法教学后,笔者在所教两个班级(共90人)中将例5展开测试,大部分学生能较准确的设计出实验方案,实际情况见表3。“准确设计”未经讲解,接着从高考题和模拟题中选择与实验设计对应的3个习题以及2018年全国Ⅰ卷第26题,进行35分钟限时训练(每题15分),训练结果见表4。同时再另外选取成绩相当的90名同学,未经过插空法的学习,展开同类训练。

表3 例题5完成情况(30 min)

表4 大题专题练情况(35 min)
插空法解题的高效性可见一斑,对气体参与制备类实验的设计能力效果明显。尤其是学生面对醋酸亚铬的制备时,通过插空法的学习,也能高效地取得好成绩。未学习插空法的学生表现具有不稳定性。
不难发现学习插空法后,学生做习题情况明显与实验设计表现相似,见表5,反之,呈现相关性不明显。

表5 大题专题练情况与实验设计表现的关系
学生发现实验设计和习题有区别时,纷纷表示想走进实验室展开实验,通过插空法的教学与习题应用,极大地激发了学生敢于实验设计、敢于实践的兴趣和勇气。
同时让学生通过实验设计与化学物质的性质之间的关系,意识到科学探究是具有一定的风险,需要正确的认知和决策。在实验教学中要让学生形成风险意识,要充分考虑可能存在的风险,有处理风险发生的方法和措施,使学生逐步具备能够根据实际不断优化、简化设计方案的能力。
三、插空法的教学意义
插空法可迅速解决有气体参与的制备类实验综合题,通过此法让学生走出“怕实验题”的困境,并为实验设计和其他实验题的思考提供了方向。


