克唑替尼靶向治疗NSCLC的肿瘤学效果研究
庄桂宝,王明元
非小细胞肺癌(NSCLC)是肺癌的主要类型,约占75%~80%。由于NSCLC早期症状不典型,有症状的患者已为晚期肺癌,严重缩短其生存期[1]。相关研究发现,发生棘皮动物微管相关类蛋白4与间变性淋巴瘤激酶(EML-ALK)基因重排的NSCLC患者高达13%,化疗治疗该病已没有显著效果,因此,有效筛选ALK融合基因阳性表达,对患者进行必要的靶向治疗是治疗的关键[2]。克唑替尼作为中国唯一上市的EML-ALK双靶点口服抑制剂,常用于EML4-ALK、ROS1融合基因阳性表达的晚期 NSCLC治疗[3-4]。本研究探讨了克唑替尼靶向治疗晚期NSCLC患者的肿瘤学效果和对血清肿瘤标志物、EML-ALK阳性表达水平及患者预后的影响,旨在为晚期NSCLC患者的综合治疗提供参考。
1 资料与方法
1.1 病例资料 收集本院肿瘤内科2014年2月~2017年2月收治的60例NSCLC患者。入组标准:经细胞学、组织学检验确诊为NSCLC,经CT或MRI显示有可测量病灶;经荧光原位杂交(FISH)检测确诊为棘皮动物微管相关类蛋白4与EML-ALK的融合基因阳性;卡氏体能状态(KPS)评分≥70分;预计生存期≥3个;符合赫尔辛基关于受试者基本原则。排除标准:有其他抗癌药物治疗史;伴有其他恶性肿瘤;合并脑、肝、肾等严重器质性疾病;存在神经系统转移;伴有严重的基础性疾病如高血压、糖尿病等;对2周期化疗耐受性差者。依照密封信封法,将入组患者随机以1∶1比例均分为常规化疗组与克唑替尼组,各30例,两组基线资料比较无显著差异(P>0.05),具有可比性。
1.2 治疗方法 化疗前30 min,静脉滴注阿扎司琼5 mg,预防化疗的胃肠道反应。常规化疗组行吉西他滨(GEM)+卡铂(CBP)方案化疗,于治疗第1 d及8 d,静脉滴注GEM 100 mg/m2+生理盐水100 ml,在50 min内滴注完毕。同时,给予CBP按血药浓度-时间曲线下面积=5,max=800 mg,加入生理盐水250 ml,静脉滴注 30~60 min,于治疗第 1 d 开始,连续治疗3 d。克唑替尼组在常规化疗组治疗基础上,给予克唑替尼(德国 Pfizer Inc.,注册证号:H20130079),250 mg/次,口服,2次/d,连续服用。两组化疗均28 d 1个疗程,共化疗4个疗程,治疗期间定期检查患者肝肾功能、血常规、心电图及CT,并进行1年随访。
1.3 观察指标 (1)肿瘤学疗效:治疗4个疗程后,依照实体瘤疗效评价标准(RECIST)1.0标准评定肿瘤学疗效,分为完全缓解(CR)(肿瘤组织体积减少率≥30%)、部分缓解 (PR)(病灶体积减少率<30%)、稳定(SD)(病灶体积增加率<20%)和疾病进展(PD)(病灶体积增加率≥20%)共4个维度,客观缓解率(ORR)=(CR+PR)例数/总例数×100%。(2)肿瘤标志物:于治疗前及治疗4个疗程后,采集患者清晨空腹静脉血3 ml,采用电化学发光法检测血清癌胚抗原(CEA)、细胞角蛋白19片断21-1(CYFRA21-1)、神经特异性烯醇酶(NSE)和癌胚抗原125(CA125)水平。(3)EML4-ALK阳性表达:治疗4个疗程后,采用FISH检测患者ALK融合基因是否发生重排,计数100个细胞,其中异常细胞超过20%为阳性,统计两组EML4-ALK融合基因阳性表达病例。(4)不良反应:采用美国国家癌症研究所(NCI)关于癌症常见不良反应标准(CT-CAE0)4.0版评估患者的不良反应。(5)随访:患者治疗出院均采用上门或电话随访,均获得有效随访,无一例脱组,随访时间为截止时间2018年6月。于治疗前和疾病进展或未进展的末次随访时间,依照WHO关于KPS评分标准评估患者生存质量,计算KPS评分增长值(治疗后KPS评分-治疗前KPS评分),分为提高(KPS评分增长值≥10分)、稳定(KPS评分增长值在 1~10分)及下降(其数值为-10~0 分)3 个维度,KPS 稳定率=(稳定+提高)例数/总例数×100%,统计两组1年随访期间患者的生存情况。
1.4 统计学方法 应用SPSS 19.0统计软件分析,计量资料以±s表示,组间比较采用t检验;计数资料以[n(%)]表示,采用χ2检验;等级资料采用秩和检验,P<0.05为差异有统计学意义。

表1 两组基线资料比较(n=30)
2 结果
2.1 对实体瘤疗效 克唑替尼组ORR显著高于常规化疗组(P<0.05,表2)。
2.2 血清肿瘤标志物水平比较 治疗后,两组血清 CEA、CYFRA21-1、NSE及 CA125水平显著降低(P<0.05),且克唑替尼组低于常规化疗组(P<0.05)。见表3。
2.3 EML4-ALK阳性表达率和不良反应比较 克唑替尼组治疗后的EML4-ALK阳性表达率显著低于常规化疗组(P<0.05);两组不良反应发生率比较无统计学差异(P>0.05,表4)。
2.4 KPS生存质量和1年生存率比较 到末次随访时,克唑替尼组KPS生存质量稳定率和1年生存率均显著高于常规化疗组(P<0.05,表5)。
3 讨论
EML4-ALK属于治疗NSCLC的新型分子靶向治疗靶点,EMIA-ALK融合基因发生主要与第2号染色体短臂插入引起有关,一旦EMIA与ALK分子激酶功能区对接成功,经ALK激酶磷酸化,有效发挥转录调节功能,激活下游靶基因表达,从而诱导细胞恶性转变[5]。克唑替尼可通过特异性靶向抑制EML4-ALK,阻断c-MET和R0S1等通路来改变基因转录水平,并刺激细胞凋亡蛋白分子BAX以及BCL-2的表达,进而调控肺癌病灶组织肿瘤细胞增殖、分化和迁移,影响肿瘤细胞G1/S期过渡,纠正细胞增殖周期异常,从而达到促进NSCLC细胞凋亡的目的[5-6]。本研究结果显示,将克唑替尼组的ORR可达86.67%,显著高于常规化疗组的63.33%,表明克唑替尼可提高治疗NSCLC的效果,高于赵静等[1]报道的64.29%,与郑明英等[7]报道的91.67%相似。

表2 两组实体瘤疗效比较[n(%)]

表3 两组治疗前后血清肿瘤标志物水平比较(n=30)
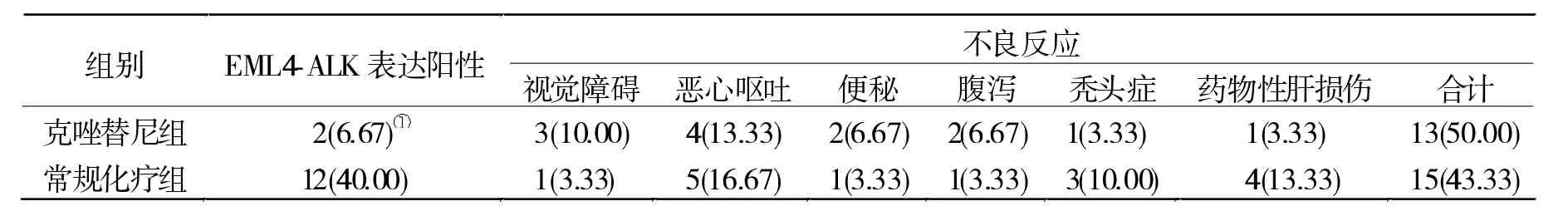
表4 两组治疗后EML4-ALK阳性表达率和不良反应比较[n(%)]
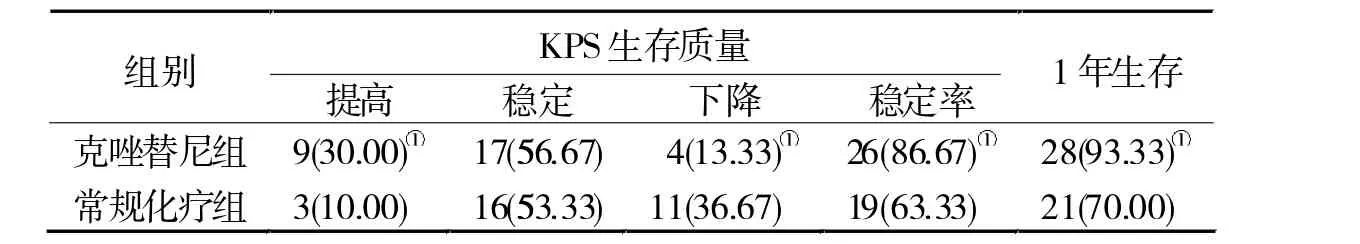
表5 两组KPS生存质量和1年生存率比较[n(%)]
CEA、NSE在肿瘤组织及胚胎组织中呈高水平表达,是预测NSCLC患者肿瘤复发及预后和评判EML4-ALK靶向治疗疗效的有效指标,CYFRA21-1、CA125作为NSCLC特异性肿瘤标志物,与肿瘤增殖活性、肿瘤负荷呈正相关[2,7]。本研究结果显示,治疗后, 克唑替尼组血清 CEA、CYFRA21-1、NSE及CA125水平明显低于常规化疗组,说明克唑替尼可靶向下调晚期NSCLC的血清肿瘤标志物水平。此外,克唑替尼组治疗后的EML4-ALK阳性表达率显著降低,提示克唑替尼靶向治疗可有效减少ML4-ALK阳性表达,与乌日罕等[8]报道相似。
本研究两组不良反应发生率比较无显著差异,说明克唑替尼靶向治疗安全性良好。两组经1年有效随访发现,克唑替尼组末次随访时的KPS生存质量稳定率和1年生存率均显著高于常规化疗组,进一步证实克唑替尼靶向治疗可提高NSCLC患者生活质量,延长其生存期,利于其预后。
综上所述,克唑替尼靶向治疗晚期NSCLC疗效确切,可抑制血清肿瘤标志物表达,降低EML4-ALK阳性表达,提高患者生存质量,利于患者生存期延长及预后。

