CT引导多靶点经皮椎体成形术治疗椎体转移瘤疼痛探讨*
付 敏 钟 琼 陈新荣 杨 俊 魏 俊
(1赣南医学院第一附属医院疼痛科,赣州 341000; 2赣南医学院疼痛医学研究所,赣州 341000)
恶性肿瘤易发生骨转移,脊柱为好发部位,约有20% 恶性肿瘤病人发生椎体转移[1]。椎体转移瘤病理表现以溶骨性破坏为主,易诱发顽固性疼痛及脊椎不稳,严重者甚至可引起截瘫。椎体转移瘤治疗方法较多,但镇痛药物及放化疗对疼痛缓解效果及脊柱稳定性干预的疗效不佳[2,3]。1987年,国外Galibert[4]率先报道了经皮穿刺注射骨水泥治疗颈椎血管瘤获成功,其后经皮椎体成形术 (percutaneous vertebroplasty, PVP) 逐步应用于治疗脊柱溶骨性肿瘤,认为具有镇痛效果好、增加脊椎强度和稳定性、预防病椎塌陷、改善病人活动状况、杀灭局部肿瘤细胞等作用[5,6],得到广泛的认可。尽管PVP在治疗椎体转移瘤疼痛方面取得了较为乐观的成果,但对于溶骨性破坏范围广、椎体后缘、附件破环严重病例,如何精准骨水泥填充、减少骨水泥渗漏导致不良后果等仍是目前面临的问题,尤其椎管内渗漏严重的将造成脊髓压迫等灾难性后果,影响该技术临床推广。本研究拟运用CT引导下图像分析,精准设计手术入路,多靶点将骨水泥注入到椎体肿瘤破坏灶内以期更好解决以上问题,同时观察疗效及安全性,现报道如下。
方 法
1.一般资料
本组132例病人,男62例,女70例。年龄34~86岁,平均64.4±5.6岁。共累及160个椎体,其中颈椎4个,胸椎81个,腰椎70个,骶椎5个。原发灶:肺癌46例,乳腺癌39例,肾癌7例,胰腺癌5例,肝癌3例,结肠癌12例,胃癌7例,前列腺癌11例,卵巢癌2例。
纳入标准:①临床诊断肿瘤伴椎体转移病人,影像为溶骨性或混合性破坏表现;②无脊髓及神经根受压症状;③椎体转移瘤病灶为病人主要疼痛部位,与疼痛相关涉病椎体≤3个;④预期生存时间> 3个月。
排除标准:①无法耐受局麻药物或手术病人;②凝血功能障碍病人;③不能完成随访;④有脊髓及神经根受压症状;⑤合并无法进行知情同意的精神疾病;⑥伴发其他导致生存期缩短、慢性疼痛的严重疾病;⑦恶液质,器官功能失代偿
术前均经X线片、CT或MRI检查,确定病人受累椎体的部位及数量、椎体塌陷程度、溶骨破坏程度、椎体后壁的完整性、椎弓根侵犯程度、脊髓受压情况,并常规检查心肺功能、血糖、 凝血功能、肝肾功能检查,本组手术均在介入室于CT引导下进行。
2.手术方法
多靶点手术方案制订原则:①常规双侧入路(见图1),如转移肿瘤病灶较局限,椎体边缘破坏不严重,单侧穿刺即可覆盖目标病灶,则考虑单侧入路(见图2);②依据椎体转移肿瘤灶个数、部位、范围设计穿刺入路,以骨水泥注射能尽可能完善填充病灶为首选(见图1A-E);③如椎体后缘等边缘破坏严重,可考虑一侧穿刺靶点相对靠近边缘破口,另一侧穿刺靶点在主要病灶区域(见图3A),可先在近破口处在CT扫描严密监视下少量、多次、多点注射骨水泥,待骨水泥凝固加固破口后再注射另一侧(见3B-D);④如有椎弓根破坏,同侧穿刺针必经椎弓根入路(见图1E),在椎体病灶区注射骨水泥后,逐步退针到椎弓根位置,分次、多点、少量推注骨水泥于椎弓根病灶处(见图1H, L);⑤骨水泥调配时,配制不同浓度,延长骨水泥可注射时间;⑥每次推注骨水泥量在1~2 ml左右,注意病人不适情况,每次推注后CT快速扫描明确骨水泥在病灶内分布情况,依据填充情况多次、多点注射骨水泥(见图1F-L)。
颈椎:病人取仰卧位,肩下垫枕,两肩尽量下移,头部后仰,CT扫描定位病变椎体,根据选定椎体平面的标记,在气管旁确定穿刺点,常规消毒铺巾,1%利多卡因局麻后,用中指和食指分离气管与颈动脉间隙按压至椎体前缘,将穿刺针穿刺入病变椎体,反复CT扫描,确认穿刺针尖达病椎转移肿瘤病灶处(见图4A-C),CT监视下少量、多次注射骨水泥(见图4D)。
胸、腰、骶椎: 取俯卧位,一般采用椎弓根入路,CT扫描定位后,确定穿刺点位置、穿刺角度、深度。常规消毒铺巾,1%利多卡因局麻,在CT引导下,穿刺针经椎弓根入路穿刺达椎体靶点处,CT监视下少量、多次、多点注射骨水泥。
骨水泥调制、注射:依据溶解液多少配制不同骨水泥浓度,准备多根1.0 ml注射器,待骨水泥在不同稀、稠度时,分别用多支1.0 ml注射器抽取,按照骨水泥浓度由稀到稠顺序排列,经穿刺针缓慢注入1~2 ml左右骨水泥,同时询问病人四肢感觉、肌力变化,及时观察病人是否有异常情况,即刻CT扫描观察骨水泥在病灶内的分布、有无外渗等,如无异常,根据需要分别再次CT监视下多次、多点注入骨水泥。注入完毕后,待骨水泥凝固后,旋转穿刺针后并拔出,局部敷料覆盖,返回病房,平卧2小时后如无异常可下床活动。
根据椎体肿瘤破坏灶容积的不同,注入骨水泥的量有所不同,一般不外漏前提下病灶内尽量多注射骨水泥为原则,推注时应缓慢保持一定压力,不应采取冲击式推注,防止从椎体边缘溢出,或突破骨质破坏部位进入椎管内形成脊髓或神经根压迫。
3.观察指标
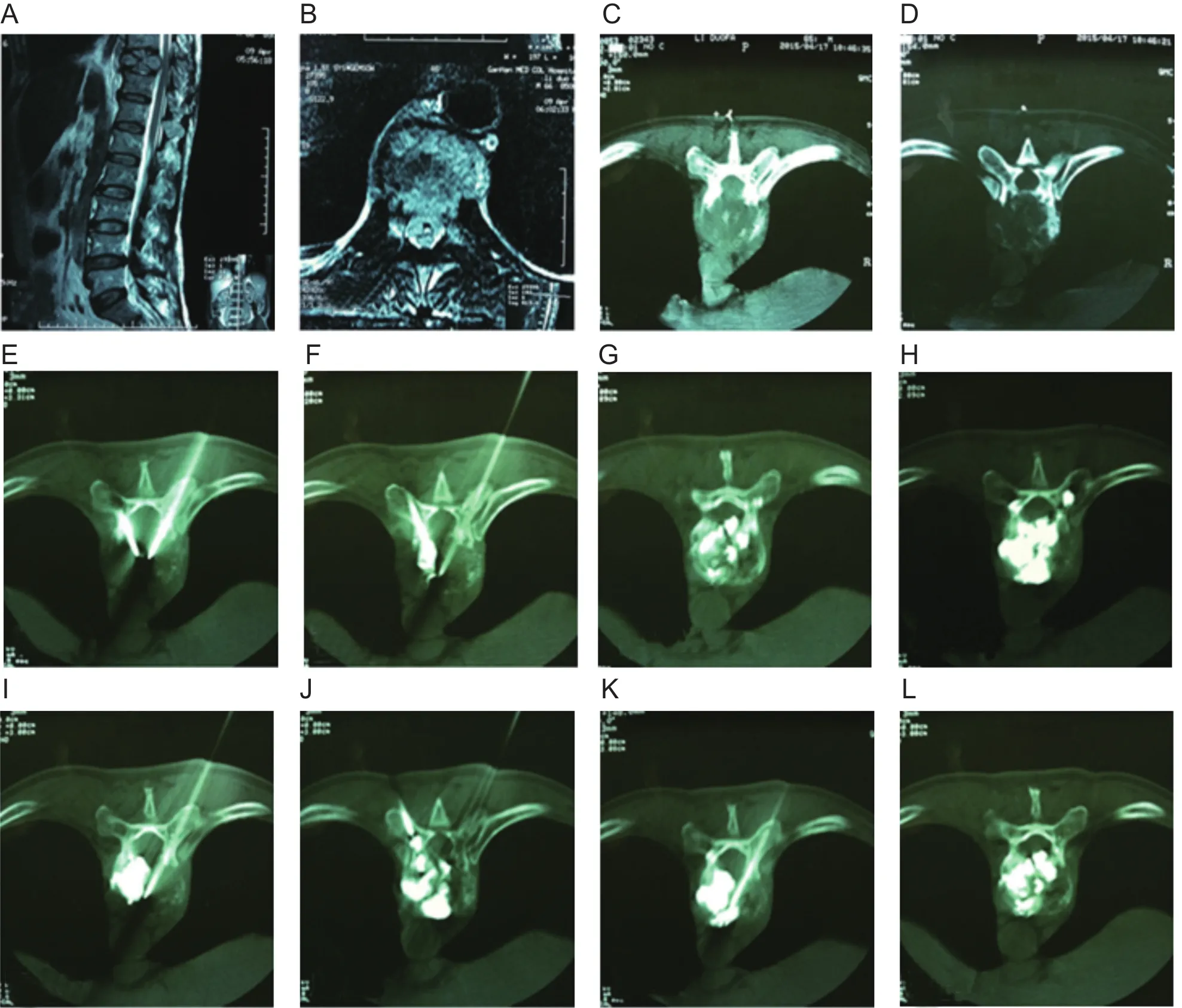
图1 (A) MRI矢状位示T10 椎体破坏;(B) MRI轴位示T10椎体及双侧椎弓根破坏,部分肿瘤组织破坏椎体后缘进入椎管;(C, D) CT示T10椎体、双侧椎弓根及椎体后缘破坏严重;(E) 选择双侧椎弓根入路;(F-H) CT监视下左侧注射骨水泥,每次推注骨水泥量在1~2 ml左右,注意病人不适情况,每次推注后CT快速扫描明确骨水泥在病灶内分布情况,依据填充情况多次、多点注射骨水泥;(I-L) 左侧骨水泥凝固后,CT扫描严密监视下右侧少量、多次、多点注射骨水泥;(H, L) 在椎体病灶区注射骨水泥后,逐步退针到椎弓根位置,分次、多点、少量推注骨水泥于椎弓根病灶处Fig.1 (A) Ruined T10 vertebrae in MRI sagittal view; (B) Ruined bilateral vertebral pedicle and T10 vertebrae in MRI axial view;some tumor tissues in spinal canal; (C, D) Seriously ruined T10 vertebrae, bilateral vertebral pedicle, posterior vertebral edge in CT view; (F-H) Injection of bone cement under CT guidance; Observing distribution of bone cement in vertebrae after each operation; Multipoint and repeated injection according to distribution of bone cement; (I-L) Multipoint and repeated injection of bone cement in right vertebrae, after bone cement freezing under CT guidance; (H, L) Separate multipoint injecting a little bone cement in ruined vertebral pedicle when puncture needle backing to vertebral pedicle gradually after injecting bone cement in vertebral disease focus.
记录术中推注骨水泥总量(ml)。分别观察术前与术后1周、1个月、3个月疼痛视觉模拟评分法(VAS):镇痛药使用评分(AUS)[7],0:不使用镇痛药物;l:使用非甾体消炎药;2:不定时口服麻醉类镇痛药;3:定时口服麻醉类镇痛药;4:静脉或肌肉注射麻醉类镇痛药;生活质量评分(QLS)[8]:由食欲、面部表情、睡眠、精神、疼痛、治疗不良反应等12项指标体现,每项指标计1~5分,总分为60分。记录相关并发症。
4.统计学分析
实验数据采用SPSS 18.0软件处理和分析,计量资料以均数±标准差(±SD)表示,采用重复测量方差分析进行统计学分析,P< 0.05认为差异有统计学意义。
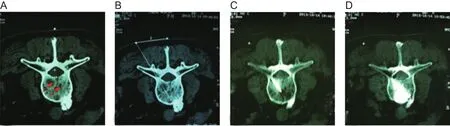
图2 (A) 红色箭头示椎体主要破坏病灶;(B) 术中CT扫描确定穿刺路线;(C) 术中CT扫描确定穿刺针在破坏病灶处;(D) 术中示骨水泥在椎体内弥散分布情况Fig.2 (A) Red arrows show the main ruined vertebral disease focus; (B) Determining puncture approach in operation under CT guidance; (C) Puncture needle in the disease focus under CT guidance; (D) Distribution of bone cement in vertebrae in operation.
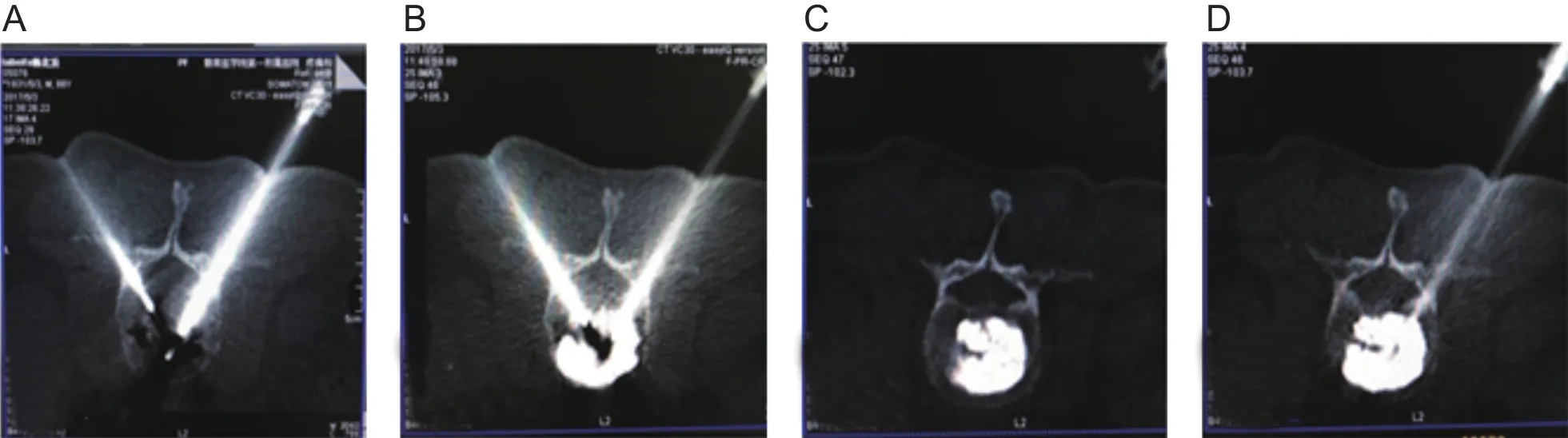
图3 (A)椎体后缘破坏严重,左侧穿刺靶点相对靠近椎体后缘破口,另一侧穿刺靶点在主要病灶区域;(B-D) 在CT扫描严密监视下于左侧近破口处少量、多次、多点注射骨水泥,待骨水泥凝固加固破口后再注射另一侧Fig.3 (A) Left puncture needle closing to rupture of vertebral posterior edge; Right needle in the main ruined disease focus; (B-D)Multipoint and repeated injection of bone cement in left vertebral rupture, after bone cement freezing under CT guidance.

图4 (A) 颈5椎体转移肿瘤行椎体成形术;(B, C) 颈5椎体穿刺到位;(D) 颈5椎体注射骨水泥后Fig.4 (A) PVP in C5 veterbral metastasic tumors; (B, C) Needle in exact place in C5; (D) Bone cement injection in C5 vertebrae.
结 果
132例病人在CT引导下均顺利完成手术,骨水泥充填到位。颈、胸、腰、骶椎体骨水泥平均注射量分别是 0.8±0.1 ml、2.2±1.4 ml、3.4±1.3 ml、4.2±1.7 ml(见图5)。术中出现17例(10.6%)骨水泥渗漏,其中椎管内渗漏4例、椎间盘内渗漏7例、椎旁渗漏6例,所有渗漏病例均未出现神经损伤症状。所有病人均完成3个月随访。术后1周、1月、3月VAS、AUS及QLS均较术前有显著性差异 (P< 0.01,见图6、7)。术后3月VAS、AUS及QLS较1月有病情加重趋势,但无统计学差异。
讨 论
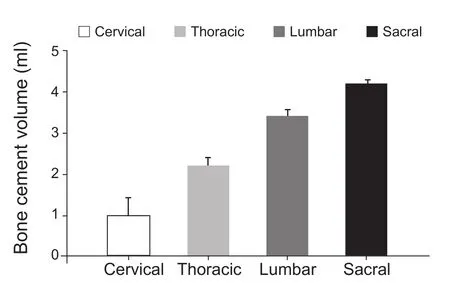
图5 椎体骨水泥推注量Fig.5 Bone cement injection volume in vertebrae

图6 VAS与AUS评分**P < 0.01,与术前相比较Fig.6 VAS and AUS score**P < 0.01, compared with pre-operation.

图7 生活质量评分(QLS)**P < 0.01 ,与术前比较Fig.7 Quality of Life scale**P < 0.01, compared with pre-operation.
脊柱椎体松质骨血供丰富,血流缓慢,转移瘤易累及椎体,且病理表现以溶骨性破坏为主,易引起脊椎剧烈疼痛和脊椎稳定性减弱。应用镇痛药物治疗脊椎转移瘤疼痛疗效往往欠佳,约有45%的脊柱转移瘤未获得满意的镇痛疗效[9]。癌痛流行病学调查显示[10],约1/3病人以1个部位疼痛为主,1/3以2个部位疼痛为主,另1/3病人以3个或3个以上部位疼痛为主。临床上椎体转移肿瘤由于骨破坏、继发性骨折、周围丰富的神经组织所受刺激等常为病人主要疼痛部位,如何有效处理症状相关的椎体转移病灶对病人疼痛控制、生活质量改善有重要意义。
PVP可应用于镇痛药物疼痛控制不佳的脊柱转移瘤病人,有即刻的疼痛缓解、稳定椎体结构及破坏局部肿瘤组织的作用。PVP治疗椎体转移性肿瘤的优势:①骨水泥凝聚过程产生的热量可以破坏病灶内的神经末梢,疼痛缓解或消失;②骨水泥凝固后通过增强骨骼刚性强度,增加脊柱稳定性;③骨水泥凝固时产生高热和局部压力,造成部分肿瘤细胞缺血坏死;④骨水泥自身的化学毒性也会产生一定的灭活肿瘤作用[11]。⑤无开放手术的较大创伤、无镇痛药物的不良反应。⑥病人疼痛减轻后,为进行下一步其他治疗创造了更好的条件。
本研究结果显示,术后1周、1个月及3个月的VAS、AUS均较术前明显下降,表明该微创技术具有良好的镇痛效果,同时可显著地减少镇痛药的使用量。QLS较术前明显提高,术后病人生活质量改善具有显著性差异。VAS及镇痛药物评分在术后3个月较术后1周、1个月都稍有增高,而生活质量评分稍有下降,但无统计学差异,分析原因可能:①病人体内肿瘤病灶进一步扩散、发展,产生新的癌性疼痛;②疼痛药物的耐受性发生变化;③病人的身体消耗状况继续恶化。
PVP手术最常见并发症是骨水泥渗漏造成的相关损伤,Prie[12]报道PVP术后渗漏的生率较高,达65%左右,但大多数为少量渗漏,未引起临床症状。Burton[13]报道渗漏至椎管内及椎间孔处而造成神经损伤的并发症发生率为5.8%。本组研究有17例病人(10.63%)术中出现骨水泥渗漏并发症,没有明显神经损伤症状,故未做特殊处理。比较上述的报道,采用多靶点方式的并发症明显减少,这种处理方式的优势在于[14]:①术前CT扫描椎体病变区以明确骨质破坏范围及病灶数量部位,设计穿刺入路(见图1C-E、图2A-B、图3A)。②必要时可双通道甚至多通道穿刺针注射(见图1E、图3A),先靠近破损处注射少量骨水泥,以便填充骨皮质破损处,待该处骨水泥硬化堵塞后,再经另通道,行病灶内注射骨水泥(见图1I-L、见图3B-D),减少外渗风险。
相对于骨质疏松性椎体病变,椎体转移瘤病灶有其特殊性,主要表现为:①椎体内常合并多个病灶区,且病灶区分布广;②椎体内常破坏严重,这就需要骨水泥尽量填充覆盖;③常有严重的椎体边缘破坏,尤其椎体后缘,易导致骨水泥椎管内渗漏,严重者致脊髓、神经压迫;④双侧的椎弓根病变需兼顾椎体和椎弓根骨水泥的填充。针对上述转移瘤病灶的特殊性,为了获得对病灶最大化处理,减少并发症,扩大手术适应范围,本研究依托CT引导能个体化设计手术入路及即时观察的优势,根据病人病灶变化特点提出了多靶点概念,即术前CT扫描病灶确定多个穿刺目标点,达到多个骨水泥填充目标。与C臂机引导PVP相比,CT引导PVP具有以下优势:①术中能观察到转移病灶大小、部位、数量,根据病灶个体化选择穿刺入路、穿刺点位置、角度(见图1E、图2A-B、图3A);②术中具有穿刺定位精确优势,在CT引导下可以更加精准明确穿刺针位置是否正确,是否到达靶点病灶部位(见图1A-D、图4A-C);③术中可以即刻观察到骨水泥的弥散和渗漏情况[15](见图1F-L、图2C、图3B-D、图4D)。
CT引导多靶点PVP手术适应证: ①椎体后缘及边缘破坏严重,可考虑一侧穿刺靶点相对靠近破口缘,另一侧穿刺靶点在主要病灶区域(见图3-1A),可先在近破口处在CT扫描严密监视下少量、多次、多点注射骨水泥,待骨水泥凝固加固破口后再注射另一侧(见图1F-L、图3 B-D);②针对椎弓根破坏,同侧穿刺针必经椎弓根入路(见图1F),在椎体病灶区注射骨水泥后,逐步退针到椎弓根位置,分次、多点、少量推注骨水泥于椎弓根病灶处(见图1H、L)。
骨水泥的调配及注射量:①骨水泥调配时,按照浓度由稀到稠准备若干个1.0 ml骨水泥注射器,方便术中调整骨水泥注射部位和注射量;②适当控制骨水泥注射量。本研究结果显示,骨水泥平均注射量最大值为4.2±1.7 ml,明显低于纪经涛[2]等骨水泥平均灌注量5.83±1.11 ml,这符合我们提倡CT引导下精准注射、适量注射理念。
CT引导多靶点经皮椎体成形术确实能有效地减轻病人的疼痛,但该技术仍存在不确定风险:①Dean[16]指出,肿瘤组织破坏椎体内松质骨,病灶内的骨水泥灌注,存在挤压肿瘤组织向周围加速扩散可能;②溶骨性肿瘤破坏椎体后壁甚至侵入椎管,骨水泥注射时有导致肿块移位或加重压迫的危险性。
研究结果表明,CT引导下多靶点PVP对于缓解或消除由椎体转移性肿瘤引起的疼痛有明显的治疗效果、创伤小、并发症少,还能减少镇痛药物使用量及改善生活质量。

