腹腔镜下内外括约肌间切除术治疗低位直肠癌的效果观察
王 昆 雷云安 周延河
(河南省邓州市中心医院普外科,邓州市 474150)
直肠癌是指从齿状线到直肠乙状结肠交界处之间的肿瘤,也是消化道最常见的恶性肿瘤之一[1]。内外括约肌间切除术(ISR)是超低位直肠癌保肛手术的极端形式[2],手术要求切除部分或者全部内括约肌以达到肿瘤根治性的要求。保留肛门功能的同时,ISR局部复发率较低,5年生存率可高达70%[3-4]。本研究回顾性分析在我院确诊为低位直肠癌并行ISR手术的患者资料。现报告如下。
1 资料与方法
1.1 一般资料 分析我院2016年1月至2017年4月确诊为低位直肠癌且行ISR手术的160例患者的临床资料,其中行腹腔镜ISR手术的80例患者为观察组,行开腹ISR手术的80例患者为对照组。观察组男37例,女43例,年龄(57.47±11.77)岁;肿瘤距肛缘距离(3.25±0.46)cm;既往腹部手术史4例;接受新辅助治疗22例;临床分期:T1期10例,T2期51例,T3期19例。对照组男35例,女45例,年龄(54.00±12.75)岁;肿瘤距肛缘距离(3.14±0.38)cm;既往腹部手术史8例;接受新辅助治疗15例;临床分期:T1期12例,T2期52例,T3期16例。纳入标准:①病理诊断为直肠癌,临床TNM分期为T1~T2期;②肿瘤下缘距离肛缘<5 cm;③病理证实远端切缘以及环周切缘均呈阴性;④术前肛门排便功能正常。排除标准:①穿孔、出血或肠梗阻;②术前证实癌症复发者;③结直肠合并两处以上肿瘤;④肿瘤组织侵犯至外括约肌或肛提肌。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2 手术方法
1.2.1 观察组 所有患者均行全身麻醉,手术依据全直肠系膜切除术(TME)的原则和无瘤原则。取头低右侧高膀胱截石位,在腹腔镜监视器观察下,避开腹壁下动脉,置入5 mm trocar,切开乙状结肠系膜中线侧,肠钳抓紧直肠向腹侧提拉,张紧乙状结肠系膜,以骶岬为入刀点,以“黄白交界线”为指引,从尾侧向头侧切开乙状结肠系膜,进入左结肠系膜和肾前筋膜之间的融合筋膜间隙。在此间隙内,向左侧扩展外科平面,达到乙状结肠系膜消失的Toldts线。注意保持左半结肠系膜及肾前筋膜的完整性,并在主髂血管前保留一层透明的肾前筋膜,透过此筋膜可见乙状结肠系膜根部后外侧的左输尿管和生殖血管,分离范围从中央向左达生殖血管外侧左结肠旁沟,自尾侧向头侧达肠系膜下动脉根部。在其包绕该动脉远心端骨骼化,并分离肠系膜下动脉2 cm,清扫周围脂肪组织和淋巴结,保留左结肠动脉。从骶岬水平开始,在直肠上段系膜后方的疏松结缔组织间隙,向前侧、后侧、外侧锐性扩展外科平面至直肠后间隙,沿着后壁到侧壁顺序在括约肌间隙进行剥离,打通腹腔内游离面,最后再剥离前壁。将直肠及其系膜从肛门内脱出,确认上切缘的位置后切除直肠标本。将脱出的结肠与肛门行结肠-肛门吻合(间断缝合),吻合完毕后需反复确认吻合口的血供是否存在问题,必要时需要行预防性末端回肠造口术。
1.2.2 对照组 接受开腹直肠癌IRS术,于下腹正中处切开,先行腹腔探查,熟悉腹腔和盆腔的状况,了解肿瘤是否发生转移,且明确腹腔和盆腔淋巴结情况。将直肠和乙状结肠的左侧系膜进行彻底分离,然后再将其右侧肠系膜进行分离,于腹膜返折部位集结。将盆底腹膜打开,于骶前间隙处将游离的直肠后壁逐步分离,且尽量向尾侧部位进行,分离内括约肌和耻骨部位的直肠肌,扩大括约肌之间的平面。结扎肠系膜下方血管的根部、分离直肠前壁和侧壁、游离直肠末端,手术步骤与腹腔镜下手术步骤相同。通过腹部切口将直肠取出,最后进行结肠与肛管吻合。
1.3 观察指标 ①手术相关指标:手术时间、术中出血量、术后肛门排气时间、住院时间、死亡率、并发症。②肿瘤相关指标:淋巴结清扫数量、肿瘤远端切缘以及环周切缘病理结果、肿瘤恶性度、TNM临床分期。③患者术后肛门功能,采用kirwan分级评估:分为Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ级。④复发、远处转移、生存情况指标。
1.4 统计学分析 应用SPSS 20.0统计学软件进行数据处理。计量资料用均数±标准差(x±s)表示,组间比较采用t检验;计数资料用百分率(%)表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结 果
2.1 手术指标比较 两组手术时间比较,差异无统计学意义(P>0.05)。观察组术中出血量、术后肛门排气时间、恢复正常饮食时间及住院时间均少于对照组,差异均有统计学意义(P<0.05)。见表1。

表1 两组患者手术相关指标比较 (x±s)
2.2 病理结果比较 两组淋巴结清扫数量、组织分化程度及TNM分期比较,差异无统计学意义(P>0.05)。见表2。
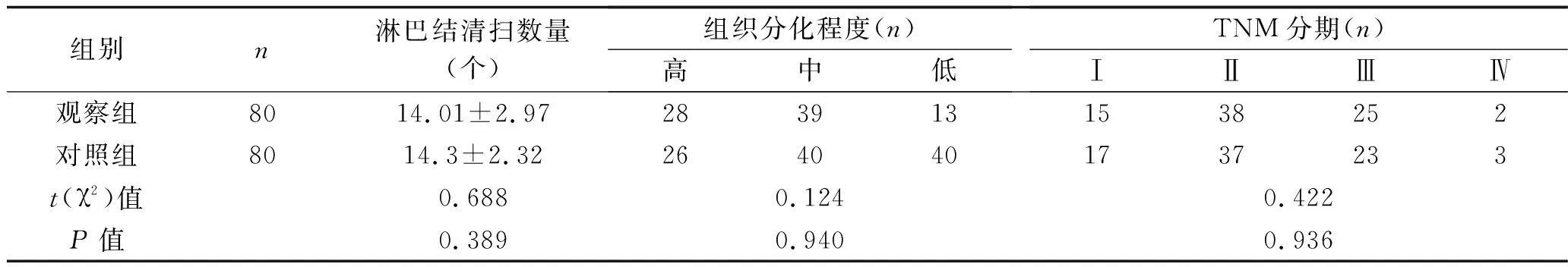
表2 两组患者淋巴结清扫数量与病理结果比较
2.3 肛门功能比较 两组均未出现肛门完全失禁患者。用Kirwan分级评估,观察组Ⅰ级52例,Ⅱ级20例,Ⅲ级8例;对照组Ⅰ级49例,Ⅱ级19例,Ⅲ级12例。两组术后肛门功能Kirwan分级比较,差异无统计学意义(u=0.324,P=0.850)。
2.4 并发症情况比较 观察组发生吻合口瘘4例、直肠阴道瘘1例、盆腔脓肿1例、出血1例、尿潴留1例、深静脉血栓1例、肛门疼痛4例,并发症发生率为16.25%(13/80);对照组发生吻合口瘘4例、直肠阴道瘘4例、盆腔脓肿3例、肠梗阻3例、出血3例、尿潴留1例、深静脉血栓1例、肛门疼痛5例,并发症发生率为30.00%(24/80)。两组并发症发生率比较,差异有统计学意义(χ2=6.737,P=0.009)。
2.5 远期结果比较 两组5年局部复发率、5年远处转移率、5年总生存率比较,差异均无统计学意义(P>0.05)。见表3。
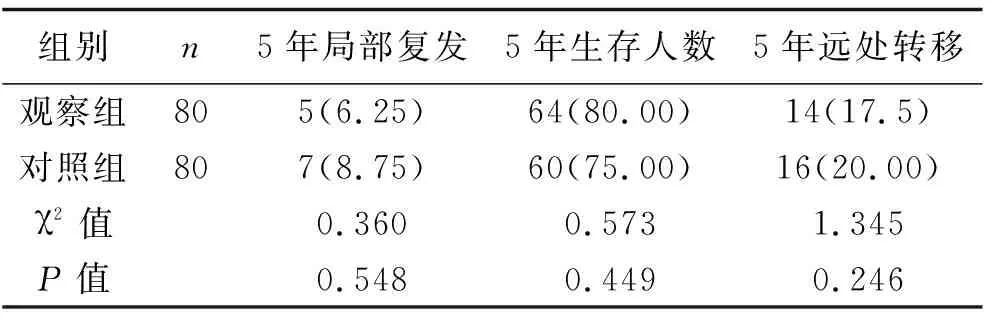
表3 两组患者远期结果比较 [n(%)]
3 讨 论
随着科技水平的进步,医学水平也在不断地发展,对于极限保留肛门在直肠癌手术的应用更为普遍[5]。腹腔镜下内外括约肌间切除术不仅达到了肿瘤根治的效果,而且达到了保留肛门功能的目的。本次对80例行腹腔镜ISR术治疗的低位直肠癌患者进行观察,其腹腔镜ISR手术病理结局与开腹ISR术无统计学差异。由于腹腔镜ISR手术具有出血量更少、术后恢复更快、手术并发症发生率更低等优势,并且两组随访结果显示,5年局部复发率及5年总生存率比较也无统计学差异。
ISR已经渐渐成为低位直肠癌极限保肛的标准术式[6]。以前,ISR术是否会增加癌症的复发率不是十分清楚,而近些年的报道显示,直肠癌患者行ISR术能够得到满意的癌症治疗效果[7]。
手术时间会影响患者的术后恢复,且手术时间越长患者术后并发症发生率就越高[8-10]。研究显示[11],腹腔镜与开腹手术时间的对比存在较大差异,这与外科医生手术熟练程度以及患者的病情关系密切。腹腔镜下行ISR术的另一显著优势是术后肠道功能恢复更快、并发症更少、住院时间更短[12]。因为腹腔镜手术的创伤相对于开腹手术较小,术中对腹腔内脏器刺激更少,也能够很好地保留重要的自主神经[13]。
治疗直肠癌关键是要彻底切除肿瘤[14],并且要提高患者的生活质量。全面探讨ISR术对肛门功能以及生活质量的影响,才能反映患者术后整体的恢复状况,但是各种相关指标尚没有统一标准,目前的评价标准也仅仅是评价肛门功能或生活质量方面。低位直肠癌患者行ISR术,大多数会出现不同程度的功能障碍,如肛门功能障碍会导致肛周湿疹以及肛周疼痛等问题,影响患者的日常生活。其中大便失禁是直肠癌患者术后最常见的肛门功能障碍,常因无法忍受大便失禁而行永久性结肠造口。
综上所述,腹腔镜ISR术可以达到肿瘤根治性切除的治疗效果,相对于开腹手术具有创伤小、出血量少、胃肠功能恢复快等优势。

