丘脑底核脑深部电刺激术联合美多芭治疗原发性帕金森病疗效观察
陈志凌,万辉
(1、福州总院476医院急诊科,福州 350002;2、南昌大学第四附属医院神经外科,南昌 330000)
帕金森病是一种好发于中老年人的神经退行性疾病,主要临床症状包括:运动迟缓、肌强直、静止性震颤以及姿势和步态损害,除上述运动症状外,便秘、嗅觉减退、睡眠障碍和抑郁症状等非运动症状也是其重要临床特征,严重影响帕金森病患者生活质量[1-5]。多巴制剂是治疗帕金森病的最有效药物之一,但长期服用导致帕金森病患者发生心脑血管疾病、认知功能障碍等的危险性增加[6]。随着功能神经外科治疗手段的发展,丘脑底核-脑深部电刺激术 (subthalamic nucleus-deep brain stimulation,STN-DBS)是治疗运动障碍性疾病的方法,与传统的立体定向神经核团毁损术治疗帕金森病相比较,具有疗效佳、手术安全、并发症发生率低等优点[7]。目前被广泛用于治疗原发性帕金森病,能改善帕金森病患者的症状,降低多巴胺能药物的使用剂量,从而减少长期口服药物所引发的不良反应[8-10],且术后可程控调节以改善运动障碍,本研究比较STN-DBS联合美多芭治疗与常规美多芭药物治疗原发性帕金森病的有效性和安全性,以期明确STN-DBS的优势。
1 资料与方法
1.1 临床资料
1.1.1 纳入标准 ⑴原发性帕金森病的诊断参照国际运动障碍学会 (MDS)2015年修订的临床诊断标准[11]。⑵18≤年龄<75岁。⑶急性左旋多巴冲击试验(ALCT)证实运动症状(UPDRSⅢ评分)改善率>30%。⑷药效逐渐减退,或出现药物治疗无效的症状波动(开关现象)和(或)异动症。⑸头部MRI未见明显异常。⑹行手术治疗的患者,术中可配合测试、术后可配合程控。⑺有独立能力并签署知情同意书。
1.1.2 排除标准 ⑴排除继发性帕金森综合征、阿尔茨海默病(AD);帕金森综合征或帕金森叠加综合征患者;⑵有明显认知功能障碍,并对患者日常生活能力产生严重影响 (如社交、工作和药物服用等);⑶严重的难治性抑郁或其他精神疾病;⑷不愿或无法配合手术患者;⑸整体状况不佳,严重脑损伤、严重脑萎缩、严重凝血障碍、无法控制的高血压等。
1.1.3 临床资料 选择2013年8月-2018年1月在解放军福州总院476医院神经外科诊断并治疗的原发性帕金森病患者共计75例,男性45例,女性 30 例;年龄 50~70 岁,平均(63.36±10.55)岁;受教育程度 5~20 年,平均(11.28±4.57)年;病程 2~10年,平均(6.27±2.65)年;入院时 UPDRS 评分 60~140分,平均(96.39-26.52)分;帕金森病生活质量量表(PDQUALIF)评分 40~105 分,平均为(87.63±29.75)分。根据患者自愿原则分为单纯药物治疗组(对照组)和STN-DBS联合药物治疗组(DBS组)。(1)对照组:35例患者,男性19例,女性16例;年龄50~75岁,平均为(65.36±9.55)岁;受教育程度 5~19 年,平均(11.85 4±1.55)年;病程 2~10 年,平均(6.26±1.75)年;人院时UPDRS评分60-140分,平均(102.35±23.42)分;PDQUALIF 评分 40~105 分,平均为(90.25±26.56)分。 (2)DBS组:40例患者,男性 21例,女性 19 例;年龄 55~75 岁,平均为(67.38 4±6.52)岁;受教育程度 5~20 年.平均为(10.53 4±2.35)年;病程2~10 年,平均(6.86±0.83)年;入院时 UPDRS 评分60~140 分,平均(100.13±25.64)分;PDQUALIF 评分为 40~105 分,平均为(87.32±24.19)分。 两组患者一般资料比较,差异无统计学意义(均P>0.5,表1)。
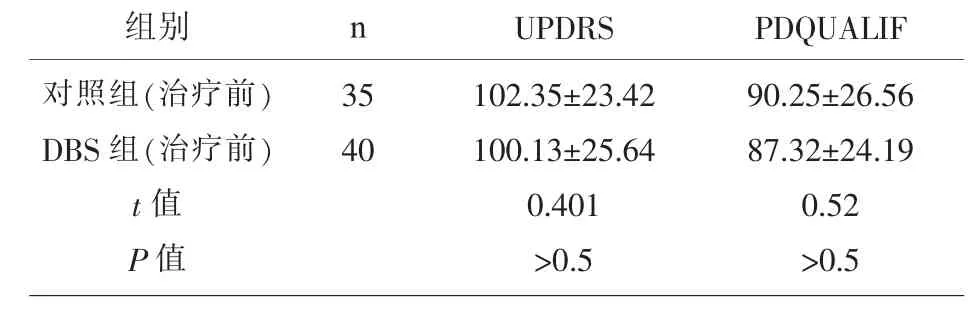
表1 治疗前两组患者UPDRS综合评分(x±s)、PDQUALIF综合评分(x±s)
(UPDRS,Unifield Parkinson’s Disease Rating Scale.统一帕金森病评价量表;PDQUALIF,Parkinson’s Disease Quality of Life Scale,帕金森病生活质量量表;DBS,deep brain stimulation,脑深部电刺激术)
1.2 研究方法
1.2.1 治疗方式 ⑴DBS组:40例患者于手术当日停用抗帕金森病及其他抗肌张力障碍药物,术前以 3.0 TMRI仪扫描,术中在局麻下安装 Leksell.G型立体定位仪(瑞典Elekta公司)后行CT薄层扫描(1.25mm或2.50mm),框架应平行于大脑前联合与后联合连线头皮投影,将图像输入Leksell Surgi Plan定位计划系统与术前的MRI数据融合,丘脑底核(STN)在眩像为相对可视靶点,确定坐标后,局麻下于额顶部弧形切开头皮,颅骨钻孔后根据确定的靶点坐标植入刺激电极,予实验性刺激,患者症状明显缓解,增加电压无明显副作用,用同样的方法植入对侧电极;(3)取下立体定向架,全麻下做右侧胸部锁骨下和右耳后切口,用探条制作皮下隧道,右锁骨下囊袋内植入神经刺激器,予延伸导线通过皮下隧道连接神经刺激器与双侧电极,逐层缝合头部切口、耳后切口和右锁骨下切口,术毕,术后2~4周开启神经刺激器,进行持续电刺激。患者意识恢复后1h予以多巴丝肼 (美多芭)375mg/d口服6个月。⑵对照组:35例患者均予以多巴丝肼(美多芭)治疗:规格:250mg/片(左旋多巴250mg,芐丝肼50mg,上海罗氏制药有限公司),750mg/d口服,连续治疗6个月。
1.2.2 疗效评估指标 所有患者均于治疗后3个月采用UPDRS量表评价治疗效果和PDQUALIF量表评价生活质量。
1.3 疗效评估标准 ⑴显效,治疗后运动功能显著改善,可进行日常工作及活动,且UPDRS评分下降>30%;⑵有效,治疗后运动功能有一定程度的改善,可进行简单活动、但不能工作,且UPDRS评分下降>10%~30%;⑶无效,治疗后运动功能无变化甚至加重,无法正常活动或工作,且UPDRS评分降低≤10%。总有效率(%)=(显效例数+有效例数)/总例数×100%。DBS术后并发症发生率 (%)=(DBS术后出现并发症例数)/DBS手术总例数×100%。
1.4 统计方法 采用SPSS 18.0统计软件进行数据处理与分析。计数资料以相对数构成比(%)或率(%)表示,两组间比较采用独立样本t检验;以P≤0.05为差异具有统计学意义。
2 结果
2.1 手术联合美多芭治疗或独立的美多芭药物治疗后,患者UPDRS量表之精神、行为和情绪、日常活动能力、运动功能和运动并发症评分均低于治疗前(P<0.01)。2、DBS 组患者 UPDRS 量表之精神、行为和情绪、日常活动能力、运动功能、运动并发症评分均低于对照组(P<0.01);(表 2),表明美多芭治疗后患者临床症状明显改善,脑深部电刺激术联合美多芭治疗效果更佳。DBS组患者PDQUALIF评分低于对照组(P<0.001;表 3),治疗后亦低于治疗前(P<0.001),表明美多芭治疗后患者生活质量明显改善,脑深部电刺激术联合美多芭治疗效果更佳。DBS组患者显效30例 (75%)、有效9例(22.50%)、无效 1例(2.50%),总有效率为 97.50%(39/40);对照组患者显效18例(51.43%)、有效10例(28.57%)、无效 7 例(20.00%),总有效率为 80.00%(28/35)。两组总有效率比较,差异具有统计学意义(P<0.001)。DBS组术后并发症发生率10%。
2.2 DBS组术后并发症 ⑴无一例患者发生皮质下穿刺道或颅内出血;⑵3例(7.50%,年龄均>70岁)术后短期内出现一过性精神症状(包括淡漠、抑郁及躁狂等),调整刺激参数及口服抗帕金森病药物剂量后,症状改善或基本消除;⑶1例(2.50%,年龄>70岁)术后出现语言、学习、记忆轻度下降,而语言流畅性有中度下降;⑷无一例患者出现感染、皮肤破溃以及电极断裂。后期回访期间,无死亡或颅内出血患者。
3 讨论
DorSey等[12]研究推测,我国人口老龄化趋势明显,到2030年,我国将有近500万帕金森病患者,届时将成为拥有帕金森病患者最多的国家。帕金森病的外科治疗有着悠久的历史,早在1817年外国学者就描述了相关帕金森病的外科治疗方法[13]。相对于传统毁损术,脑深部电刺激术具有可调节、并发症少等特点。脑深部电刺激术(DBS)是一种通过影像学方法(CT或MRI)立体定位靶点,手术中植入微电极并予以电刺激,从而达到改善帕金森病患者的运动症状和减少左旋多巴剂量的目的,其刺激靶点主要是丘脑底核(STN)、苍白球内侧部(GPi)、丘脑腹中间核(Vim)和脚桥核(PPN),尤以丘脑底核是最常见的脑深部电刺激术靶点[14]。STNDBS对改善静止性震颤、肌强直、运动迟缓和异动症等运动症状疗效显著,已广泛应用于帕金森病中晚期治疗[15-17]。但DBS治疗帕金森病的作用机制目前尚不明确,推测可能由于神经元受到刺激后产生不同效应,这种效应与电刺激的特性存在一定联系,并发挥平衡神经元电冲动的作用,降低其兴奋性,从而达到缓解静止性震颤、肌强直、运动迟缓和异动症等的目的。此次通过研究常规美多芭药物治疗与STN-DBS联合美多芭治疗原发性帕金森病的效果,结果显示,无论接受手术或药物治疗后两项评分 (患者UPDRS和PDQUALIF评分)均低于治疗前;STN-DBS联合美多芭治疗患者UPDRS和PDQUALIF评分均低于常规美多芭药物治疗组,STN-DBS联合美多芭治疗的总有效率为97.50%(39/40),高于常规美多芭药物治疗的 80.00%(28/35)。说明STN-DBS联合美多芭治疗可以显著改善帕金森病患者运动功能和生活质量,与既往研究相一致[18]。

表2 两组患者治疗前后UPDRS评分的比较(x±s评分)

表3 两组治疗前后PDQUALIF评分比较(x±s,分)
同时,我们通过上述研究发现,少数高龄的帕金森病患者(3例,年龄均>70岁,发生率7.50%)在接受STN-DBS治疗后出现短期的淡漠或抑郁等非运动症状,可能是因为刺激影响丘脑底核外侧缘引起的情绪变化,另外抑郁可持续数月与术后过多减少使用抗帕金森病药物有关,而增加药物使用可以减轻症状。也有学者研究发现STN-DBS还能改善帕金森病患者的焦虑、抑郁等非运动症状[19,20]。上述两种观点看似矛盾,但结合此次研究结果,我们发现接受STN-DBS手术后出现焦虑、抑郁等非运动症状的帕金森病患者中,均为高龄患者。同时Ory-Magne等[21]研究发现,STN-DBS的手术年龄与淡漠和抑郁的发生率呈正相关,认为手术年龄是术后疗效的重要预测指标。故我们认为高龄帕金森病患者接受STN-DBS手术治疗后出现焦虑、抑郁等非运动症状的概率相对较高,应充分权衡手术对患者的利弊后,完善术前评估及术后预防措施,从而减轻或降低患者术后出现焦虑、抑郁症状的程度。
对于少数患者(1例,年龄>70岁,发生率2.50%)术后出现语言、学习、记忆轻度下降等认知功能下降的情况,可能因为丘脑底核与前额皮层和基底节区有着广泛的联系,同时直接的电极刺激作用也会对认知功能产生影响,手术本身及术后减少使用多巴胺能药物也会导致认知功能下降,对于STN-DBS对认知功能影响的相关研究有许多,大多数学者认为尽管有轻度的认知功能下降发生可能,但STN-DBS是相对安全。一项随机对照研究[22]发现STN-DBS不会影响患者整体认知功能,但选择性降低患者前额部的认知功能,这些不会影响生活质量的改善。
综上所述,STN-DBS治疗帕金森病总体是安全可行的,帕金森病患者接受STN-DBS可以有效改善临床症状,减少药物用量,减少药物不良反应,提高生活质量。年龄可能是影响帕金森病患者术后疗效的重要因素之一,对于高龄帕金森病患者是否实施手术治疗,应采取审慎的态度,术前应综合评估,严格把握手术适应症及手术禁忌症。

