隆突性皮肤纤维肉瘤28例临床病理分析
万慧颖,徐敏燕,吴冬梅
(四川省医学科学院·四川省人民医院皮肤病性病研究所,四川 成都 610031)
隆突性皮肤纤维肉瘤(dermatofibrosarcoma protuberans,DFSP)是皮肤科少见的一种间叶源性低度恶性肿瘤,发生于皮下,多呈结节状,具有局部侵袭性,且易局部复发[1,2]。本文就28例DFSP的临床特征、组织学特点、免疫组化表达等进行分析,讨论其诊断和鉴别诊断要点,进一步降低临床误诊率。
1 资料与方法
1.1一般资料回顾性收集四川省人民医院皮肤性病研究所1993~2013年诊断的DFSP标本,均为手术切除后的肿物组织,经10%福尔马林液固定,常规取材、脱水、石蜡包埋。由两位高年资病理医生参照Ackerman外科病理学[3]进行复诊,去除有争议的病例,最终纳入28例,其中男17例,女11例,男女比例1.55∶1。临床发现皮肤斑片、斑块或隆起性结节5个月至10余年不等。
1.2方法提取筛选出的相应病例蜡块,取4 μm厚度做切片,苏木素-伊红(HE)染色,HE制成切片后行显微镜下形态学观察。免疫组织化学染色采用Envision二步法。一抗包括CK、Vim、CD34、Des、SMA、CD68、S-100、HMB-45、P53、和Ki-67。相关抗体及DAB显色试剂盒等由福建迈新及北京中杉金桥提供。同时选取已知阳性的组织切片做实验阳性对照,相同切片以PBS代替一抗做空白对照。免疫组化按一抗的显色定位不同,观察细胞胞浆、胞膜或胞核出现棕黄色颗粒状着色视为阳性。并结合临床和病理资料对28例DFSP进行归纳分析。
2 结果
2.1临床特征发病年龄19~64岁,其中20岁以下1例,20~50岁23例,50岁以上4例,平均发病年龄(38.5±14.3)岁。病程5个月至10余年不等。发病部位为腹部10例,腰部8例,胸部5例,肩部2例、上臂、大腿后侧、肘部各1例。临床表现为生长缓慢的暗红色、暗褐色、紫红色斑块或结节,隆起于皮面,局部可见瘢痕样或萎缩性斑块,直径1.5~10.0 cm不等,质地坚硬,部分可见表面破溃结痂(见图1)。
2.2病理结果
2.2.1大体检查 送检肿物直径1.5~10.0 cm,表面均有皮肤及皮下组织,质地坚硬,形状不规则。切面多为灰白色鱼肉状,未见明显出血坏死。2例有局灶蜂窝状改变。

图1 隆突性皮肤纤维肉瘤大体表现
2.2.2镜检 本组病例以经典型为主,占23例,粘液型3例,纤维肉瘤型2例。镜下肿瘤位于真皮层,病变部位肿瘤细胞呈短梭形,弥漫生长,周边界限不清,未侵及表皮,并与表皮形成狭窄的细胞疏松区。肿瘤中心细胞丰富,形态呈较为单一的短梭形,呈旋涡状排列形成席纹状或车辐状结构,细胞核细长,核分裂像多数<5/HPF,仅1例为9/HPF。泡沫状细胞、多核巨细胞不明显,可见脂肪细胞被包入瘤细胞内形成蜂窝状结构。间质出现多少不等的粘液样变,粘液型者更为明显(见图2)。纤维肉瘤型可见部分细胞异型性明显,核分裂增加,瘤细胞排列呈束状、人字形或鱼骨状。其它镜下表现还包括细胞异型、间质炎性反应等。见表1。

图2 隆突性皮肤纤维肉瘤镜下表现(HE,×100) a:表皮棘层增生,肿瘤与表皮之间可见细胞疏松区;b:丰富的梭形肿瘤细胞,呈典型的编席状或车辐状排列;c:肿瘤分割包裹皮下脂肪细胞,呈特征性的蜂窝状排列;d:肿瘤间质粘液样变

表1 28例隆突性皮肤纤维肉瘤镜下部分病理特征
2.2.3免疫组化染色 肿瘤细胞成分主要呈CD34和Vim弥漫强阳性表达,粘液型和纤维肉瘤型对CD34的表达稍弱。SMA部分病例见少量细胞散在表达,CD68在泡沫细胞和多核巨细胞中表达,CK、S-100、HMB-45、P53、Des均为阴性,Ki-67指数普遍<5%,纤维肉瘤型在10%左右(图3)。见表2。
3 讨论
隆突性皮肤纤维肉瘤是真皮和皮下间叶性肿瘤,本病于1890年首次报道,1925年Hoffman将其命名为DFSP。新的世界卫生组织肿瘤分类认为它是表浅的低度恶性肿瘤[4]。约占软组织肉瘤的6%[5]。容易局部复发,但转移率低。DFSP的起源仍无定论,目前认为,隆突性皮肤纤维肉瘤及其亚型来源于纤维母细胞[6]。
DFSP通常出现在青年或中年,男性略多,发病高峰20~50岁[7]。也有证据显示儿童时期起病,青年时期变得明显。甚至还有先天发病的报道[8,9]。肿瘤最常发生在躯干,包括胸、背、腹壁。其次为四肢及头颈部[10]。其它部位少见。本病的发病原因尚不明确,遗传、疫苗接种、手术瘢痕和创伤等均可能与肿瘤的发生有关[11,12]。DFSP通常表现为皮肤斑块状的实性结节,具有缓慢而持续生长的病史,常持续数年或数十年。皮损特点缺乏特异性[13],以无痛性皮肤肿块为主要症状。早期病变界限清楚,为孤立、较硬的斑疹,周围呈红色、褐色或正常肤色,可类似于局限性硬皮病或硬化型基底细胞癌。肿瘤进展缓慢,最终发展成典型的隆突形态,在斑块状的基底之上长出大小不一的一个或数个结节,质地较为坚实。临床易被误认为良性肿瘤而延误治疗。因此,早期病理诊断尤为重要。使用细针抽吸,可以诊断或至少怀疑为DFSP[14]。
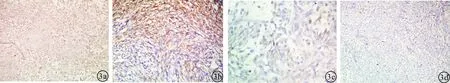
图3 隆突性皮肤纤维肉瘤免疫组化表达 a:Vim肿瘤细胞强阳性表达(Envision,×100);b:CD34肿瘤细胞弥漫阳性表达(Envision,×400);c:SMA部分病例灶性表达(Envision,×400);d:Ki-67阳性指数低(Envision,×100)。
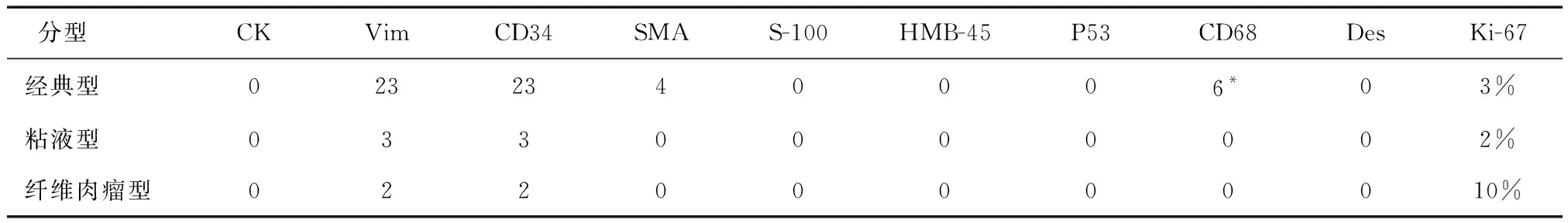
表2 28例隆突性皮肤纤维肉瘤免疫组化阳性染色结果 (例)
DFSP几乎都位于真皮,常由真皮侵犯皮下组织。整体而言,这类肿瘤比良性纤维组织细胞瘤大得多,但是不能仅依据大小就做出或排除DFSP的诊断。多数切除的DFSP,表现为质硬的斑块伴有一个或多个相关结节。多发性皮肤隆起和皮下肿物较常见于复发性肿瘤。肿瘤切面灰白色、质硬,个别区域显示凝胶或半透明形态。有时可见出血和囊性变,很少见到坏死。
DFSP按组织学形态可分为经典型、粘液型、色素型、颗粒细胞型、纤维肉瘤型、萎缩型、硬化型、栅栏状和Verocay小体型、伴有巨细胞纤维母细胞样区域型等10多个亚型[13]。其中以经典型最为多见,纤维肉瘤型预后最差,有较高的复发和转移趋势[15]。镜下DFSP典型表现为肿瘤弥漫浸润真皮层,侵及皮下组织,尤其是沿脂肪的纤维分隔带。表皮通常不受累,肿瘤的浅表与表皮间常见狭窄的肿瘤细胞稀疏区,称分界区(Grenz zone)。肿瘤中心由致密、一致、纤细、异型性低的梭形细胞组成,排列成编席状、旋涡状或车辐状。肿瘤细胞常紧密包绕汗管、毛囊等皮肤附属器,但不破坏它们。细胞核多形性不明显,具有较低的核分裂活性。有些肿瘤具有明显的粘液性基质。肿瘤周边表浅区域细胞密度降低,梭形细胞被真皮胶原分割。深在区域梭形细胞增生,包绕脂肪组织,形成蜂窝状结构。少数病例可见泡沫细胞、炎性细胞以及类似于巨细胞纤维母细胞瘤的巨细胞等。有时可见独特的粘液样结节,粘液样结构可以是局灶性,有时也可以是肿瘤的显著特点[16]。间质炎细胞较少,偶可见大片淋巴细胞及浆细胞浸润。纤维肉瘤型DFSP的诊断标准为纤维肉瘤样区域超过肿瘤的5%[13];粘液样型DFSP的诊断标准是粘液样区域需占肿瘤的50%以上[17];色素型DFSP也称为Bednar瘤,除了具有一般DFSP的所有表现外,还有数量不等的树突状细胞,这些细胞含有大量黑色素。有文献报道10%-15%的DFSP会向纤维肉瘤转化[18],纤维肉瘤病变区域不再呈席纹状生长,而呈典型的青鱼骨样。有时DFSP可向更加多形性的恶性纤维组织细胞瘤或软组织恶性巨细胞瘤发展[19]。
免疫组化上,肿瘤细胞对波形蛋白、肌动蛋白(局灶且不稳定)和CD34(很强且稳定)呈阳性反应[20],而对S-100、HMB-45、CK、EMA、Des等标记阴性。但需要特别注意的是,CD34和Vim的表达并非特异,诊断时必须结合光镜形态学综合判断。
近年来,随着细胞遗传学及分子病理技术的发展,发现在90%的DFSP病例中,有t(17;22)(q22;q13)染色体易位,从而导致17号染色体上胶原基因的I型α链和22号染色体上的血小板源性生长因子β相互融合,产生COL1 A1/PDGFB融合基因,从而导致肿瘤的发生[21,22]。通过FISH或RT-PCR检测方法,几乎所有DFSP包括各种亚型,其中包括存在高度恶性区域的DFSP都能检测出融合基因COL1 A1和PDGFB这种特征性染色体[23,24]。因此,检测DFSP中的COL1 A1/PDGFB融合基因的表达对DFSP的诊断有重要价值[25]。
DFSP在镜下应与以下肿瘤相鉴别:①纤维组织细胞瘤或皮肤纤维瘤:本病通常较小,有表皮增生,瘤细胞由成纤维细胞构成,但是较少延伸到脂肪小叶。②神经纤维瘤:肿瘤细胞排列稀疏,呈波纹状,可见现触觉样小体,免疫组化S-100阳性,CD34阴性。③纤维肉瘤:此肿瘤多位于四肢深部软组织,呈特征性的“人字形”或“鱼骨样”排列,异型性明显,核分裂易见,CD34阴性。④恶性纤维组织细胞瘤:多见于老年患者,生长迅速,显示较高程度的细胞非典型性、多形性和分裂活性,常见坏死,CD34阴性。⑤粘液性脂肪肉瘤:与粘液性隆突性皮肤纤维肉瘤的区别在于无编席状或车辐状结构、存在脂母细胞、CD34阴性以及深层软组织侵犯。此外,临床上还应与硬斑病、萎缩性皮肤病、血管瘤等相鉴别。
DFSP的自然病程特点是小范围切除后极易局部复发。复发率可高达26%~60%[11,21]。但罕见有局部淋巴结和远处转移,文献有转移至肺的报道[26]。临床治疗以局部手术切除为主,并适当扩大范围2~3 cm。Mohs外科手术具有高治愈率和手术创面小两大优势[27],基本原则是在肿瘤切除干净的前提下最大限度的保留正常组织及功能。本组DFSP均行肿物单纯切除或扩大切除术,部分患者经我院活检确诊后回当地医院治疗,切缘无法估计。28例患者中失访6例,其余22例随访,复发4例,未发现转移患者,患者均健在。

