连续性θ节律性磁刺激对卒中后疼痛病人皮层诱发电位的影响*
段 强 黄肖群△ 肖 斌 袁 华 牟 翔 孙 玮
(1三峡大学人民医院 宜昌市第一人民医院康复医学科,宜昌443000;2陕西省西安市新城区第四军医大学西京医院康复理疗科,西安710032)
中枢性卒中后疼痛 (central post-stroke pain, CPSP)是脑卒中病人常见的一种并发症,是“中枢神经系统体感通路上的脑血管性病灶的直接后果所导致的疼痛”。近年来,其临床报道逐渐增多,最近的报道其发病率已高达35%[1]。与不伴中枢性卒中后疼痛的病人相比,患有CPSP病人的运动功能、日常生活活动能力的改善明显偏低,极大的影响了病人的恢复进程,降低了病人的生活质量[2]。自重复经颅磁刺激 (repetitive transcranial magnetic stimulation,rTMS) 应用于临床以来,其对各种中枢性疼痛如脊髓损伤神经病理性疼痛、中枢性卒中后疼痛、肌筋膜痛等均有一定的疗效。连续性θ节律性磁刺激 (continuous theta burst stimulation, cTBS)又叫做丛状刺激,是模式化磁刺激的一种,其作用原理与rTMS基本一致,但是它能快速引出神经功能的抑制作用,而不引起神经功能兴奋性增加,具有一定的镇痛作用。然而,临床上关于cTBS的应用报道并不多见,其镇痛持续的效果和机制也完全不清楚。因此,本研究通过观察cTBS对CPSP的治疗效果,初步探讨其对卒中病人大脑皮层诱发电位的影响,从而为临床诊疗工作提供客观的理论与实践依据。
方 法
1.一般资料
入选标准:①年龄在30~70岁之间;②符合全国第四届脑血管病学术会议修订的各类脑血管病诊断要点中脑血管病诊断标准,均经头颅CT/MRI扫描证实[3]; ③首次卒中,病程在2周~24月之间。④有明确的CPSP症状,符合国际CPSP诊断标准[2];⑤所有病人经VAS疼痛评分,≥3分;⑥所有病人均签署知情同意书。
排除标准:①合并严重心肺肾等疾病;②意识障碍 ;③严重言语障碍;④其他原因致类似CPSP疼痛;⑤对奥卡西平禁用或慎用者;⑥因各种原因脱落者。
选取在2012年1月至2015年1月我科住院治疗并诊断为CPSP的脑卒中病人共18例。按照数字表法随机分为治疗组与对照组,每组各9例。两组病人的一般资料组间比较,差异无统计学意义(P< 0.05)。
2.研究方法
所有病人在入院后据病情给予内科对症处理,并给予偏瘫肢体综合训练、中频脉冲电治疗、松弛治疗等常规康复干预,并接受奥卡西平片(150 mg口服 2次/日)。对照组在常规物理干预和药物治疗的基础上给予假刺激,无输出的线圈放置在治疗组相同的脑区,只给予相同频率声音的提示。治疗组在此基础上增加cTBS (武汉依瑞德公司生产,型号CCY-1) 治疗,刺激部位为健侧大脑M1区,静息运动阈值 (resting movement threshold, RMT) 为80%,强度为16%,刺激时间40 ms,间歇160 ms,总刺激个数600,每次40 s[4];以上所有治疗均每天1次,每周6次,连续2周。
3.疗效评定
所有病人均在治疗前及治疗2周后均接受VAS疼痛量表、运动诱发电位 (motor evoked potentials,MEP)、短皮层内抑制/皮层内易化 (short intracortical inhibition/ intracortical facilitation, SICI/ICF)等评估[5]。其中,VAS疼痛量表按疼痛等级分为0~10分;运动诱发电位采用磁刺激仪,刺激线圈外径10.5 cm,最大输出强度2.5 T。刺激点:头顶Cz点前5 cm,刺激强度度以第一背侧骨间肌出现收缩为准,采用90%。受测试者仰卧位,记录电极置于双侧第一背侧骨间肌的肌腹表面,阳极置远端,阴阳极距离为2 cm,极间阻抗小于5 kΩ,信号经肌电图仪放大并记录,重复测多次,并以波幅最大、峰潜伏时最短,重复性好的电位为准。SICI:是先给予一个阈下刺激(条件刺激),约1~6 ms后再给予一个阈上刺激(试验刺激); ICF:间隔8~30 ms后给予阈上刺激;通过EMG在第一背侧骨间肌记录条件刺激对试验刺激所产生的MEP的影响来评价,即条件刺激引起神经元活性改变后,使该神经元对下一个试验刺激的反应阈发生改变,从而在可见相应肢体肌肉上所记录到的MEP波幅改变。
4.统计学分析
采用SPSS 17.0统计学软件进行统计学分析。计量资料采用均数±标准差 (±SD)表示,组内治疗前、后比较采用配对t检验;组间治疗前、后比较采用独立样本t检验;MEP波幅、SICI/ICF的变化与VAS评分的相关性研究采用Pearson相关分析,以P< 0.05为差异有统计学意义。
结 果
1.两组病人治疗前一般资料比较
两组病人在年龄、病程、卒中部位和治疗前VAS疼痛评分等方面均无显著性差异(见表1)。
2.治疗前及治疗后VAS,MEP,以及SICI/ICF比较
治疗2周后发现,两组VAS疼痛评分均有降低(P< 0.01),与对照组比较,治疗组降低更明显(P< 0.05); 治疗组中,上肢MEP波幅和潜伏期均较治疗前明显改善(P< 0.05),对照组也有改善,但无统计学意义;治疗组中SICI,较治疗前明显降低(P< 0.05),对照组也有变化,但无统计学意义;治疗后两组中ICF值均有变化,但无统计学意义(见表2)。
3.Pearson相关分析
将VAS疼痛的改善程度与MEP波幅、SICI、ICF分别进行相关性分析发现,VAS疼痛的改善程度与SICI呈正相关(P< 0.05,见表3)。
讨 论
脑卒中是临床常见的脑血管意外,目前卒中后的康复主要集中在卒中后运动、认知、言语、吞咽、单侧忽略等各方面,在对中枢性卒中后疼痛的认识较少。卒中后疼痛 (Pain after Stroke, PS) 根据其发病原因及表现一般可以分为三类[6]:CPSP、卒中后肩痛 (post-stroke shoulder pain, PSSP) 和复杂性区域疼痛综合征 (complex regional pain syndrome,CRPS)。 其中,CPSP是因中枢神经系统损伤导致偏瘫患肢或者伤侧大脑的一种神经性疼痛。近年来,因其极大的影响了卒中后病人肢体功能的康复效果和病人的生活质量,临床医师也逐渐认识到其在康复中的作用,其临床报道也逐渐增多[7]。但其治疗方法并不如意,主要有手术治疗及非手术治疗,手术治疗因有创、手术风险及费用等原因多作为非手术治疗无效的选择;非手术治疗中以药物治疗较常见,主要为抗癫痫药物及三环类药物为主,其效果欠佳[8,9]。
TMS作为一种无创、安全的刺激方式,目前主要用于促进卒中病人运动、感觉功能的恢复,但研究也发现,TMS对于脊髓损伤后神经病理性疼痛、三叉神经痛、纤维肌痛、卒中后神经痛、幻肢痛等也具有较好的镇痛作用[10~12]。根据TMS刺激模式的不同[13],大致可以分为单脉冲TMS、成对经颅TMS、成对关联TMS、重复经颅TMS和模式化磁刺激。节律性磁刺激 (TBS) 是模式化磁刺激的一种,又叫做丛状刺激,按照刺激间隔时间的不同可以分为间歇性TBS (iTBS) 和连续性TBS (cTBS),后者丛内频率为50 Hz,3个脉冲为一丛,连续重复频率为5 Hz。cTBS虽然是5 Hz内携带50 Hz的高频连续刺激,但不引起神经功能兴奋性增加,而能快速引出神经功能的抑制作用。本研究中也发现,与重复经颅磁刺激相似,治疗组中9例病人的神经痛均有不同的缓解,与对照组相比,具有更好的镇痛效果。这表明cTBS结合常规药物治疗对于卒中后中枢性神经痛也具有较好的镇痛作用。
表1 两组病人一般资料的比较 (n = 9,±SD)Table 1 General information of patients in two groups (n = 9,±SD)
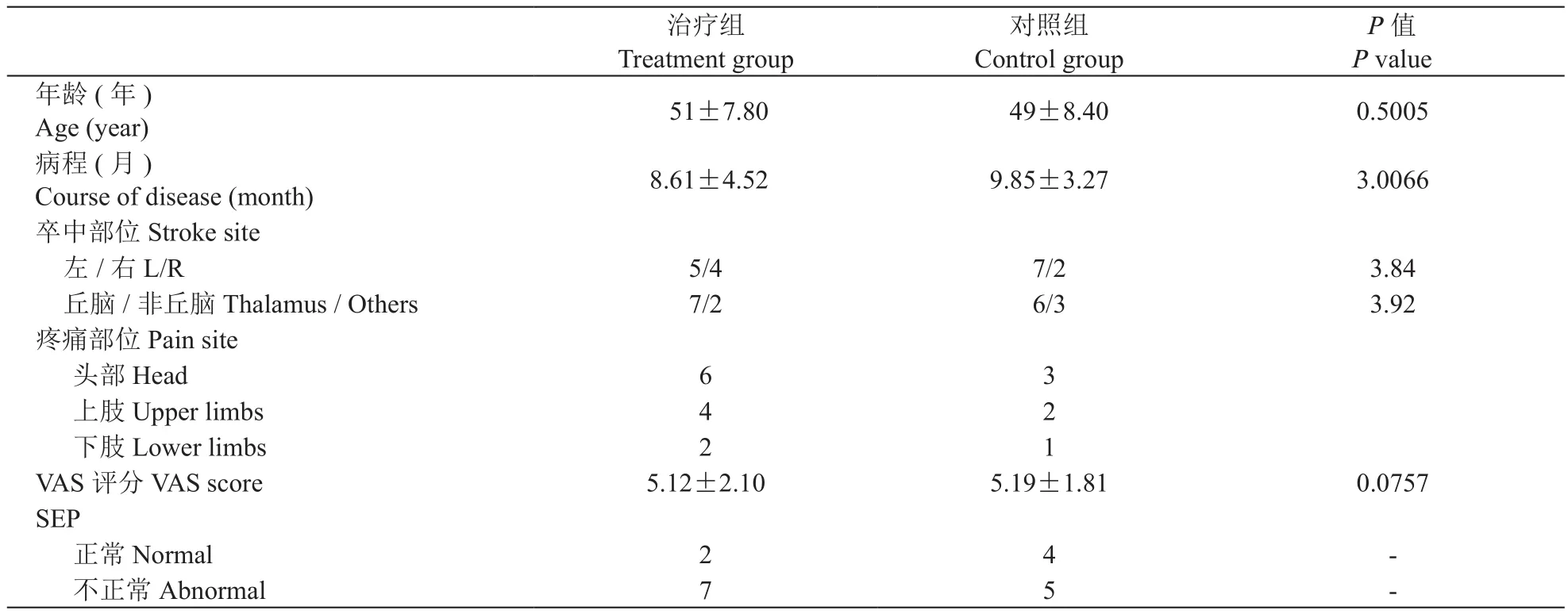
表1 两组病人一般资料的比较 (n = 9,±SD)Table 1 General information of patients in two groups (n = 9,±SD)
P值P value年龄(年)Age (year) 51±7.80 49±8.40 0.5005病程(月)Course of disease (month) 8.61±4.52 9.85±3.27 3.0066卒中部位Stroke site左/右L/R 5/4 7/2 3.84丘脑/非丘脑Thalamus / Others 7/2 6/3 3.92疼痛部位Pain site头部Head 6 3上肢Upper limbs 4 2下肢Lower limbs 2 1 VAS评分VAS score 5.12±2.10 5.19±1.81 0.0757 SEP正常Normal 2 4 -不正常Abnormal 7 5 -治疗组Treatment group对照组Control group
表2 两组病人治疗前后VAS, MEP, 以及SICI/ICF比较 (n = 9,±SD)Table 2 The VAS scores, MEP and SICI/ICF in two groups (n = 9,±SD)

表2 两组病人治疗前后VAS, MEP, 以及SICI/ICF比较 (n = 9,±SD)Table 2 The VAS scores, MEP and SICI/ICF in two groups (n = 9,±SD)
*P < 0.05,与对照组相比;#P < 0.01,与治疗前相比*P < 0.05, compared with control group; #P < 0.01, compared with pre-treatment.
t值t value VAS 治疗组Treatment 5.12±2.10 2.73±1.29* 2.9092#对照组Control 5.19±1.81 3.80±0.77 2.1200#MEP波 幅Amplitude, uV组别Groups治疗前Before治疗后After治疗组Treatment 25.09±3.28 19.89±4.68 2.7297*对照组Control 24.79±4.08 22.45±4.92 1.0983 SICI (uV) 治疗组Treatment 0.58±0.11 0.39±0.18 2.7021*对照组Control 0.40±0.27 0.37±0.13 0.3003 ICF (uV) 治疗组Treatment 1.01±0.13 1.09±0.24 0.8793对照组Control 1.19±0.26 1.20±0.16 0.0983治疗组Treatment 3.19±0.46 3.83±0.52# 2.7655*对照组Control 3.13±0.39 3.19±0.41 0.3181潜伏期Latencies, ms

表3 相关性分析Table3 the Correlation Analysis
关于TMS治疗神经痛的刺激部位的选择,也是临床关注的焦点之一[14,15]。磁刺激最初报道缓解中枢性疼痛的刺激部位是1995年Migita记录的初级运动皮质区,随后人们对不同的刺激部位进行了研究。目前常用的主要刺激部位有初级运动区 (M1)、运动前区 (preM)、辅助运动区 (SMA) 和初级感觉区(S1) 等。Hirayama[16]等对病人的M1、S1、preM和SMA进行刺激,结果M1区的疼痛减少50%,而其他部位无效。因此,一般多认为M1区是TMS有效治疗疼痛的刺激靶区。然而,这些研究的刺激部位多为患侧M1区高频刺激,单独在健侧的M1区刺激较少。本研究发现,cTBS作用于健侧M1区亦能缓解卒中后中枢性神经痛。那么,其缓解疼痛的机制可能是什么呢?
目前,卒中后神经痛的机制主要有半球间去抑制(disinhibition)、中枢失衡(central imbalance)、中枢敏化(central sensitization)和脊髓丘脑束功能改变等,多认为其疼痛与皮质-丘脑-脊髓通路有关[17]。TMS能够缓解疼痛,主要有改变神经组织的兴奋性、调节神经递质、改变血流代谢和神经可塑性改变有关[18,19]。本研究中观察到,在采用cTBS刺激M1区后病人的疼痛减轻的同时,我们记录到的患侧MEP和SICI潜伏期有不同程度的降低,而MEP波幅增加,且与对照组相比,治疗组的改善更明显(P< 0.05),而SICI是反应皮层间的抑制程度的指标。在相关性研究中,我们发现,VAS疼痛缓解程度与SICI的改变正相关,这也同样证明这一点。而MEP波幅虽然降低,但并没有相关性,这我们考虑是因为MEP记录的是上肢拇短展肌的波幅变化,对部分疼痛位于下肢和头面部的病人虽有改善,但并无显著性相关。因此,我们的研究中更倾向于,cTBS一方面可能通过降低健侧皮质兴奋性,减少对患侧半球过度支配,重建跨胼胝体抑制的平衡,相对增加患侧皮质兴奋性,调节丘脑核团兴奋性,提高痛阈,从而缓解疼痛;另一方面,cTBS作用于运动皮层后,可能同时作用于与因疼痛激活的相关其他结构,如前额叶皮层内侧、扣带回前部等,它们共同对发生疼痛的丘脑位点产生下行抑制,从而产生镇痛效应[20,21]。另外,关于SEP检测,部分病人因SEP不能引出,而不能进行统计分析,但并不能排除皮层感觉区对疼痛产生影响。
总而言之,连续性θ节律性磁刺激联合药物治疗可以有效缓解卒中后中枢性疼痛,且其机制可能是通过改善病人皮层兴奋性及大脑半球间的抑制作用来达到镇痛目的,其具体的分子机制有待于进一步研究。
当然,研究中我们也发现了一些不足之处,比如,没有进行rTMS与cTBS疗效的比较观察、没有将SI区与M1区进行对照研究,疼痛评估方法缺少量化标准,主观性强等,今后我们将选取大样本,结合EEG或者功能性磁共振、头颅导航磁刺激,准确定位、量化疼痛评估标准,或者与脑血流图、相关神经递质结合,进一步观察卒中神经痛的脑电活动及皮层兴奋性改变等。

