腹横肌平面阻滞药物扩散范围及治疗腹壁痛的效果*
袁 帅 崔敬禄 熊东林 郑虎山△ 金文哲△
(1延边大学附属医院疼痛科,延吉 133000;2深圳市南山区人民医院疼痛科,深圳 517000)
超声引导下腹横肌平面 (transversus abdominis plane, TAP) 阻滞具有损伤范围小、成功率高、并发症少等特点而广泛应用于临床实践。不同入路的TAP阻滞,由于药物注射点不同,药物的沉积不同而使阻滞范围不同。那么TAP阻滞后,药物扩散范围到底有多大,这方面的研究并不多见。TAP临床运用中,要根据具体手术方式、具体疼痛原因及部位选择较为适合的入路阻滞方式[1]。TAP阻滞作为一种新的区域阻滞技术,结合TAP阻滞的多模式镇痛用于减轻腹部手术后疼痛的效果在国内外均已经得到了广泛的证实[2]。而TAP阻滞治疗各种腹壁痛的临床研究很少,因此,有必要深入研究超声引导侧入路法TAP阻滞药物扩散范围,并进一步证明其治疗腹壁痛的效果。
方 法
1.一般资料
选择2016年3月至2017年10月延边大学附属医院疼痛科收治的腹壁痛病人40例,男11例,女29例,年龄35~59岁,体重53~80 kg;腹壁痛在T9~T12支配区。本研究已获本院伦理委员会批准,并与病人及家属签署知情同意书。
纳入标准:支配区位于T9~T12伴有腹壁痛的肌筋膜疼痛综合征病人。
排除标准:①腹腔内脏器官器质性病变及肿瘤病人;②合并严重心、肺、肝、肾功能不全病人;③凝血功能障碍者;④ 腹部或者皮肤软组织感染者;⑤有腹部手术史者。
2.方法
超声引导侧入路法(又称腋中线法):病人取仰卧位,采用MyLab Five超声诊断系统进行超声引导,将探头平行脐水平置于腋前线上,扫描该区域,获得清晰的TAP阻滞图像。在超声探头纵轴中位线进针(平面内技术),当针尖刺破腹外斜肌和腹内斜肌到达腹横肌平面后,回抽无血无气,A组第一次注射造影剂及镇痛混合液10 ml(造影剂5 ml + 2%利多卡因2 ml + 地塞米松1 ml +生理盐水2 ml = 10 ml),DSA设备前后位和侧位上观察图像的变化,第2次至第5次注射镇痛液10 ml,间隔时间1周; B组第1次治疗时注射造影剂及镇痛混合液20 ml(造影剂10 ml + 2%利多卡因4 ml +地塞米松1 ml + 生理盐水5 ml = 20 ml),DSA前后位和侧位上观察图像的变化,第2次至第5次注射镇痛液20 ml,间隔时间为1周。
3.观察指标
abcde代表的含义如图1所示,在X线引导下,以针尖为中心,在前后位上,向上向下分别划与脊柱的平行线,a代表在这条线上针尖0点到与图形最上端与脊柱垂直线的交点A的距离;b代表在这条线上针尖0点到与图形最下端与脊柱垂直线的交点B的距离;在前后位上,向左向右分别划与脊柱的垂直线,c代表在这条线上针尖O点到与图形最左端划脊柱的平行线交点C的距离;d代表在这条线上针尖O点到与图形最右端划脊柱的平行线交点D的距离;e代表在侧位图形上,经过针尖图形的宽度。分别于治疗前、治疗后行视觉模拟评分法(visual analogue scale, VAS)评分,评分标准:0分,无痛;10分,难以忍受的疼痛。
4.统计分析
采用SPSS 14.0软件包进行统计学处理,计量资料采用均数±标准差(±SD)表示,组间比较采用t检验,治疗前后比较采用配对t检验,P< 0.05为差异有统计学意义。
结 果
两组病人年龄、体重及治疗前VAS评分的差异均无统计学意义(见表1)。B组药物扩散面积明显大于A组(P< 0.05,见表2)。两组病人与治疗前相比,腹壁痛明显改善(P< 0.05),治疗后,两组病人的VAS评分较治疗前均下降(P< 0.05),治疗结束后第7天、1个月、3个月及6个月,与A组比较B组VAS评分降低更明显(P< 0.05,见表3)。
表1 两组病人一般资料比较(n = 20,±SD)
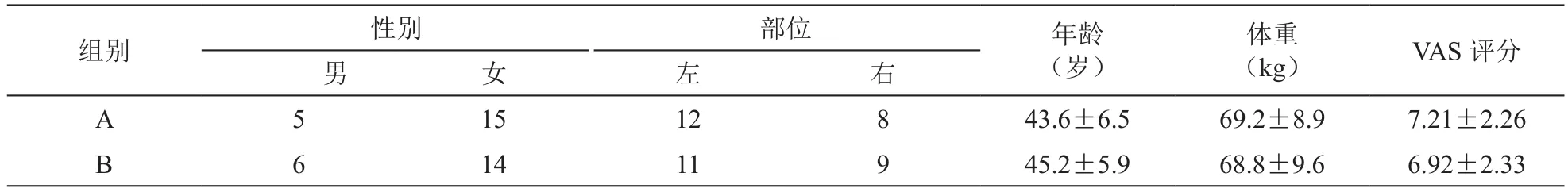
表1 两组病人一般资料比较(n = 20,±SD)
组别 性别 部位 年龄(岁)男女左右体重(kg) VAS评分A 15 12 8 43.6±6.5 69.2±8.9 7.21±2.26 B 6 14 11 9 45.2±5.9 68.8±9.6 6.92±2.33 5
表2 两组病人药物分布范围的比较(n = 20,±SD, mm)

表2 两组病人药物分布范围的比较(n = 20,±SD, mm)
*P < 0.05,与 A 组比较
组别 a b c d e A 27.98±5.36 25.26±4.49 11.18±3.37 7.36±2.79 14.99±4.46 B 43.88±6.83* 32.58±5.29* 16.88±3.69* 10.21±3.65* 22.82±5.19*
表3 两组病人VAS评分的比较(n = 20,±SD)

表3 两组病人VAS评分的比较(n = 20,±SD)
*P < 0.05,与治疗前比较;△P < 0.05,与 A 组比较
治疗后7天 1个月 3个月 6个月A 7.21±2.26 3.15±1.22* 3.18±1.53* 3.45±0.65* 3.50±0.77*B 6.92±2.33 1.26±0.63*△ 1.38±0.37*△ 1.95±0.47*△ 2.02±0.50*△组别 治疗前
讨 论
有数据显示,腹壁痛占慢性腹痛的30%,占消化内科就诊病人的10%[3],可见在临床上,腹壁痛病人并不少见。而在医疗实践中,急慢性腹壁痛往往被认为是腹腔内脏引起,很容易被忽视,导致误诊误治。
腹壁痛的发病机制最公认的假说认为,在T7-T12胸神经前皮支经过腹直肌鞘[4],该神经在进入纤维环以前形成一个直角,经过腹直肌鞘后层,而后再经过前鞘,神经分支在下方再次形成直角[3]。脂肪垫通常可使神经血管束自由通过纤维环,然而神经卡压可能导致缺血,进而产生疼痛。受卡压的神经可随腹内、外压力的变化而被推动或牵拉。此外,如糖尿病、带状疱疹、外伤、癌症也可引起类似的疼痛[5]。
腹壁痛的诊断相对简单,准确的病史采集和体格检查就可提示有腹壁痛的可能。疼痛常为局限性锐痛,并常出现在伤口附近。抬举、站立或咳嗽等使腹壁张力增加的活动常可诱发,坐位、平躺或用手轻触亦可缓解。体格检查的体征是小范围的局限痛,提示疼痛来源于腹外侧。病人可以用手指出其痛点,最大的触痛范围半径为1~2 cm。然而,有些病人可能有多处疼痛,此类病人会感觉到更大范围的钝痛。Carnett试验有助于鉴别疼痛来源于腹内或腹壁[6]。Carnett试验是病人取仰卧位,令其抬头或抬腿使腹部肌肉紧张,若该体位时疼痛持续甚至加剧,可以认为Carnett征为阳性,其腹痛可能源自腹壁;反之,若疼痛减轻,则为Carnett征阴性,疼痛源自腹内[7]。
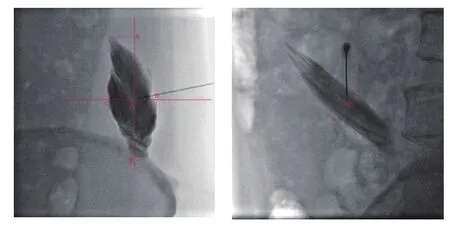
图1 TAP阻滞注射10 ml造影剂和生理盐水的混合物,前后位及侧位扩散图像

图2 TAP阻滞注射20 ml造影剂和生理盐水的混合物,前后位及侧位扩散图像
对于病情较轻者,避免剧烈活动以及局部治疗就有明显效果[8]。然而,对于中度至重度的疼痛的病人,TAP阻滞优于传统的腹直肌鞘和髂腹股沟、髂腹下神经阻滞[9]。TAP阻滞前腹壁神经麻醉腹部组织,在TAP平面注射局麻药,可以成功阻滞相对应神经疼痛信号的传导,产生有效的镇痛作用,常用于腹部手术麻醉和急慢性疼痛治疗[10]。传统体表定位法穿刺成功率低,而超声引导使TAP阻滞更加容易操作,应用范围更广。
Tran[11]等利用超声技术在尸体侧腹部腋中线水平行超声引导下TAP阻滞,通过解剖发现染料扩散涉及T10-L1神经,本研究认为这种腋中线水平的TAP阻滞较适合脐水平以下腹部切口手术。本研究穿刺针尖在脐水平(T10),造影剂向头侧垂直扩散距离为43.88±6.83 mm,估计上升平面可达到T8、T9,在活体和尸体上TAP扩散范围肯定是不同的。另有研究报道,TAP阻滞的镇痛范围取决于注射药物的部位和药物在体内的扩散方式。肋缘下和腋中线法药物向前扩散,后路法药物向后扩散[12]。
综上所述,本研究通过超声引导侧入路法的注药后扩散范围的研究,观察到的结果是超声引导下TAP阻滞后,DSA前后位及侧位上药物呈“叶子”型扩散,随着注药量增加,扩散面积亦增加,腹壁痛减轻更显著,本研究推测,可能通过扩大阻滞平面,增强其疗效。本研究为超声引导不同入路TAP阻滞的应用提供了指导,也为TAP阻滞的临床实践奠定了坚实的理论基础。本文的不足之处是病例数相对较少、扩散容量比较略显简单、没有结合其他影像技术及其他入路作综合比较,因此,还有待于进一步深入研究。

