不同肝素化时机用于体外循环心脏手术的对比研究*
张 建,刘达兴,梁贵友,刘 靖,汤 全(遵义医学院附属医院心血管外科,贵州遵义563003)
体外循环是心血管外科领域最重要的辅助技术。在国内有近75%的心脏外科手术需应用体外循环技术辅助[1]。同时,为防止血液在体外循环管道中凝固,全身肝素化是体外循环技术的必要环节。近年来,有学者认为,在体外循环中过度肝素化会增加手术出血及感染风险[2]。因此,如何选择不同全身肝素化时机、减少肝素化对患者的不利影响目前尚未见相关文献报道。本研究通过前瞻性研究,比较开胸前肝素化与开胸后肝素化患者围手术期临床结果,旨在为临床体外循环心内直视手术个性化选择肝素化时间点提供客观依据。
1 资料与方法
1.1 资料
1.1.1 研究对象 选取2013年1月至2016年1月本院收治的体外循环心脏手术患者200例,通过分层随机化分为开胸前组(99例,手术切皮前肝素化)和开胸后组(101例,开胸后完成创面止血再肝素化)。
1.1.2 纳入标准 (1)诊断明确的非发绀型先天性心脏病或风湿性心脏瓣膜病;(2)术前心功能纽约心脏病协会分级:先天性心脏病患者心功能Ⅰ~Ⅱ级,风湿性心瓣膜病患者心功能Ⅱ~Ⅲ级;(3)术前凝血功能、肝肾功能均正常;(4)近2周内未应用影响凝血功能的药物;(5)无感染性及血液疾病史。
1.1.3 排除标准 (1)术中大血管损伤及其他大出血情况;(2)急诊手术;(3)所用肝素非同一生产厂家的病例;(4)术中发生心室颤动、停机困难等事件。
1.2 方法
1.2.1 手术方法 2组患者均采用全身麻醉气管插管复合麻醉,胸部正中切口体外循环心脏停搏下完成心内手术。全身肝素化采取颈静脉注射肝素3~4 mg/kg,体外循环期间维持全血激活凝固时间480 s,停机后给予鱼精蛋白3~6 mg/kg中和肝素。术中止血纱布均进行使用前后称重,并禁止使用盐水纱布及创面负压吸引,通过术中止血纱布增重统计创面出血量。
1.2.2 观察指标
1.2.2.1 术前基础指标 包括患者性别、年龄、体重、疾病名称、手术时间、既往病史、纽约心功能分级、血常规、肝肾功能、凝血功能等。
1.2.2.2 手术情况 包括手术方式、肝素化时机、手术关胸时间、转机时间、主动脉阻断时间、术中创面出血量、术后24 h引流量、术中及术后输血量等。
1.3 统计学处理 应用SPSS20.0统计软件进行数据分析,计量资料以表示,采用单因素方差分析;计数资料以率或构成比表示,采用χ2检验或确切概率法;变量呈偏态分布采用非参数检验,采用Mann-WhitneyU检验。检验水准:α=0.05。P<0.05为差异有统计学意义。
2 结 果
2.1 2组患者术前一般情况及手术指标比较 200例患者中男83例,女117例;行先天性心脏病手术98例,其中房间隔缺损修补术40例,室间隔缺损修补术58例;行心脏瓣膜手术102例,其中二尖瓣置换术41例,主动脉瓣置换术20例,二尖瓣、主动脉瓣联合瓣膜置换术41例。2组患者术前基础指标、手术方式、体外循环时间、主动脉阻断时间比较,差异均无统计学意义(P>0.05)。见表 1。

表1 2组患者术前一般情况及手术指标比较

续表1 2组患者术前一般情况及手术指标比较
2.2 2组患者术后临床结果比较 2组患者均顺利完成手术,术中均未发生组织、血管意外损伤事件。2组患者除术中及术后输血量、术后24 h引流量比较,差异均无统计学意义(P>0.05),开胸后组患者手术关胸时间、肝素及鱼精蛋白用量、术中创面出血量、术后切口感染率、术后血红蛋白降低值均明显低于开胸前组,差异均有统计学意义(P<0.05)。见表 2。
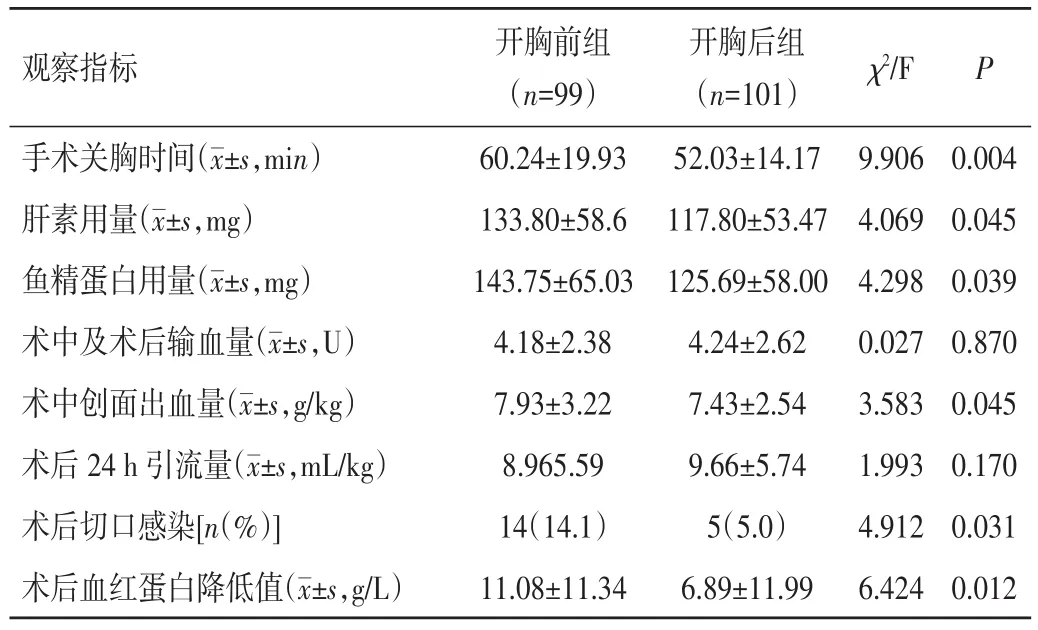
表2 2组患者术后临床结果比较
3 讨 论
3.1 不同肝素化时机的临床结果 肝素化是体外循环心内直视手术的必要环节。临床进行全身肝素化通常为2个时间点:(1)手术开始前全身肝素化;(2)开胸先完成术区创面止血后肝素化。全身肝素化抗凝后,可防止体外循环栓塞风险,同时,也会影响术中止血。即使体外循环停机后,鱼精蛋白也只能中和90%的肝素。因此,过多剂量的肝素使用会加重对术中凝血功能的干扰,增加止血难度。本研究结果显示,开胸止血后全身肝素化更有利于手术止血,缩短手术关胸时间,减少术区创面渗血。尽管本研究结果显示,2组患者术中输血量比较,差异无统计学意义(P>0.05),然而开胸后组患者术后血红蛋白降低程度明显低于开胸前组。因此,采取开胸后肝素化的策略可节约手术用血。切口创面渗血、长时间暴露、电凝刀的频繁使用均可增加切口感染发生率[3-4]。鱼精蛋白中和肝素形成的鱼精蛋白-肝素复合物可诱发机体炎性反应;而减少该复合物的生成量则可有效减少对组织的感染和器官的损害[5]。采取开胸止血后肝素化可减少上述风险因素。本研究结果也证实,开胸后组患者切口感染发生率明显低于开胸前组。采取开胸后肝素化可减少体外循环期间全身肝素化的抗凝时间,尤其是体外循环时间较长的患者,可减少术中肝素维持量。饶效等[6]发现,在满足体外循环肝素化需求下采用较低剂量肝素可减轻患者凝血功能紊乱,并减少术中输血量。由于术中输血可增加心脏术后急性肺损伤、心肌梗死、脓毒血症及切口感染等术后并发症发生率,而减少心脏外科手术用血则可降低术后并发症发生率[7]。NILSSON等[2]也发现,在体外循环冠状动脉搭桥术中应用小剂量肝素,可缩短患者气管带管呼吸机辅助及重症监护时间,更有利于患者康复。
3.2 体外循环肝素化时机的选择 体外循环心脏手术一直是外科中的“用血大户”[8]。近年来,血液紧张已逐渐成为常态化趋势[9-10],已影响了心脏外科手术的正常开展。因此,如何节约用血,已成为新的临床研究热点。在体外循环手术中肝素及鱼精蛋白过量使用均可增加术中失血量,肝素反弹也可导致更多的术后引流,并延长患者在重症监护病房的住院时间[11-12]。尽管肝素的应用仍是一把“双刃剑”,肝素不足可导致栓塞事件的发生。但目前有研究表明,在国内,体外循环肝素化发生出血的不良事件仍明显多于栓塞[13]。因此,最佳的肝素化方案应使肝素用量相对较少,以保证体外循环安全。本研究结果显示,采取开胸止血后肝素化具有节约用血、减少肝素用量及降低术后切口感染率等优点。然而因全身肝素化及全血激活凝固时间检查的耽搁,开胸后再肝素化却不利于危急患者的紧急抢救。因此,对择期体外循环手术患者可推荐采取开胸后肝素化的方式建立体外循环,而对危急心脏手术患者则可采取术前肝素化,以便更快地回收术中出血及建立体外循环。
3.3 本研究的局限性 本研究纳入过多病种,受样本量限制未能进行分层分析。本研究虽为前瞻性研究,但仍存在一定的选择偏移。因此,需更大样本量的单病因随机临床对照试验进一步验证。
综上所述,择期体外循环心脏手术采取开胸止血后肝素化的策略更有利于术中止血,具有缩短手术时间、降低术后切口感染率、节约手术用血等优点,值得临床推荐。

