猪伪狂犬病病毒TaqMan荧光定量PCR检测方法的建立及应用
李晓菲,陈 婷,魏笑笑,孙爱荣,秦立廷
(山东新希望六和集团有限公司,山东 青岛 266000)
猪伪狂犬病(Pseudorabies,PR)是由猪伪狂犬病病毒(Pseudorabies virus,PRV)引起的一种猪的烈性传染病。PRV可感染各个年龄段的猪,临床症状主要表现为种猪不育、仔猪高死亡率以及妊娠母猪流产、死胎、木乃伊胎。随着PRV变异毒株的出现以及近年来养猪业的快速发展,我国PR的发生与流行日益增多,目前许多规模化养殖场的PRV野毒实验室检测结果呈阳性,其他中小规模养殖场以及个体户养殖场的野毒感染情况更加严重,从而给该病的防治带来很大的困难。因此对PRV野毒感染尤其是感染早期的快速、准确诊断对PRV的种群净化以及PR的防控具有重要意义。
gE基因是OIE规定的伪狂犬基因缺失苗的缺失基因,因此基于gE基因建立相应的鉴别诊断方法可以区分PRV野毒和疫苗毒。本研究旨在gE基因序列上设计引物与探针,建立一种可区分PRV基因缺失疫苗株和野毒感染的荧光定量检测方法,为PRV感染初期的快速准确诊断及其流行病学调查提供可靠的技术工具。
1 材料与方法
1.1 病毒与临床样品来源 猪瘟病毒(CSFV),猪流行性腹泻病毒(PEDV),猪传染性胃肠炎病毒(TGEV),猪轮状病毒(RV),猪繁殖与呼吸综合征病毒(PRRSV),猪细小病毒(PPV)、猪伪狂病病毒(PRV)和猪圆环病毒2型(PCV2)等由新希望六和动保中心青岛中心实验室保存。疑似PRV感染病料,由新希望六和动保中心青岛中心实验室在山东、河北等地的养猪场收集。
1.2 仪器与试剂 荧光定量PCR仪、分光光度计、核酸提取试剂盒、胶回收试剂盒、质粒提取试剂盒、PCR酶、Premix Ex Taq(Probe qPCR)等。
1.3 引物探针设计与合成 通过对多个PRV毒株gE基因序列进行比较分析,在其保守区域设计特异性引物和Taq-Man探针。上、下游引物序列分别为Primer F:5'CGGCTTCGACGTCTGGTT 3'和 Primer R: 5' GCCATAGTTGGGTCCATTCG 3'。探针序列为5'FAM-CCGGAGAAACCGGAAG-MGB 3',其中5'端标记 FAM,3'端标记MGB。
1.4 标准品制备 将PRV gE目的基因进行PCR扩增,然后将目的片段回收纯化,与pMD19-T载体连接后进行转化,提取质粒,经鉴定为阳性的质粒即为质粒标准品。将标准品浓度换算成拷贝数,-20℃保存备用。
1.5 反应条件优化 首先通过温度梯度PCR确定引物的最适退火温度,然后用矩阵法对探针和引物的用量进行摸索与改进,最终获得最适合的探针引物浓度配比,确定反应体系。
1.6 标准曲线的建立 将1.4中制备的标准品进行10倍连续倍比稀释,稀释后对9.2×101~9.2×109copiesμL-1浓度范围的标准品进行荧光定量PCR反应,获得标准曲线。
1.7 特异性试验 利用建立的荧光定量方法对CSFV,PEDV,TGEV,RV和PRRSV的cDNA以及PPV和PCV2的DNA进行检测验证该方法的特异性。
1.8 敏感性试验 将阳性DNA进行连续10倍倍比稀释至最低浓度为1.12×101copiesμL-1,进行荧光定量PCR反应。同时以该DNA为模板,进行常规PCR反应,比较两种检测方法的敏感性。
1.9 重复性试验 用5种浓度的标准品质粒分别进行4次批内和批间的重复性试验并且根据Ct值计算变异系数。
1.10 对临床样品的检测 由本实验室收集可疑PRV临床样品60份,分别进行荧光定量PCR检测和常规PCR检测,比较分析结果。
2 结 果
2.1 质粒标准品的制备 通过常规PCR扩增PRVgE目的基因,将扩增的目的片段纯化后与pMD19-T载体连接,转化后提取质粒,经鉴定为阳性的质粒即为荧光定量标准品。测定标准品浓度,换算成拷贝数为9.2×109copiesμL-1,-20℃保存备用。
2.2 反应条件优化 荧光定量PCR反应体系共为25μL,含 12.5μL 2 ×PremixExTaq (ProbeqPCR),10μL RNase-free water,0.5μL Probe (10μM),0.5μL Primer F(10μM),0.5μL Primer R(10μM),质粒标准品 1μL。反应条件为:95℃5min;94℃15sec,55℃35sec,40 个循环。
2.3 荧光定量PCR标准曲线的建立 用荧光PCR仪对9.2×101~9.2×109copiesμL-1的标准品进行荧光定量PCR反应,获得标准曲线。由图1和图2可知,线性关系良好,标准曲线建立成功,可用于临床样品的检测。
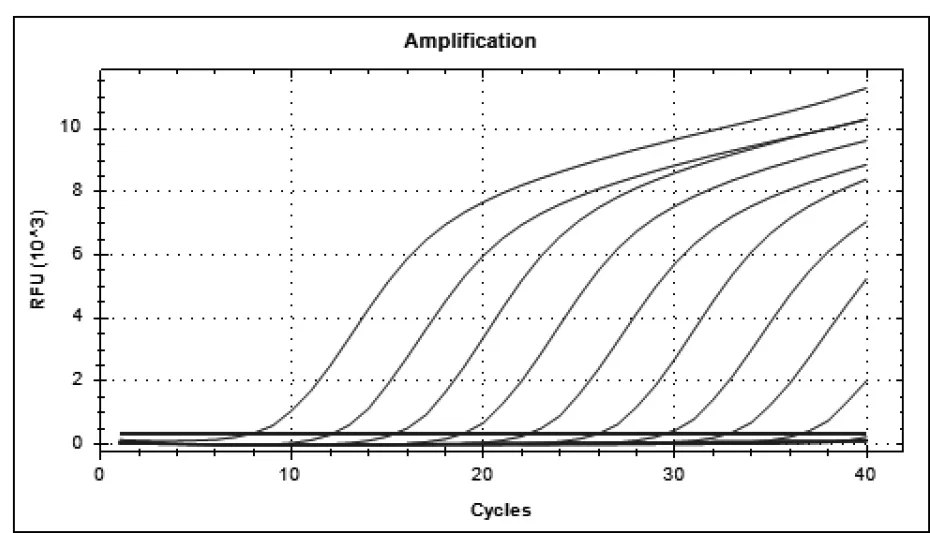
图1 PRV荧光定量PCR动力学曲线
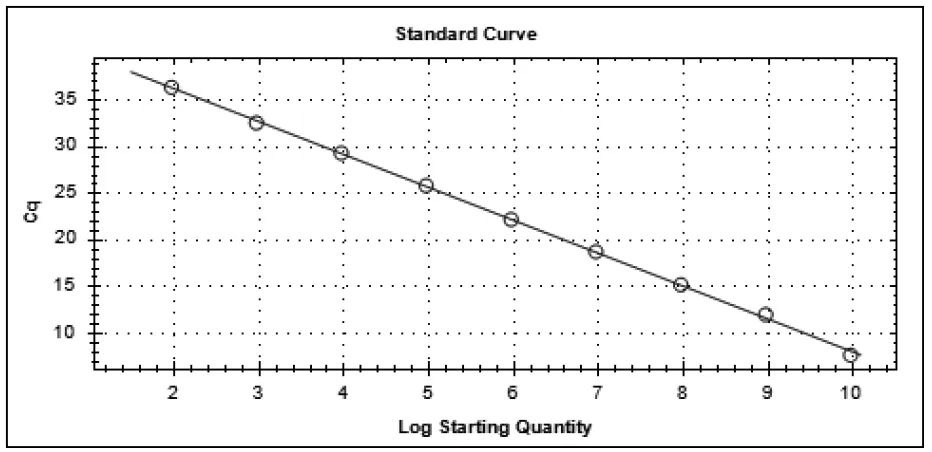
图2 PRV荧光定量PCR标准曲线
2.4 特异性试验 用所建立的荧光定量PCR方法对CSFV,PRRSV,PEDV,TGEV,RV,PPV和 PCV2等病毒的 cDNA或者DNA的检测结果均为阴性,说明该方法与这些猪病病毒无交叉反应(图3),试验结果表明该方法具有良好的特异性。
2.5 敏感性试验 荧光定量PCR方法能检出的DNA模板最低浓度为9.2×101copiesμL-(1图1),而常规PCR能检出的模板最低浓度为1.12×104copiesμL-(1图4),试验结果表明所建立的荧光定量PCR方法的敏感性是常规PCR方法的100倍左右。
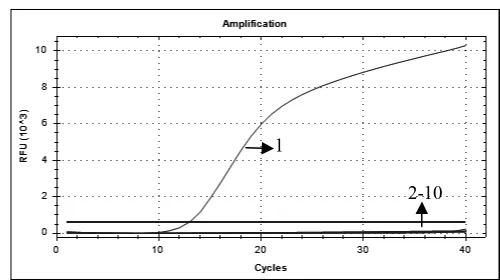
图3 PRV荧光定量PCR特异性试验
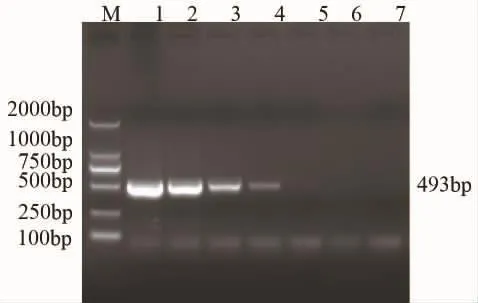
图4 PRV常规PCR敏感性试验结果
2.6 重复性试验 用5种不同浓度的标准品分别进行批内和批间重复性试验。试验结果表明,批内和批间重复性试验的变异系数均小于1.5%(表1),表明该方法具有良好的重复性与稳定性。
2.7 临床样品检测结果 对本实验室收集的可疑PRV临床样品60份,分别进行荧光定量PCR和常规PCR检测。检测结果表明,荧光定量PCR方法阳性检出率(58.3%)比常规PCR方法(46.7%)更高(表2)。对临床样品的检测结果表明荧光定量方法具有更高的敏感性,更适用于PRV野毒的临床检测,尤其是感染早期病毒含量较低时。
3 讨论
PR是由PRV感染家畜或野生动物引起的一种急性传染病,临床症状主要表现为发热、奇痒、呼吸系统和神经系统症状。从2011年开始,由PRV变异株引起的PR疫情在我国多个省份相继暴发,给我国养猪业造成了严重的经济损失。因此对PRV野毒感染尤其是病毒感染早期的及时、准确诊断对PR的防控具有重要意义。
荧光定量PCR在常规PCR基础上引入了荧光探针,使得检测方法具有更高的特异性和敏感性,并且PCR结束后可以直接观察结果,无需进一步凝胶电泳,同时也降低了开盖点样造成污染的可能性。荧光定量PCR整个过程操作简单,用时短,最快可以在2h内得到检测结果,已经越来越多的被应用于病原检测领域。本研究根据GenBank中PRV gE基因序列设计特异性引物和TaqMan探针,建立了一种可区分PRV野毒株及基因缺失疫苗株的荧光定量PCR方法。通过对反应条件的优化,使得该方法在 9.2×101~9.2×109copiesμL-1模板范围内具有良好的线性关系,灵敏度达到9.2×101copiesμL-1,是常规PCR方法的100倍。与常规PCR方法相比,该方法对临床样品的检出率更高。
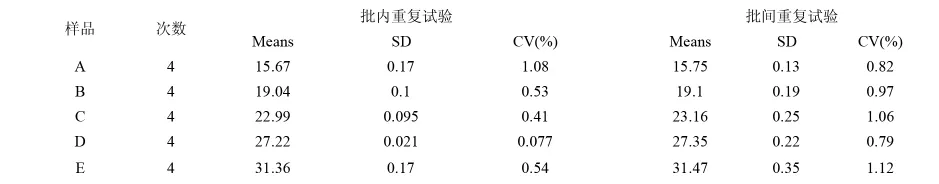
表1 PRV荧光定量PCR重复性试验

表2 临床样品检测结果
综上所述,本研究所建立的区分PRV野毒株及基因缺失疫苗株的荧光定量PCR方法为PRV感染的早期诊断及其流行病学调查提供了快速、简便和可靠的技术工具。

