改性羧甲基壳聚糖复合材料的制备、表征与研究
董丽丹, 魏长平, 李中田, 汪凤明
(1. 长春理工大学 材料科学与工程学院, 吉林 长春 130022;2. 长春医学高等专科学校, 吉林 长春 130031; 3. 中水东北勘测设计研究有限责任公司, 吉林 长春 130061)
1 引 言
随着医学技术的发展,应用医用可吸收止血材料处理伤口受到科研人员和医务工作者的广泛关注,世界范围内,可吸收止血材料逐渐成为医疗和制药行业发展的热门方向[1-4]。壳聚糖因具有抗菌、止血和良好的组织相容性,且其凝血过程不依赖凝血系统等性能而被广泛作为止血材料[5-8]。
近年来通过复合一些具有止血、消炎、抗菌效果的药物或离子来提高壳聚糖及其衍生物类止血材料的止血效果研究见诸文献。尹刚等[9]通过剂型改造和结构改变向壳聚糖中加入Ca2+及Zn2+,研制出一种新型壳聚糖止血粉,通过凝血、止血实验,证明了这种新型止血粉剂是一种有效、安全、可降解的生物止血材料。羧甲基化的壳聚糖较单纯的壳聚糖具有更好的水溶性、生物可降解性等优点,且无细胞毒性作用,可促进细胞生长,其止血作用比之壳聚糖更加优秀[10-13]。Ag+能通过缓释技术使微生物蛋白质结构遭到破坏,造成微生物死亡或使其产生功能性障碍,从而达到抗菌效果[14]。TiO2具有广谱长效抗菌、屏蔽紫外线等优点,目前已被国家批准为食品添加剂[15]。
本文首先在壳聚糖分子结构中引入羧甲基,得到的羧甲基壳聚糖再与硝酸银和纳米二氧化钛溶液充分反应,得到羧甲基壳聚糖复合止血材料。采用 FTIR、XRD、SEM等手段对复合材料的结构进行表征并考察了其凝血、止血性能。实验结果表明,羧甲基壳聚糖络合了Ag+和纳米TiO2生成了新的复合物,且较羧甲基壳聚糖具有更好的止血性能。
2 实 验
2.1 样品制备
羧甲基壳聚糖:向三口烧瓶中加入一定量的脱乙酰度为80.0~95.0壳聚糖和分析纯的异丙醇,搅拌。加入30%NaOH溶液,将6 g分析纯氯乙酸分4次加入溶液中,加热反应3 h,加入蒸馏水,调pH为7.0。抽滤,用70%甲醇、95%乙醇、无水乙醇洗涤。所得产品放入烘箱烘干,即得羧甲基壳聚糖。
羧甲基壳聚糖银:称取一定量羧甲基壳聚糖溶入蒸馏水中,再加入0.10 mol/L 的AgNO3溶液,加热搅拌2 h。所得产品放入鼓风干燥箱中干燥,研磨成粉。
羧甲基壳聚糖吸附纳米TiO2:首先进行纳米TiO2粉体改性。称取一定量分析纯纳米TiO2加入到70 mL水中,调pH为5.0,加入月桂酸钠,反应30 min,干燥,得白色纳米TiO2粉体,研磨成粉,备用。称取微量改性纳米TiO2溶于蒸馏水中,搅拌,再加入一定量羧甲基壳聚糖,搅拌3 h,烘干,研磨成粉。
羧甲基壳聚糖银吸附纳米TiO2复合材料:称取少量改性纳米TiO2溶于蒸馏水中,搅拌,分别加入一定量羧甲基壳聚糖和0.10 mol/L的AgNO3溶液,搅拌,制得Ag+-TiO2-CMCS混合液,洗涤后,干燥10 h,得到成品。
2.2 样品分析与性能测试
羧甲基壳聚糖取代度的测定:测定羧甲基壳聚糖的取代度,采用的方法是电位滴定法。具体步骤:将0.2 g羧甲基壳聚糖样品溶于20 mL浓度为0.1 mol/L的HCl标准溶液中,用0.1 mol/L的NaOH标准溶液进行缓慢滴定,用pH计观察pH值的变化情况,分别记下pH值是2.1和4.3时所消耗的NaOH标准溶液的体积V1和V2,通过公式(1)、(2)计算羧甲基壳聚糖取代度(KDS):
KDS=0.161A/(1-0.058A) ,
(1)
A=(V1-V2)M,
(2)
式中:A代表每克样品中羧甲基的物质的量,mmol;0.161是每个乙酸氨基葡萄糖残基的物质的量,mmol;0.058是每毫克当量的羧甲基质量;M代表NaOH标准溶液的浓度;W代表样品的净重。
红外光谱(FT-IR):在傅里叶变换红外光谱仪上,使用KRS-5型ATR探头,用反射法在500~4 000 cm-1波数范围内扫描,并记录各样品的红外光谱。
射线衍射光谱(XRD):室温下使用Rigaku D/MAX-RB型X射线衍射仪记录样品的X射线衍射图谱。X射线源为Cu-Kα线,电压为40 kV,电流为50 mA,扫描范围为10°~80°,扫描速度为10(°)/min。
扫描电镜(SEM):为了更明显地看见混合了金属离子,所以将其铺成膜。用Quanta-200扫描电镜观察膜表面。
样品的凝血、止血性能测试:为了测试实验样品的凝血和止血性能,本文建立了动物实验模型,选用体重在18~26 g之间的成年雄性昆明鼠,进行样品的体外凝血和止血实验。
3 实验结果与讨论
3.1 样品结构测试分析
3.1.1 羧甲基壳聚糖取代度的测定
根据取代度的测定方法,在本文实验条件下,制得的羧甲基壳聚糖的取代度为1.43。
3.1.2 样品的红外光谱分析
壳聚糖和羧甲基壳聚糖的红外光谱如图1所示。由图像分析可知,CS:波数3 423 cm-1处属于N—H键伸缩振动吸收峰,2 876 cm-1是—CH—键对称伸缩振动吸收峰,1 596 cm-1处是—COO键不对称伸缩振动吸收带,1 380 cm-1处是C—H键对称变形振动和弯曲振动吸收带,1 080 cm-1处吸收峰很宽,是C—O键吸收带。CMCS:波数3 386 cm-1处是N—H键伸缩振动吸收峰,2 918 cm-1处是—CH—键不对称伸缩振动吸收峰,1 593 cm-1处是酰胺Ⅱ吸收峰,1 413 cm-1处有两个吸收峰,故判断为羰基对称伸缩振动吸收峰,1 072 cm-1处为醚键C—O—C吸收峰。由于图像在3 423 cm-1和1 380 cm-1处吸收峰发生了明显的偏移,说明取代反应分别发生在N位、O位上,所得产物为N,O-羧甲基壳聚糖。
CMCS复合Ag+、纳米TiO2红外光谱如图2所示。从图中可看出,随着Ag+和TiO2的加入,CMCS于3 386 cm-1处羟基和胺基的伸缩振动吸收宽峰发生了波数移动,这表明Ag+、TiO2和CMCS间有较强的氢键相互作用;此外,CMCS复合物在1 072 cm-1处羟基伸缩振动吸收峰移至低波数1 062 cm-1,这进一步证明了Ag+、TiO2和CMCS间存在较强的氢键相互作用。
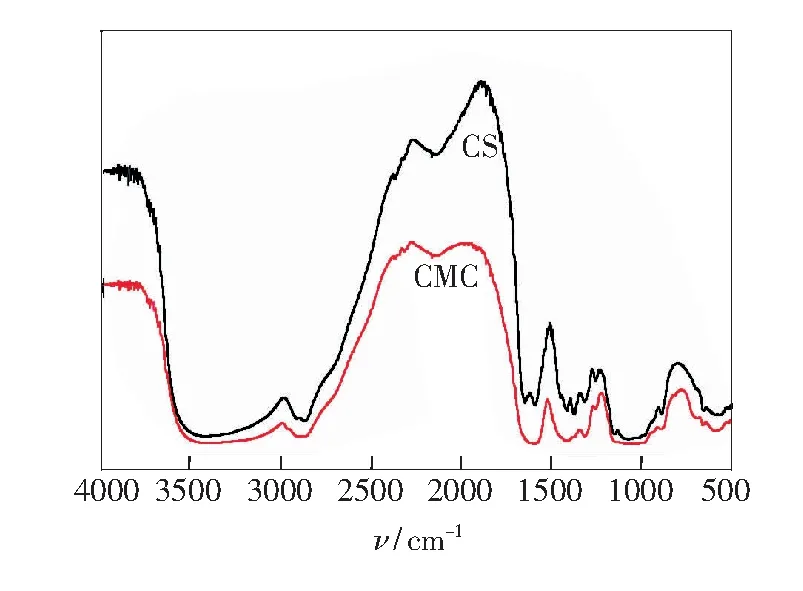
图1 CS和CMCS的红外光谱图
Fig.1 FT-IR spectra of chitosan and carboxymethyl chitosan
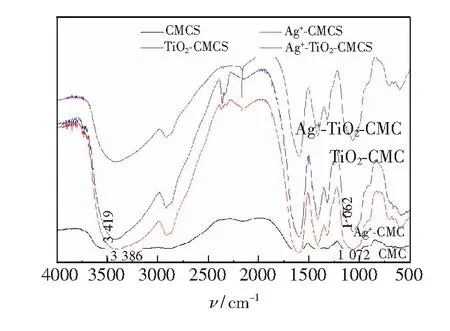
图2 CMCS复合Ag+、TiO2的红外光谱图。
Fig.2 FT-IR spectra of carboxymethyl chitosan composite Ag+, TiO2.
3.1.3 样品的射线衍射分析
CS和CMCS的XRD如图3所示。研究表明,壳聚糖X射线衍射图谱峰的强度与其结晶性有关,结晶性越强则峰的强度也越强;反之,峰的强度则减弱。壳聚糖结构单元引入羧甲基后削弱了2、6位羟基与3位羟基的氢键作用,使壳聚糖的结晶性减弱,因而峰的强度减小。
CMCS复合Ag+、纳米TiO2的XRD如图4所示。羧甲基壳聚糖在2θ=19.56°处出现衍射吸收峰,可以看出CMCS是非晶态的。当CMCS复合Ag+时,其2θ=27.42°,36.11°,54.22°,67°处出现衍射峰,这些衍射峰与 JCDPS卡片上立方晶系银的衍射峰基本一致,分别对应标准晶态银卡片上的(111)、(200)、(220)、(311)晶面,说明成功复合了银离子。当CMCS复合纳米TiO2时,在44.34°处出现特征衍射峰,表明CMCS复合了纳米TiO2。

图3 CS和CMCS的XRD图
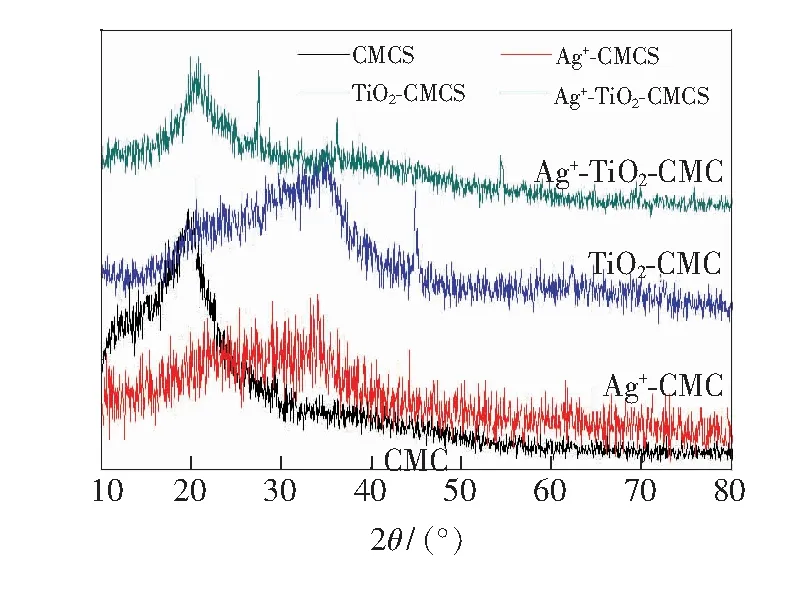
图4 CMCS复合Ag+、TiO2的XRD图。
Fig.4 XRD patterns of carboxymethyl chitosan composite Ag+, TiO2.
3.1.4 样品的扫描电镜分析
羧甲基壳聚糖复合Ag+、TiO2的扫描电镜图如图5所示,(a)、(b)、(c)分别为Ag+-CMCS、TiO2-CMCS、Ag+-TiO2-CMCS的SEM图片。
通过图片可以看出CMCS的粒径为14.8 nm左右,Ag+粒径为143.5 nm左右,纳米TiO2的粒径为267.2 nm左右。Ag+和纳米TiO2负载在CMCS的表面和内部,3种物质分布均匀。

图5 Ag+-CMCS(a)、TiO2-CMCS(b)和Ag+-TiO2-CMCS(c)的扫描电镜图。
Fig.5 SEM micrographs of Ag+-CMCS(a), TiO2-CMCS(b) and Ag+-TiO2-CMCS(c), respectively.
3.2 样品性能测试分析
3.2.1 凝血测试分析
样品的凝血性能测试方法:向每个试管中加入1 mL浓度为 0.10 mol/L草酸钾溶液作为抗凝剂备用。取全血5 mL分别放入5个试管中,按每毫升血液加入0.2 g样品粉末,每隔数秒倾斜试管,发现血液凝集立即记录时间,每个样品测试3组平行数据,取平均值,结果见表1。
由凝血测试时间可知,CMCS 的凝血时间要好于CS,这是由于CMCS的氨基具有活性,发生质子化生成阳离子,进而吸引带有负电荷的血小板和红细胞,另外,氨基的亲水性能会增加血纤蛋白原吸附的数量,加速凝血过程从而缩短了凝血时间。Ag+-TiO2-CMCS的凝血效果要优于Ag+-CMCS和TiO2-CMCS的凝血效果,同时Ag+-CMCS和TiO2-CMCS的凝血效果要好于CS和CMCS的凝血效果。
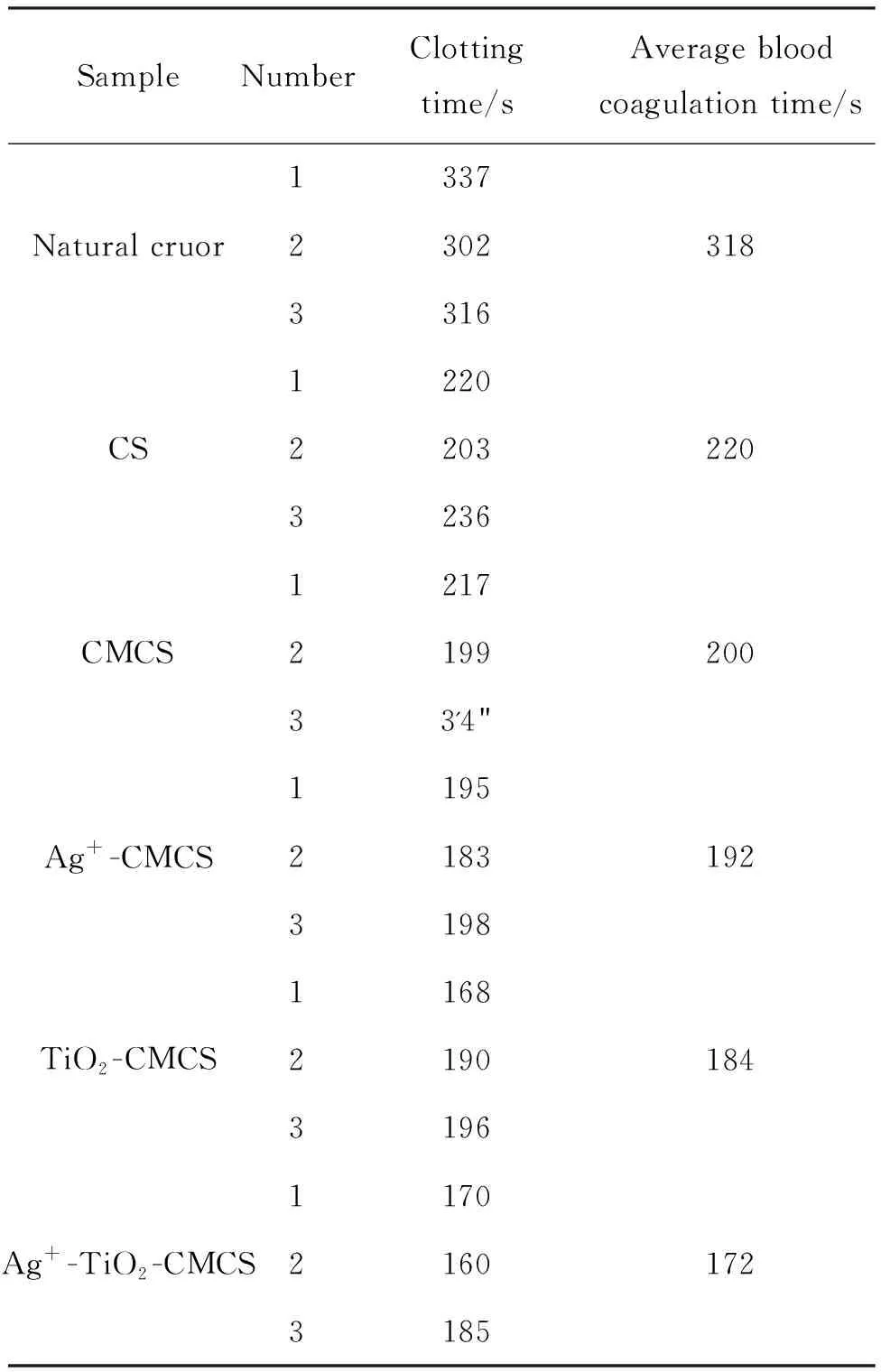
表1 样品的凝血时间测试
3.2.2 止血测试分析
样品的止血性能测试方法:将小鼠放进离心管中使其头部固定,于尾尖3 cm处切断,制造出血创面。空白对照实验使尾尖在自然状态下止血,从切断尾尖开始,到不再有血滴渗出,记录止血时间,分别测试3组平行数据,计算平均值;另外5组样品,在切断小鼠尾尖后,取0.2 g样品均匀涂抹于伤口,使尾部保持自然状态不动,使伤口与样品始终接触,从切断尾尖开始,直到不再出血为止,记录止血时间,5个样品分别测试3组平行数据,计算平均值,结果见表2。

表2 样品的止血时间测试
从平均止血时间来看,Ag+-TiO2-CMCS的止血效果要优于Ag+-CMCS和TiO2-CMCS的止血效果,同时Ag+-CMCS和TiO2-CMCS的止血效果要好于CS和CMCS的止血效果。
4 结 论
壳聚糖经羧甲基化制得羧甲基壳聚糖,向其中加入Ag+和纳米TiO2制得羧甲基壳聚糖复合止血材料。
羧甲基壳聚糖复合物的结构表征数据表明:添加了Ag+和纳米TiO2的羧甲基壳聚糖其IR图谱显示,在3 386 cm-1和1 062 cm-1处吸收峰发生了位移,XRD图谱表现出相应的晶行行态,以上说明Ag+和纳米TiO2与羧甲基壳聚糖进行了复合。SEM图像可以更直观地看出:CMCS的粒径为14.8 nm左右,Ag+粒径为143.5 nm左右,TiO2的粒径为267.2 nm左右,Ag+和纳米TiO2负载在CMCS的表面和内部,3种物质分布均匀。
复合物的凝止血测试数据表明:添加了Ag+和纳米TiO2的羧甲基壳聚糖可以有效地缩短凝血和止血时间。其中单独添加Ag+和纳米TiO2制备的止血粉相比,添加纳米TiO2止血粉其止血效果要稍好于添加Ag+止血粉。同时添加Ag+和纳米TiO2止血粉,在复合效应作用下获得了更优的凝血和止血性能。

