甲巯咪唑脂质体的制备及其对大鼠T3 、T4及TSH值的影响
王晓慧,罗湘军,曾 燕
(1.邵阳学院 药学院,湖南 邵阳,422000; 2.邵阳学院 附属第二医院,湖南 邵阳,422000)
甲巯咪唑(thiamazole)能够抑制甲状腺激素的合成,是临床治疗甲状腺功能亢进症的一线药物,目前常用制剂是甲巯咪唑片剂。由于甲巯咪唑片剂生物半衰期短,药物口服剂量大,口服后血药浓度不平稳,部分患者会出现粒细胞下降,肝功能异常等严重不良反应[1]。近年来,脂质体作为药物载体系统能减少药物不良反应和具有良好的治疗靶向性、缓释性,使其得以迅速发展和广泛应用[2-3]。本实验通过以包封率为指标,应用逆向蒸发-超声法制备甲巯咪唑脂质体,同时对比考察了脂质体溶液剂和片剂对大鼠血清T3、T4、TSH影响,旨在获得一种高效低毒的新型制剂,为该药新剂型开发及临床应用提供参考。
1 仪器与试药
1.1 仪器
LC-2100C型高效液相色谱仪(日本岛津),旋转蒸发器RE-52AA(上海亚荣),Hitachi H-600透射电子显微镜(日本日立)。
1.2 试药
甲巯咪唑对照品(青岛捷世康生物科技有限公司);内标为邻苯二酚(分析纯,湖南师范大学);甲醇(色谱纯,北京普析科技有限公司);甲巯咪唑片(北京燕京制厂);大豆磷脂(西安凯新生物科技有限公司);胆固醇(美国Sigma);甲状腺素放射免疫分析药盒(北京原子高科股份有限公司);促甲状腺激素放射免疫分析药盒(北京原子高科股份有限公司);T3、T4及TSH质控血清(中国药品生物制品检定所)。
1.3 动物
Wistar大鼠雌雄各半,体重(200±10)g,由邵阳学院药学院动物实验中心提供。
2 方法
2.1 脂质体的制备
处方:磷脂0.20mol,胆固醇0.05mol,分别加入甲巯咪唑(0.08mol、0.04mol、0.02mol、0.01mol)磷酸缓冲盐溶液至100ml。
取处方量的磷脂、胆固醇加入氯仿40ml使其全部溶解后作为油相,置250ml磨口圆底烧瓶中,另取处方量甲巯咪唑超声溶解后作为水相。将水相成细流缓慢加入油相中,超声至形成W/O型乳液。将制得的乳置于35℃恒温水浴上,旋转蒸发除去氯仿得到半固体胶状物,再向半固体胶状物中倒入磷酸缓冲盐溶液至100ml,继续超声至形成乳白色混悬液,微孔滤膜(0.45μm)过滤,得到乳白色的甲巯咪唑脂质体。
2.2 色谱条件
色谱柱:Waters C18柱(319mm×150mm);流动相:甲醇∶水容积比(10∶90);流速:110ml·min-1;检测波长:266nm;灵敏度:0.2AUFS;纸速:0.25cm·min-1;进样量:20μl。
2.3 标准曲线的绘制
精密称取甲巯咪唑对照品及内标适量,分别加甲醇制成0.2mg·ml-1的对照品溶液和0.8mg·ml-1的内标溶液。精密量取对照品溶液0.25ml、0.5ml、1.0ml、2.0ml、3.0ml、4.0ml,分别置10ml容量瓶中,精密加入内标液5ml,用甲醇稀释至刻度,摇匀。按上述色谱条件分别进行测定,以对照品与内标的峰面积比值(Y)为纵坐标,甲巯咪唑的浓度(X)为横坐标,进行线性回归。
2.4 回收率试验
按2.3的操作方法,取1.0ml空白于10ml容量瓶中,分别加入制成0.2mg·ml-1的对照品溶液和0.8mg·ml-1的内标溶液,配制低、中、高质量浓度的甲巯咪唑生理盐水溶液,按照给定的色谱条件,每个浓度重复测定3次,计算回收率均值。
2.5 精密度试验
按2.3的操作方法,低、中、高质量浓度的甲巯咪唑生理盐水溶液,按照给定的色谱条件,重复进样6次,测定甲巯咪唑浓度,计算RSD。
2.6 包封率测定
将5ml甲巯咪唑脂质体样品悬液于4℃、100000r·min-1条件下离心2h。准确测量上清体积,采用HLP法测定甲巯咪唑含量(即为游离药物浓度)。包封率计算公式:包封率/%=(1-游离药物浓度/全药浓度)×100%。
2.7 粒径分析
将甲巯咪唑脂质体稀释至一定浓度后安放于PCS检测槽中,对脂质体粒径进行测定。
2.8 透射电镜观察
取甲巯咪唑脂质体悬液加入到四氧化锇磷酸盐缓冲液中(体积比2∶1,固定30分钟后,取少量滴于铜网上,3%磷钨酸钠溶液负染后,透射电镜观察脂质体的形态。
2.9 血清T3、T4及TSH测定
2.9.1 试验分组
大鼠随机分为2组,每组9只:①甲巯咪唑脂质体溶液(A组);②甲巯咪唑片剂(B组)。每组大鼠每日给药1次,每次给药剂量为0.2mg·kg-1、0.3mg·kg-1、0.35mg·kg-1(按人有效剂量折算),连续给药8周,股动脉取血4ml,分离血清,测定大鼠血清T3、T4及TSH值,共3次。
2.9.2 T3、T4测定(由邵阳学院附属第二医院检验科提供)
取试管加血清50μl,加抗体200μl,加抗原200μl,37℃温育45min,加DP2R分离剂500μl,以4000r·min-1离心20min,测定放射性计数率。
2.9.3 TSH测定(由邵阳学院附属第二医院检验科提供)
取抗体包被管加静脉血清200μl,加标记物125 I2Ab 200μl,混匀,37℃温育过夜,弃上清液,加1.0ml洗涤液,摇匀,放置2min,弃上清液,重复洗涤1次,测定各包被管放射性计数。
3 结果
3.1 标准曲线的绘制
按2.3色谱条件分别进行测定,色谱图见图1。回归方程为:Y=0.0257X-0.0060,r=0.9998。实验结果表明,甲巯咪唑浓度在10~80μg·ml-1范围内,与对照品和内标的峰面积比值呈良好的线性关系。
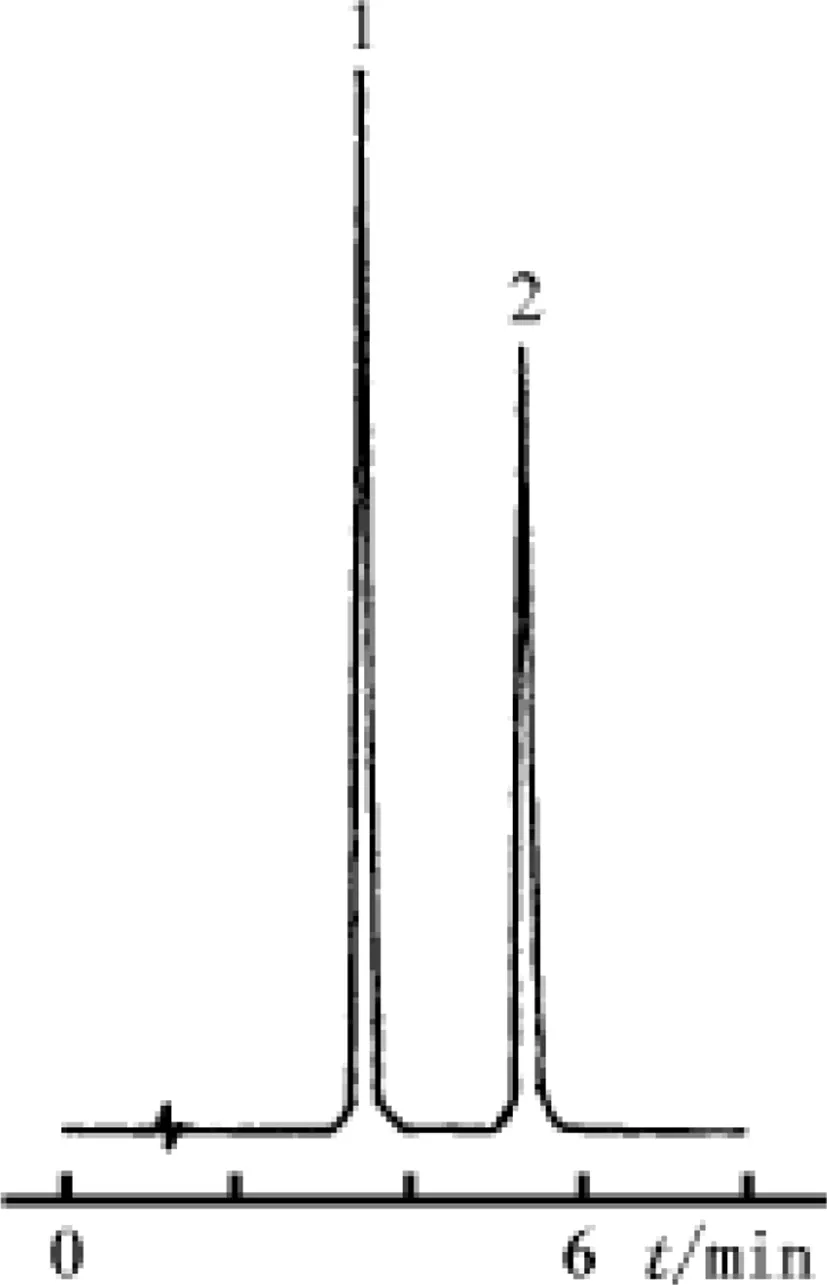
1 甲巯咪唑脂质体;2 内标图1 色谱图Fig.1 Chromatogram
3.2 回收率试验
按2.4项下测定并计算回收率均值为100.3%(n=69),RSD为0.55%。
3.3 精密度试验
按2.5项下计算RSD为0.3%。
3.4 包封率测定
在磷脂、胆固醇和甲巯咪唑摩尔浓度比为25∶6、25∶3、25∶2、25∶1时,分别制备相应的脂质体,测定其包封率,结果见表1。
3.5 粒径分析
甲巯咪唑脂质体经激光粒度仪测定,结果显示,颗粒平均粒为150±15nm,多分散系数(PI)小于0.18,见表1,说明粒径分布均匀。
表1 甲巯咪唑脂质体的考察指标结果
Table 1 Results of the investigation of methimazole liposomes
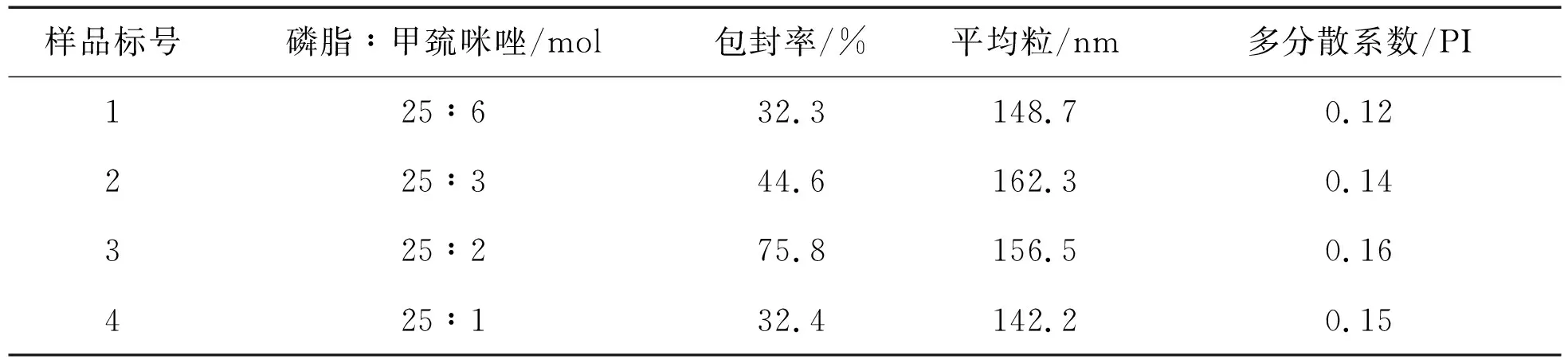
样品标号磷脂∶甲巯咪唑/mol包封率/%平均粒/nm多分散系数/PI125∶632.3148.70.12225∶344.6162.30.14325∶275.8156.50.16425∶132.4142.20.15
3.6 透射电镜观察
电镜下观察甲巯咪唑脂质体形态成圆球形,且为单层脂质体,分布均匀,见图2。
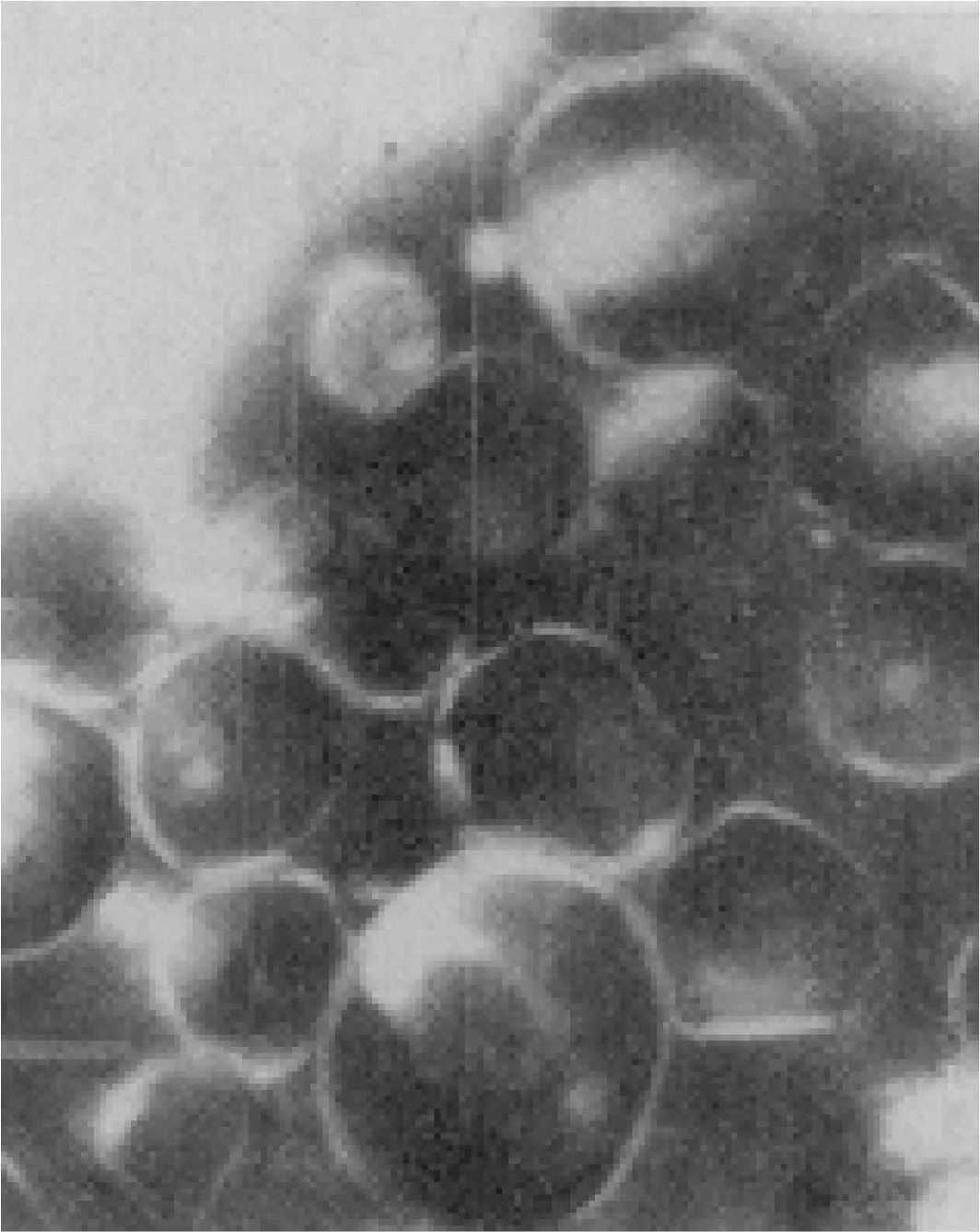
图2 脂质体透射电镜图(×30000)Fig.2 The TEM figure of lipidosome
3.7 血清T3、T4及TSH测定结果
甲巯咪唑不同给药途径对大鼠血清T3、T4及TSH值的影响,见表2。
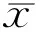

组别T3/(mol·L-1)T4/(nmol·L-1)TSH/(mU·L-1)A组0.362±0.12512.016±0.34510.217±0.1111B组0.581±0.12943.147±0.62170.202±0.1052
A组与B组比较,A组对大鼠血清T3、T4有显著抑制作用,P<0.05;对TSH的影响,两组间无显著性差异,P>0.05。
4 讨论
脂质体的制备方法多种多样[4-7],常用是薄膜分散法,还有逆向蒸发法、化学梯度法、冷冻干燥法等。本研究采用逆向蒸发-超声法在磷脂和甲巯咪唑摩尔浓度比为25∶2时,制备的脂质体,其包封率可以达到82.2%,此法不失为一种有效、快速和经济的方法。
口服甲巯咪唑脂质体组和片剂组比较,其药效显著高于口服片剂组。这可能是由于脂质体作为一种定向药物载体,属于靶向给药系统,能使药物靶向定位于特定的组织,使药物具有良好的靶向性、选择性和通透性[8],从而可减少用药的总剂量,降低药物的不良反应。
综上所述,逆向蒸发-超声法制备的甲巯咪唑脂质体具有明显提高药物活性、治疗效果和降低药物毒性的作用,值得在临床上推广。但脂质体制剂仍然因存在热稳定性差、以及制备成本高等因素的影响而制约其在临床上的应用[9]。但此次研究结果,为进一步筛选、优化流程,从而制备安全、稳定、副作用小和高效的甲巯咪唑脂质体应用制剂提高了有效的方法。

