一种EDTA—Fe合成方法的研究
(1.四川泸天化股份有限公司,四川泸州,646300; 2.四川煤气化有限责任公司,四川泸州,646300)
1 研究背景
铁是植物生长所需的7种微量元素之一,是治愈植物小叶、黄叶病症的主要制剂。传统上施用的无机盐类,不仅由于其性质的不稳定而造成使用效能低下,更为重要的是其对土壤具有破坏性作用,不利于绿色农业和可持续发展。而EDTA-Fe具有适用范围广、生物学活性高、使用量少、效能高、环境污染小等特点,施用后对土壤无任何负面影响,并且还能固定土壤中的有益成分,减少流失,有利于调节土壤的酸碱性,防止土壤硬化等。因而,农业上对于可溶性的有机螯合铁肥的需求成为当务之急。综上所述,对EDTA-Fe螯合物合成研究是很有必要的。
2 实验部分
2.1 实验原理
螯合反应就是生成螯合物的化学反应。螯合物是配合物的一种,在螯合物的结构中,一定有一个或多个多齿配体提供多对电子与中心体形成配位键。“螯”指螃蟹的大钳,此名称比喻多齿配体像螃蟹一样用两只大钳紧紧夹住中心体。金属的EDTA螯合物通常比一般配合物要稳定,其结构中经常具有五元或六元环结构,增强了稳定性。正因为这样,螯合物的稳定常数都非常高,许多螯合反应都是定量进行的,可以用来滴定。EDTA-M金属螯合物合成方法主要有水体系合成法、非水体系合成法、固相体系合成法、相平衡合成法。
本文主要采用采用水体系合成法,利用EDTA中胺基能与Cu、Zn、Fe等过渡性元素形成配位键,羧基能与金属离子以离子键结合形成较稳定胺基螯合物的性质来合成EDTA-Fe螯合物,反应原理见图1。
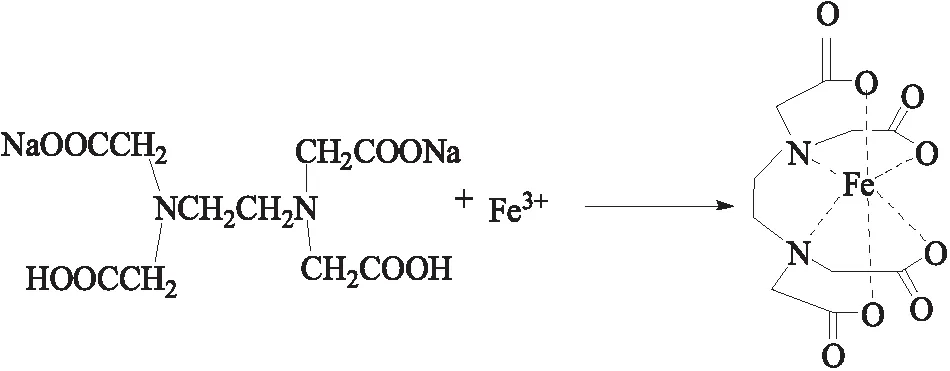
图1 EDTA-2Na与Fe3+螯合反应方程式
2.2 实验药品和仪器
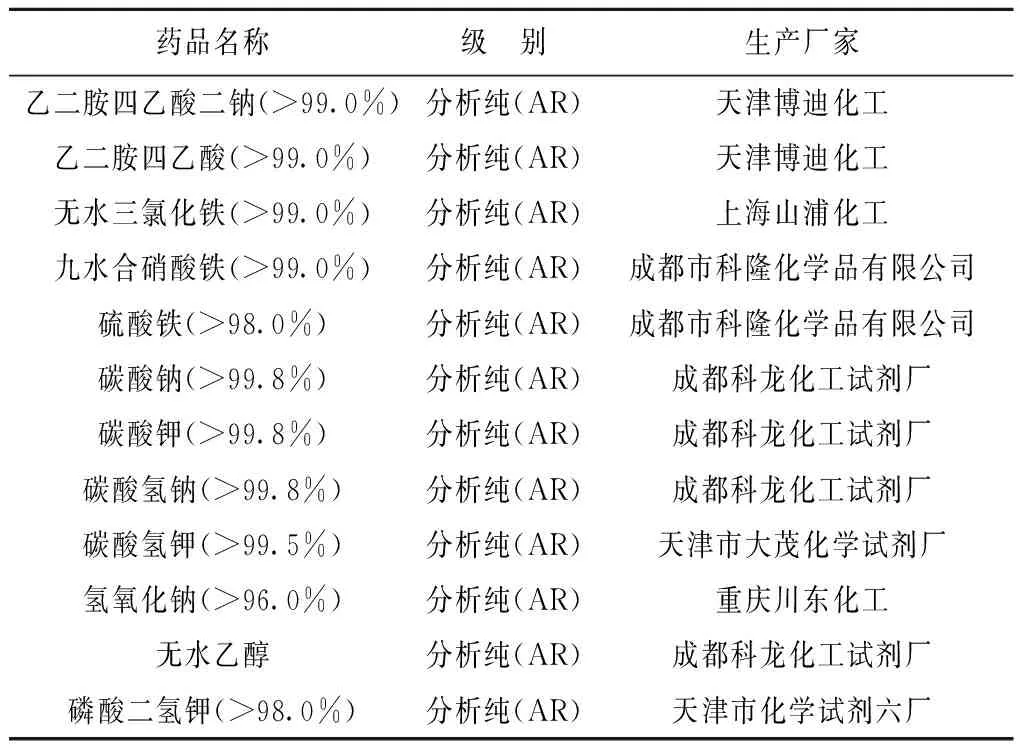
表1 主要药品

表2 主要仪器
2.3 铁的螯合实验
螯合剂采用乙二胺四乙酸(EDTA)或乙二胺四乙酸二钠(EDTA-2Na)。EDTA-2Na可溶于水,溶解后可直接与铁盐反应,在一定温度下生成EDTA螯合铁。EDTA不溶于水,可溶解于碳酸钠、氢氧化钠等碱性溶液,EDTA溶于碱性溶液后再与铁盐反应,在一定温度下生成EDTA螯合铁。螯合反应结束后进行过滤,然后加入乙醇,搅拌均匀让其自然析出晶体,抽滤干燥得EDTA螯合铁产品。工艺流程图见图2。
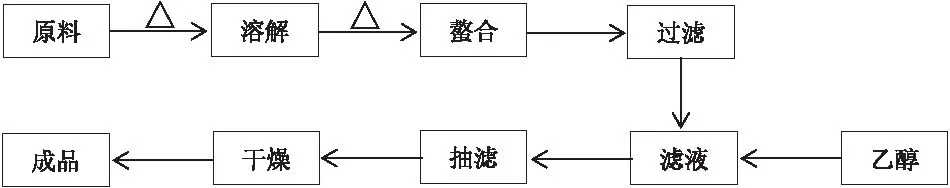
图2 EDTA—Fe生产工艺流程图
2.4 分析方法
2.4.1 定性分析
用傅里叶变换红外光谱仪、X射线衍射仪对固体成品进行检测分析,观察产品官能团的符合度,检测出成品乙二胺四乙酸铁钠分子式为C10H12N2O8FeNa·3H2O,与理论相符。
2.4.2 定量分析
将固体成品配制成含量很低的溶液,用等离子发射光谱仪检测铁元素,并通过计算得出铁的质量分数。根据以下公式算出铁的螯合率。
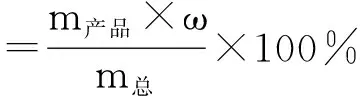
上式中m产品表示产品的质量,ω表示检测出的铁的质量分数,m总表示加入原料中铁的总质量。
2.4.3 游离Fe3+的分析
按照肥料微量元素添加量将螯合铁与磷酸二氢钾配制成一定含量的溶液,长时间放置无沉淀产生,表明产品合格,微量元素铁以螯合态存在,溶液中不存在游离的Fe3+。
3 结果与分析
3.1 原料的筛选
本文主要考察了EDTA、EDTA-2Na两种螯合剂和氯化铁、硝酸铁、硫酸铁三种铁盐,采用交叉实验的方法进行实验。实验结果表明两种螯合剂都能与铁盐进行螯合反应得到合格的产品,且收率以及产品中Fe含量都相差不大。由于EDTA不溶于水,要用碱溶,在工艺上相对要复杂同时要增加成本。氯化铁、硝酸铁、硫酸铁都能与EDTA、EDTA-2Na两种螯合剂进行螯合反应得到合格的产品,且收率以及产品中Fe含量都相差不大。硝酸铁价格较贵,氯化铁、硫酸铁价格相差不大,但硫酸铁在水中溶解度比氯化铁小,循环反应时循环次数要少3至4次。综上所述,本文在以后的实验中使用的螯合剂是EDTA-2Na,铁盐是氯化铁。
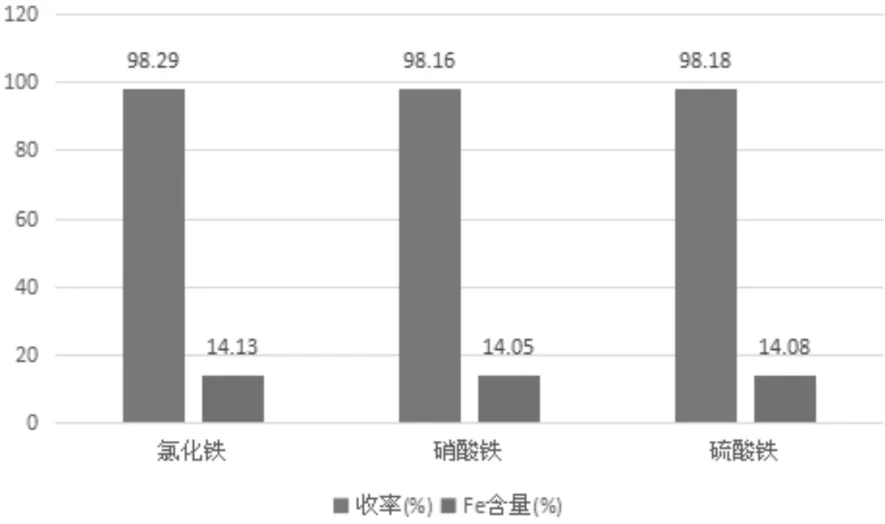
图3 EDTA为螯合剂与三种铁盐反应所得数据
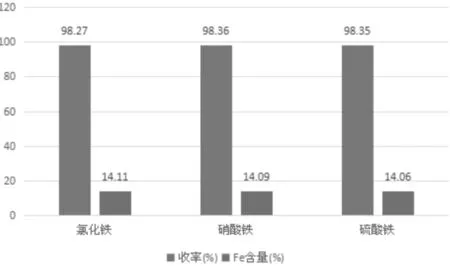
图4 EDTA-2Na为螯合剂与三种铁盐反应所得数据
3.2 螯合比对螯合反应的影响
螯合比即螯合剂EDTA-2Na与Fe3+的摩尔比。螯合比与螯合率的关系见表3。由表3中数据看出,若要EDTA-2Na和铁的螯合率同时达到100%,螯合比需要控制在1∶1。
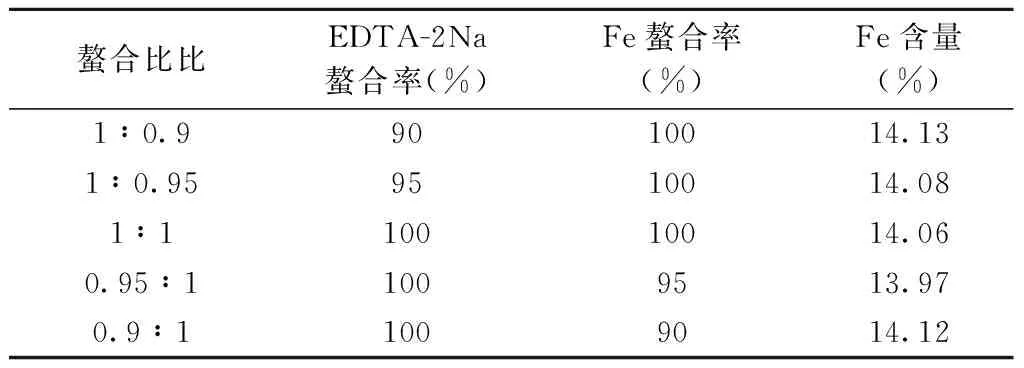
表3 螯合比比与螯合率的关系
实验表明,EDTA-2Na过量不能得到铁含量合格的产品,铁过量能得到铁含量合格的产品,但产品中会含有较多的游离态的Fe3+,对产品的应用会造成一定影响,所以螯合比以1:1为宜。
3.3 调节pH值所用碱的选择
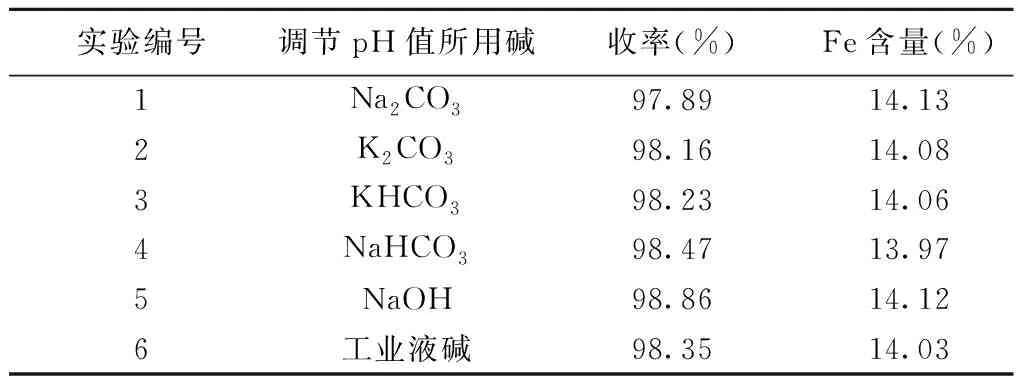
表4 调节pH值所用碱对螯合反应的影响
从表4中数据可以看出使用不同的碱对EDTA-Fe螯合反应的影响不大,而工业液碱是化工生产中常用原料,为了适应工业化生产,以后实验都采用液碱调节pH值。
3.4 温度对螯合反应的影响
螯合剂EDTA-2Na与铁盐的螯合反应可以简单的认为是酸碱中和反应,反应为放热反应,但放出热量很少,不足以加快反应速率,所以反应过程中需要外部提供热量以加快反应速率。
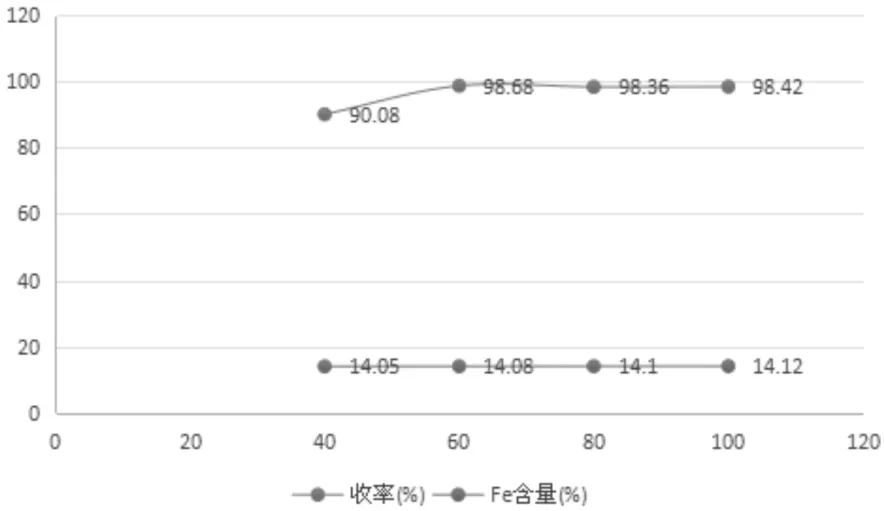
图5 温度对螯合反应的影响
实验结果表明,温度对产品铁含量影响不大,主要影响收率。温度过低,反应物不能完全反应,产品收率相对较低;温度过高虽然加快了反应速率,但增加了能耗。综合考虑反应温度选在60~70℃。
3.5 时间对螯合反应的影响

图6 时间对螯合反应的影响
实验表明,反应时间对产品铁含量影响不大,主要影响产品收率。当反应时间时间小于1.5h,产品收率相对较低,当反应时间达到1.5h以上时,产品收率较高,且处于比较稳定的范围,波动较小。反应时间较长则能耗越多,所以反应时间选在1.5~2h。
3.6 乙醇用量的考察
EDTA-Fe是易溶于水的,要想反应结束后让其从反应液中析出来是很困难的,常用的方法是减压蒸馏蒸除大部分水,然后趁热放料,在让其冷却析出。这种方法可行但需要更多的能耗,对设备要求也更高。本文采用的是加乙醇作为沉淀剂,利用相似相容原理在不蒸除水分的情况下让EDTA-Fe从反应液中析出,且母液还可以循环利用,最终乙醇也可以蒸馏甚至精馏出来继续使用。
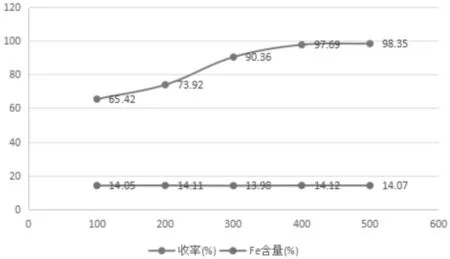
图7 乙醇添加量的考察
实验结果表明,加入沉淀剂乙醇对产品铁含量影响不大,主要影响产品收率。当反应加入水量一定时,随着乙醇量加入的增加产品收率逐渐增大,当加入乙醇量与水量达到一定比例时,产品收率增大幅度很小。实验结果表明当乙醇加入体积与水体积之比为2∶1时为最佳,经济效益最大。
3.7 母液循环利用实验

图8 母液循环实验所得数据
实验结果表明,随着循环次数的增加产品收率先增大后减小,产品铁含量在循环次数较多以后也略微有所降低。母液循环回收利用实验所得产品的平均收率为93.70%,比没有利用回收母液的收率98.21%略低。回收利用母液可以减少三废,特别是减少废水的产生,这种工艺更加生态环保,同时可以降低生产成本。
4 结论
乙二胺四乙酸螯合铁盐生产工艺简单,几乎没有“三废”污染,技术风险和环保风险较小;同时乙二胺四乙酸螯合铁盐生产设备共用性强,易于工业化生产。螯合中微量元素肥与传统上施用的无机盐类肥相比更稳定,减少了有益成分的流失,提高了肥料的有效利用率;施用后对土壤无任何负面影响,并且还能固定土壤中的有益成分,减少流失,有利于调节土壤的酸碱性,防止土壤硬化。因此乙二胺四乙酸螯合铁盐具有广阔的市场空间和经济效益。

