PVP术后手术强化椎再骨折因素分析*
王芳芳 刘红正 王拴池 陶晓冰 陈彦平
(河北医科大学附属河北省沧州中西医结合医院脊柱关节骨科,河北 沧州 061000)
老年骨质疏松性椎体骨折已成为老年人的常见疾病,而经皮穿刺椎体成形术(Percutaneous vertebroplasty ,PVP)已成为治疗老年骨质疏松性椎体压缩骨折的一种简单、微创、较好的手术方法[1]。但随着手术的广泛开展,PVP术后再发腰背部疼痛症状逐年呈上升趋势,除了相邻节段椎体骨折发生会增加以外,PVP术后骨水泥强化椎也会出现再发骨折,其发生率报道不一,但相对处于较低水平[2-3]。为探讨手术椎体再骨折发生的可能相关因素,提供防治措施,从而降低其发生率,以提高该术式的治疗效果,本文就手术椎体再骨折的发生原因及诊断要点予以分析。
1 资料与方法
1.1 临床资料 将2014年5月~2015年4月在我院行PVP术后未出现强化椎再骨折患者61例视为无骨折组,把同期行PVP术后出现强化椎再骨折患者14例视为再骨折组。纳入标准:①患者在术前均通过双能X线骨密度仪检查胸腰椎骨密度,提示骨量减少或骨质疏松;②经WHO标准被诊断为骨质疏松;③经MRI、CT、X线影像学检查被诊断为亚急性或新鲜椎体压缩性骨折。排除标准:①陈旧性骨折病史;②转移性肿瘤或脊柱原发性;③因血管瘤、多发性骨髓瘤、转移性肿瘤等而导致的病理性椎体骨折;④感染疾患或严重凝血功能障碍等不适合手术治疗的患者。
1.2 方法 取患者俯卧体位,腹部悬空,穿刺点和伤椎的定位借助C型臂X线机完成,在椎体中前1/3处缓慢注入粘稠状态的骨水泥,在透视状态下观察骨水泥扩散情况,一旦有椎体外渗漏的趋势需立刻停止。单椎体注入3.6~5.2 ml的骨水泥,术毕观察10min,当生命体征处于平稳状态时便结束手术。在术后24h进行下地活动,患者在术后行碳酸钙、活性维生素D、双磷酸盐等系统抗骨质疏松治疗。
1.3 观察指标 使用VAS评分评价患者术前、术后1d、末次疼痛缓解程度。对两组患者的年龄、性别、体质量指数、受损节段数量、骨水泥注射量、骨水泥注射方式、骨密度T值、椎体前缘高度恢复率、术后是否存在椎间盘骨水泥渗漏、术前椎体内有无合并裂隙样变、术后后凸畸形角度进行记录,并视为自变量予以统计分析。对有关危险因素进行Logistic多变量回归分析。
2 结果
2.1 不同时间点VAS评分比较 两组术前VAS评分比较差异无统计学意义(P>0.05),无骨折组在术后1d、末次随访的VAS评分低于再骨折组(P<0.05),见表1。
表1不同时间点VAS评分
Table1TheVASscoreatdifferenttimepoints
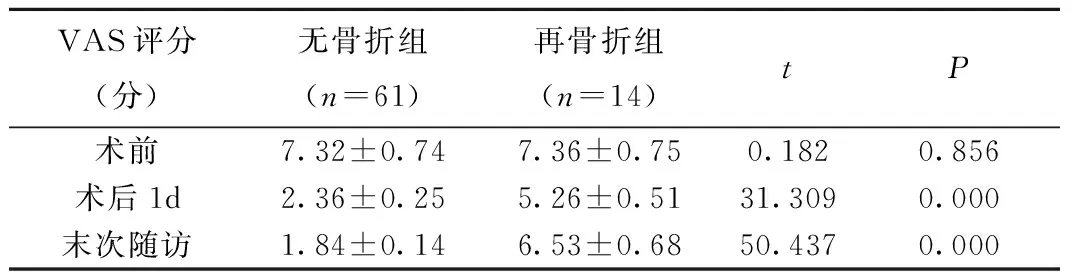
VAS评分(分)无骨折组(n=61)再骨折组(n=14)tP术前7.32±0.747.36±0.750.1820.856术后1d2.36±0.255.26±0.5131.3090.000末次随访1.84±0.146.53±0.6850.4370.000
2.2 手术椎体无骨折和再骨折组单因素分析 通过单因素分析发现体质量指数、骨密度T值、术后后凸角度是影响PVP术后手术强化椎再骨折的主要因素,见表2。
2.3 Logistic多元回归分析 通过Logistic多元回归分析发现体质量指数、骨密度T值、术后后凸角度是影响PVP术后手术强化椎再骨折的因素(P<0.05),见表3。
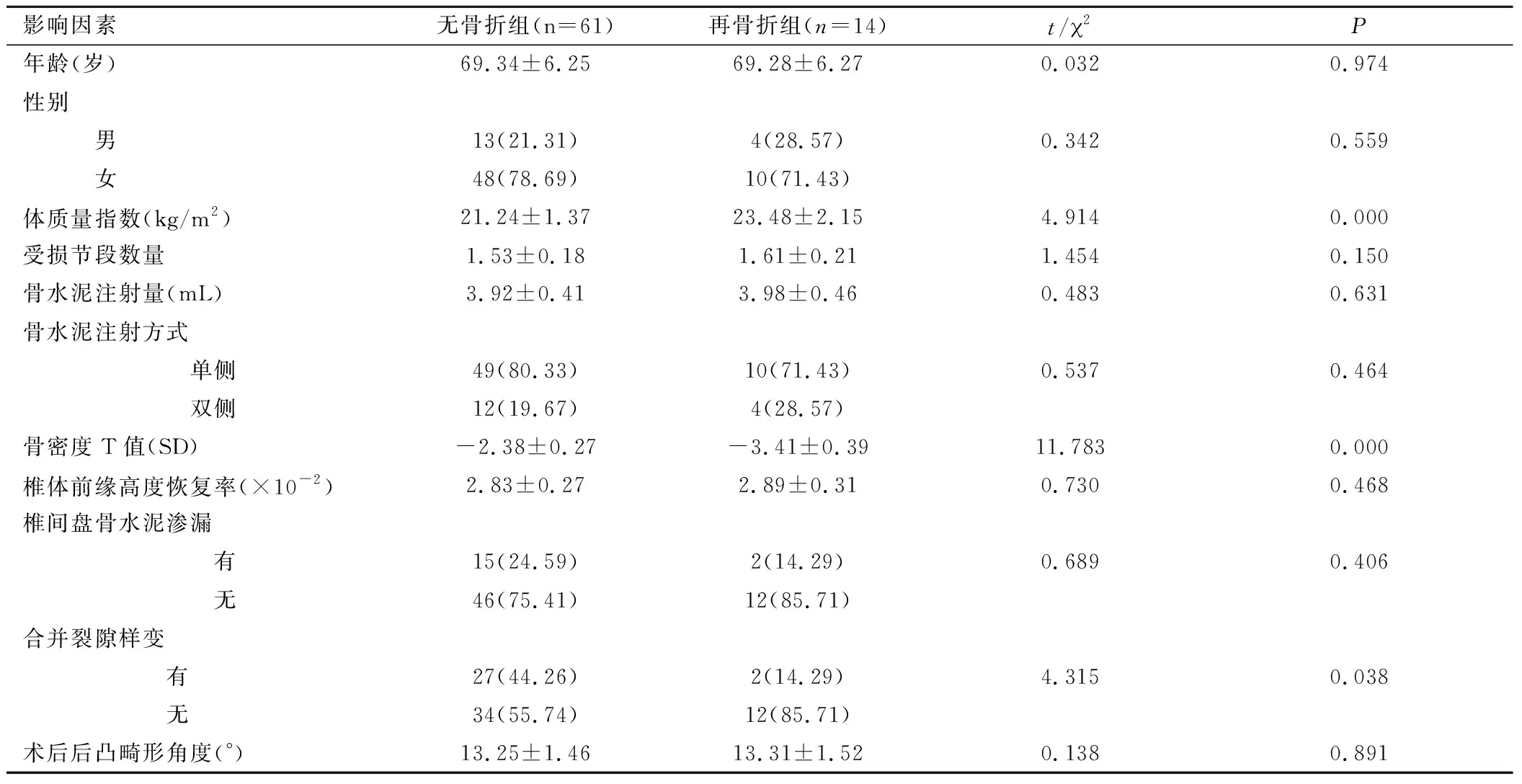
表2 手术椎体无骨折和再骨折组单因素分析Table 2 No vertebral fracture and fracture group univariate analysis
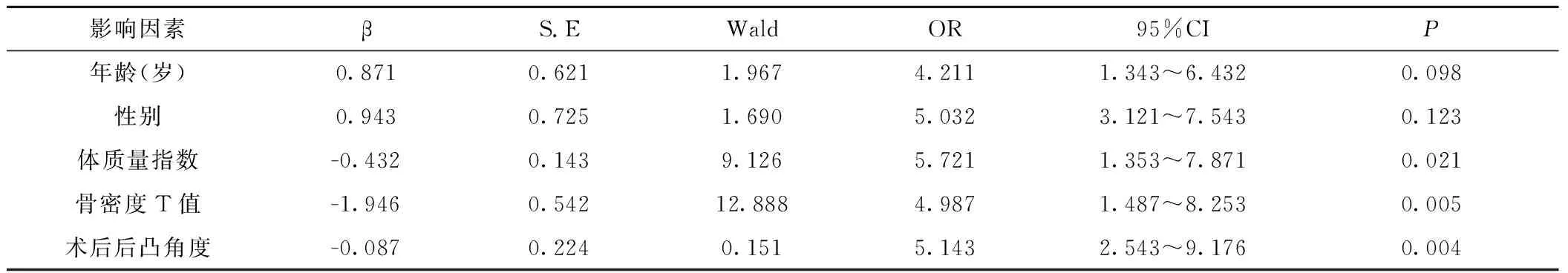
表3 Logistic多元回归分析Table 3 Logistic multiple regression analysis
3 讨论
在老年骨质疏松性压缩骨折中PVP属于应用较为广泛的一种微创手术方式,其中术后再骨折被视为一种潜在的并发症[4]。在行PVP治疗过程中有12%~52%的患者会发生新发椎体骨折。相关研究显示,老年骨质疏松性压缩骨折患者在经PVP术后70d内有18.4%的患者发生了新发椎体骨折[5]。导致再骨折的危险因素尚存争议,主要是因为再骨折患者存在个体差异、时间周期不同、发生率不同,难以明确PVP术后再骨折属于骨质疏松的自然进程,还是继发于手术本身[6]。再骨折不但会导致患者出现反复疼痛,并且会进一步加重脊柱后凸畸形,可见预防此类并发症显得颇为重要。
相关研究者曾将PVP术后再骨折的发生划分为两大类,一类和患者本身情况有关,比如激素的使用、长时间卧床、严重的骨质疏松等,其中骨质疏松病程和再骨折的发生存在着密切关联性,相对于正常人,骨质疏松患者出现骨折的风险性较高[7-8]。究其原因主要是因为骨质疏松患者有着较为稀疏的骨小梁结构,低下的骨骼强度,轻微的负重、外伤、打喷嚏、弯腰等都可能会导致相关椎体出现骨折,在骨质疏松自然进程中的椎体成形术后再骨折属于较为常见的一种并发症。相关研究显示,老年骨质疏松性压缩骨折患者不管是否经椎体成形术治疗,相对于首次骨折的发生率,其再发骨折的概率更高[9]。在评价骨质疏松患者中,骨密度属于较为重要的一个指标。相关研究显示,当骨密度每提高1%,椎体发生骨折的相对风险就会降低3%[10]。通过对PVP术后患者开展为期5年的随访发现,椎体成形术后再骨折的发生和骨密度密切相关[11]。在术后骨密度较低的患者,其术后再发骨折的概率相对较高,系统抗骨质疏松治疗能明显降低再骨折的发生率[12-13]。因此,PVP术后再骨折和低骨密度密切相关,为降低术后再骨折的发生率可采取抗骨质疏松治疗。本次研究中也发现椎体再骨折和低骨密度密切相关。另一因素主要是因为手术而引发的再骨折。相关研究显示,骨水泥会改变骨折椎体的生物力学特性,硬度为原椎体的35倍,当刚度增加至15倍会增加相邻椎节的应力[14]。相邻椎体和强化的骨折椎体间不同的刚度会导致应力分布异常,降低终板向内的应力传导,明显降低椎体的应变程度[15-16]。
PVP能恢复椎体高度,有利于脊柱后凸畸形的矫正,进而降低骨折并发症的发生率[17]。但有研究者提出后凸畸形矫正过大会明显增加再骨折的风险性[18]。强化椎体前柱高度的过度恢复以及椎体骨折和凸角度的过度矫正呈正相关性,当强化椎体前柱高度每增加1%,椎体骨折的风险性会增加7倍;当后凸角度矫正1°,椎体骨折的几率会增加9%[19-20]。本研究结果显示,术后后凸角度和老年骨质疏松性压缩骨折患者PVP术后手术强化椎再骨的发生存在着密切关联性。本次研究中还发现非再骨折患者术后1d的疼痛改善率优于再骨折患者;非再骨折患者在术后1d、末次随访的VAS评分显著低于再骨折患者。当患者伴有疼痛感时会增加骨质疏松症治疗药物的使用量,甚至会降低患者治疗依从性,不利于患者术后恢复,进而增加术后强化椎再骨折的发生率。
4 结论
体质量指数、骨密度T值、术后后凸角度是影响PVP术后手术强化椎再骨折的显著因素。

