成人型卵巢颗粒细胞瘤的MRI特征表现与病理相关性分析
河南省安阳市肿瘤医院影像科
(河南 安阳 455000)
李 铭 段成洲 张耀文夏旭东 张玉兴
卵巢颗粒细胞瘤(ovarian granulosa cell tumor,OGCT)是起源于卵巢性索间质的低度恶性肿瘤,可分为成年型和幼年型,成年型多见,主要发生在中年至绝经期后妇女,发病高峰年龄段为45~55岁,成年型颗粒细胞瘤生长缓慢,预后好但易复发,手术为首选治疗方式,需长期随访、动态监查[1]。本文对40例经手术病理证实的成人型卵巢颗粒细胞瘤患者的MRI影像资料进行回顾性分析,探讨其MRI影像表现特点,并与病理对照,旨在提高对此病诊断及鉴别诊断能力,为临床诊治提供依据。
1 资料与方法
1.1 一般资料本组40例中,年龄24~68岁,平均年龄(49±6)岁,其中29例大于45岁。位于右侧附件31例,左侧9例。合并子宫内膜增厚27例,子宫肌瘤22例。40例患者中18例为绝经后患者,11例表现为月经周期紊乱,14例意外触及下腹部包块,12例绝经后阴道不规则出血,17例为体检发现,3例下腹坠痛。
1.2 实验室检查40例OGCT患者中37例术前雌激素水平升高(血清雌二醇≥100pmol/L),35例癌胚抗原(CEA)及CAl99均正常,21例CAl25超出正常值(范围36-935 U/ml)。
1.3 检查方法采用飞利浦公司超导3.0T磁共振磁共振扫描仪,扫描前常规准备,扫描范围自肾门以下至耻骨联合上缘。扫描参数:8通道相控阵腹部体线圈。层厚5~6mm,层间距1mm。轴位采用快速自旋回波(FSE)序列,T2WITR/TE=3000/88.3ms;T1WI,TR/TE=540/7.3ms。矢状位及冠状位采用快速扰相梯度回波序列(FSPGR)序列,TR/TE=3600/111ms。增强扫描采用对比剂钆喷酸葡胺(0.1mmol/kg)经肘静脉注射后行轴位、矢状位及冠状位增强扫描。采用三维容积快速梯度回波序列(LAVA);TR 2.7ms,TE1.2ms。对比剂为Gd-DTPA,剂量15ml,流速2ml/s;动脉期、静脉期、延迟扫描时间分别为20~25s、60~70s、180s~300s。
1.4 图像分析全部MRI图像资料由两名副主任以上医师共同阅片,观测肿块的内部及相邻组织信号特征及伴随征象,对有异议的病例经过讨论后取得一致结果。
1.5 病理检查40例患者均外科切除,其病理标本以10%福尔马林液固定,石蜡包埋切片,行常规HE染色,由高年资病理医师在显微镜下观察组织形态及细胞学表现。
1.6 MRI图像与病理对照分析副主任以上影像医师对MRI图像进行分析,重点观察;病变部位、大小、形态、边界、信号特征有无分隔、囊变及腹水,对MRI形态特征逐一对照甄别,结合病理标本制作者制作切片切片情况共同分析病理成分与MRI表现特征符合程度。
1.7 统计学分析使用SPSS19.0软件进行统计学分析,对肿瘤大小与腹水量的关系用Pearson相关性分析。
2 结 果
2.1 MR表现本组40例卵巢颗粒细胞瘤均位于盆腔,MR显示起源于右侧附件区27例,左侧附件区13例,其中2例因肿瘤巨大,术前MRI未能明确其来源,经手术证实源于右侧卵巢。所有病例均行磁共振平扫及增强扫描;肿瘤最大径3~19cm,平均约10.5cm;边界均清楚,形态规则24个,不规则16个,后者呈浅分叶状。根据肿瘤影像表现分为3型:(1)囊实性肿块(23个):呈不均匀蜂窝状,分隔厚薄不一,以厚分隔为主,MRI平扫T1WI呈等低混杂信号,信号略低于同层肌肉,T2WI呈混杂高信号,内见多发大小不等的蜂房影,囊内壁光滑,增强扫描肿块实性部分及分隔强化明显,囊液性区无强化(如图1-2);(2)囊性肿块(11个):囊壁厚2~4 mm,单房多见,其内可见等信号纤细分隔线影,囊内壁较光滑,囊内容物呈长T1、长T2信号,增强扫描囊壁中度强化(如图3-6);(3)实性肿块(6个):大小约3-5cm,其内信号大致均匀,可有少许混杂信号,边缘清楚,均有假包膜(如图7-10)。
2.2 手术及病理表现40例患者均经腹行附件肿瘤切除术,术中肿瘤大小、形态、位置均与MRI所见符合。术中所见肿瘤外形呈圆形或类圆形,可有浅分叶,表面光滑,多有完整包膜,肿瘤周围组织层次清楚,无粘连。囊性肿物,质较软,囊壁切面灰白,囊内容物清亮;囊实性肿瘤,体积越大囊变区越多,肿瘤切面呈淡黄色,囊液为胶冻样或水样,囊壁光滑,壁内无突起结节;实性肿瘤囊变不明显,质地较硬,切面呈黄白色,偶见缺血坏死灶,是囊变的基础。成年型OGCT肿瘤的细胞核非常一致,呈小多边形,像“石榴子”样(见图10),三种类型病理表现区别在于纤维结缔组织的多少,实质细胞成分无区别。
2.3 腹水与肿瘤大小相关性MRI检查显示27例患者有盆腔积液,术中所见积液多粘稠,呈淡黄色,量约50~400ml;肿瘤大小以横轴位最大经线计算,腹水量以术中吸引器抽吸量计,18例患者腹水量<100ml,其肿瘤直径4.9至16.7cm,腹水量大于100ml小于200ml者共6例,腹水量大于200ml小于400ml者共3例,其腹水含量与肿瘤大小无相关性(r=0.19,P=0.08)。
3 讨 论
3.1 OGCT的临床表现OGCT作为一种相对少见的卵巢功能性低度恶性肿瘤,多见于单侧,以右侧多见。本组40例成人型OGCT,均为单侧肿瘤,平均直径约10.5cm,因肿瘤产生雌激素所引发的高雌激素症状,临床主要表现为青春期性早熟,生育期妇女月经紊乱,绝经后阴道不规则出血等[2],MRI表现为子宫体积增大,内膜增生明显,少数瘤体可自发破裂,临床出现腹痛症状伴腹腔积液。
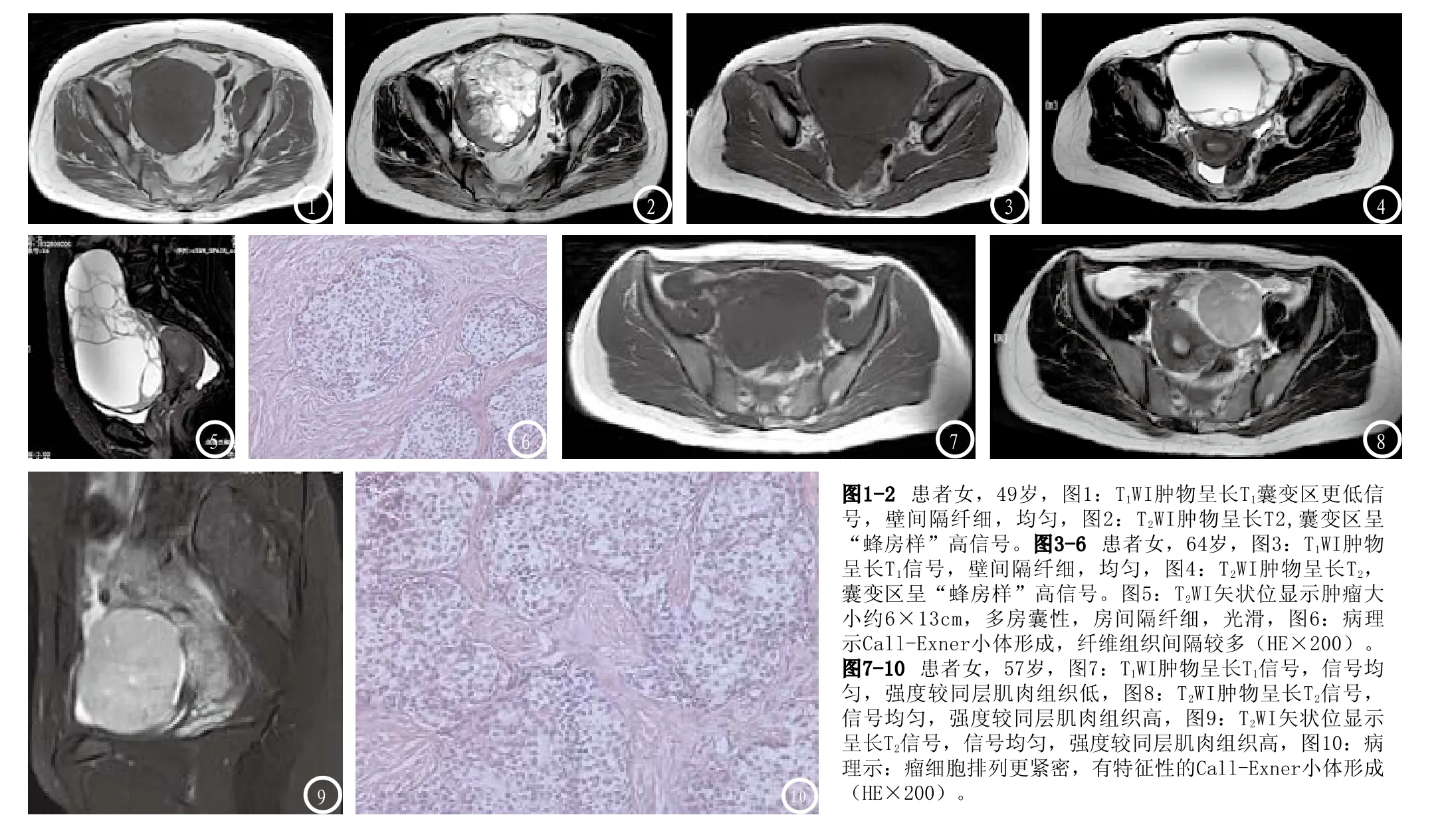
3.2 OGCT的MRI表现与病理比较卵巢颗粒细胞瘤内囊、实性比例,与肿瘤的大小有关。多数学者[3-4]认为早期肿瘤较小时以实性成分为主,肿瘤呈圆形、类圆形,可有浅分叶状,囊变不明显,MR表现与病理基础密切相关,其中T2WI像肿瘤表现最能反映病理基础。随着肿瘤体积增大,膨胀式生长使肿瘤对相邻组织以推挤压迫为主,其后瘤体逐渐可出现囊变,此时以囊实性肿块为主,随着颗粒细胞肿瘤组织进一步液化坏死,最终可造成完全囊变。本组23例(57.5%)在MRI上表现为附件区边界清楚9至15cm的囊实性肿块,与文献报道相符[5]。囊内厚薄不等的分隔为未完全坏死的颗粒细胞,囊壁厚度大致均匀,内壁光滑,无明显壁结节。OGCT大体标本上所见肿瘤囊变区与MRI T2WI上散在分布的片状或蜂窝状高信号区相一致,而肿瘤内实性区域及囊间分隔与MRI T2WI上表现为肿瘤内的片状和线样等信号区相一致。在高水平雌激素的刺激,卵巢颗粒细胞瘤内可产生大量新生血管,形成大量动静脉瘘,是MRI增强扫描时肿瘤于各期均见强化的病理基础[5]。颗粒细胞瘤的信号混杂,囊变呈“蜂房状”改变,肿瘤周边的低信号称“假包膜”,其在病理上实为被压缩的卵巢间质及纤维结缔组织;肿瘤边缘T2WI上囊状高信号影代表卵泡影或水肿区[6-8],是其MRI典型影像学表现,包膜的完整性对肿瘤是否向周边浸润重要标准,本组病例中包膜显示率为67.5%(27/40),与袁晓春[9]等报道假包膜率51.6%(16/31)接近。
3.3 鉴别诊断(1)卵巢癌:多发生双侧,形态不规则,无明显包膜,呈浸润性生长,囊壁及囊内分隔毛糙不规则,囊壁厚薄不等,常有壁结节形成;其特点有:①多房常见,各房因坏死、出血程度不同密度常不一致;②病灶形态多变,边界模糊;③乳头状壁结节,为卵巢上皮源性肿瘤的特征;④血供丰富、实质性组织增强扫描显著强化,常伴有腹膜增厚、增大淋巴结等转移征象。(2)卵巢囊腺瘤:为卵巢最常见肿瘤,约占卵巢良性肿瘤的45%,分为浆液性和粘液性两种。一般直径更大,可至15~20cm,典型的粘液性囊腺瘤囊壁较厚,增厚的囊壁或囊隔上乳头状突起多不规则,增强扫描时囊壁和囊隔强化明显,乳头状突起强化不均匀,MRI上信号高于一般的液体信号。(3)子宫浆膜下或阔韧带肌瘤:主要与实性OGCT 鉴别,子宫浆膜下或阔韧带肌瘤的组织密度一般较OGCT高,因肌瘤含有致密的平滑肌组织,其T1WI和T2WI均呈低信号,尤以T2WI上信号更低,信号均匀或不均匀,增强扫描肌瘤信号与正常子宫肌层类似,强化程度亦低于颗粒细胞瘤。由于卵巢颗粒细胞瘤因含脂质成分相对较多,T1WI和T2WI上信号常高于子宫肌层,而且颗粒细胞瘤有相应的临床特征及合并症,以资鉴别。(4)卵黄囊瘤:多呈体积较大的单发、囊实性肿块,发病年龄较低,常见于青少年女性,病灶增强扫描时常明显强化,辅助检查提示甲胎蛋白(AFP)多高于正常值。(5)畸胎瘤:囊壁更厚,囊内软组织成分信号多均匀,较少呈“蜂窝状”或“海绵状”,强化程度较低。如果含有脂肪或骨组织成分更容易鉴别,典型的囊性畸胎瘤表现为含脂肪或“脂-液”平面的囊性肿物。
卵巢肿瘤实性成分的存在对诊断卵巢恶性肿瘤具有较高的提示作用。肿块内含有实性结节或乳头状突起物,大于3mm以上多房间隔,腹盆腔积液,腹膜多发结节灶及淋巴结增大均为恶性肿瘤的特征[10],本组中27例患者有不等量腹水,原因不明确,分析可能与肿瘤压迫、对腹膜刺激、淋巴管受阻及组织通透性增加等因素有关。囊性肿瘤多为良性病灶表现,囊实性肿瘤多为交界性或恶性肿瘤。初发OGCT由卵巢动脉供血,引流静脉为卵巢静脉,正常或增粗的卵巢静脉进入盆腔肿块(卵巢血管征)常提示肿块源于卵巢。骈文婷[11]等报道卵巢肿瘤在MRI T1WI上呈高信号提示含出血或脂肪成分,或含粘液的大分子物质,结合压脂T2WI可明确病灶成分,DWI上实性成份的低信号影对良性肿瘤的诊断有重要意义。
综上所述,成人型卵巢颗粒细胞瘤MRI表现具有一定的特征,当成年妇女(尤以绝经期女性)临床上出现高雌激素血症如:内膜增厚、子宫体积增大、不规则阴道出血等,MRI表现为附件区囊实性肿块,囊壁及房间隔纤细、光滑,无壁结节呈“蜂房样”改变,增强扫描肿瘤的实性部分及间隔明显强化,肿块边界清晰,有假包膜的病例,应考虑本病的可能,最终明确诊断依靠术后病理组织学检查。

