老年宫颈上皮内瘤变锥切术切缘阳性危险因素及预后
王思灵 王丽雅 陈玉榕
(儋州市人民医院妇产科,海南 儋州 571700)
宫颈上皮内瘤变(CIN)反映患者从宫颈不典型增生向宫颈浸润癌转变的一系列连续过程,患者一般常常无明显的临床症状〔1〕,所以早期通过常规临床检查难以被发现,现如今通过阴道镜多点活检和颈管刮片术的引入让CIN早期诊断成为可能,对于阴道镜不满意CIN患者临床上通常采用手术治疗,其中宫颈锥切术是临床上常用术式,对于宫颈锥切术手术方法包括宫颈冷刀锥切(CKC)和环形电切除(LEEP)术,影响宫颈锥切术切缘的影响因素很多,术中宫颈体积、病变累及范围、宫颈萎缩程度都会对宫颈锥切术切缘状况产生影响。老年患者由于其他基础性疾病较多,机体免疫功能下降,更容易由于人类乳头瘤病毒(HPV)感染而导致CIN。近年来有研究指出,子宫颈锥切术切缘阳性通常容易造成CIN患者复发,但是对宫颈切缘阳性处理尚存在争议,切缘阳性并不代表手术失败,但是也不能排除有病变残留的可能,对于切缘阳性处理还需要进行针对性个体化处理〔2〕。有文献指出,宫颈切缘阳性的患者通过随访观察,复发率可高达18%以上,严重影响预后〔3〕。本文对比CIN患者手术方式、宫颈上皮腺体受累、宫颈柱状上皮异位、CIN分级等因素在不同切缘状态患者之间的差异,为CIN患者手术治疗与预后评价提供参考。
1 资料与方法
1.1一般资料 2015年1月至2016年1月儋州市人民医院接受治疗的323例老年CIN患者,入院后行CKC或LEEP术,依据术后病理结果,44例子宫颈切缘阳性患者为观察组,279例子宫颈切缘阴性患者为对照组,两组一般临床资料差异均无统计学意义(P>0.05),具有可比性。见表1。

表1 两组一般临床资料比较
患者术前均行阴道镜活检及术后病理检查符合CIN诊断标准〔4〕,无既往宫颈锥切手术史,均签署知情同意书,治疗方案经过儋州市人民医院伦理委员会批准。排除阴道炎症及细菌感染、肝肾功能异常、心脑血管疾病、凝血功能障碍、病理资料不全、依从性差、随访失联的患者。
1.2手术方法 根据术前行阴道镜活检情况进行选择,对阴道镜活检CIN Ⅰ期患者采用随访物理治疗或行LEEP术,CIN Ⅱ~Ⅲ期患者术前采用宫颈管搔刮术后,再采用LEEP术或CKC术,手术切除时使用碘液进行宫颈涂抹标记手术范围,以碘不着色区外0.3~0.5 cm为子宫颈外切缘,切除深度2 cm左右,术后利用丝线进行标记切缘内外口及点位,切除组织及时送病理检查。
1.3观察指标 单因素分析相关因素分别为手术方式(LEEP或CKC术)、宫颈上皮腺体受累情况、宫颈柱状上皮异位情况(Ⅰ~Ⅲ级)、CIN分级(Ⅰ~Ⅲ级、Ⅰa1~Ⅰa2期宫颈癌)、碘不着色区最大径(<1 cm,≥1 cm且<2 cm,≥2 cm)、高危HPV感染(HPV16/18)。将手术方式(LEEP或CKC术)、宫颈上皮腺体受累、宫颈柱状上皮Ⅲ级异位情况、CIN分级(Ⅰa1~Ⅰa2期宫颈癌)、高危HPV感染(HPV16/18)5个因素为自变量纳入Logistic回归方程。比较术后2年随访复发率的差异,按照随访阴道镜活检结果达到CIN Ⅱ级以上定义为术后CIN复发。
1.4统计学方法 采用SPSS22.0及GraphPad Prism6统计软件进行t、χ2检验。复发率采用Kaplan-Meier曲线计算,复发率比较采用Log-rank检验。
2 结 果
2.1两组子宫颈锥切阳性相关因素 观察组外切缘阳性15例(34.09%),内切缘阳性29例(65.91%)。观察组和对照组手术方式、宫颈上皮腺体受累、宫颈柱状上皮异位、CIN分级、高危HPV感染(HPV16/18)比较差异均具有统计学意义(P<0.05)。两组碘不着色区最大径线差异无统计学意义(P>0.05)。见表2。
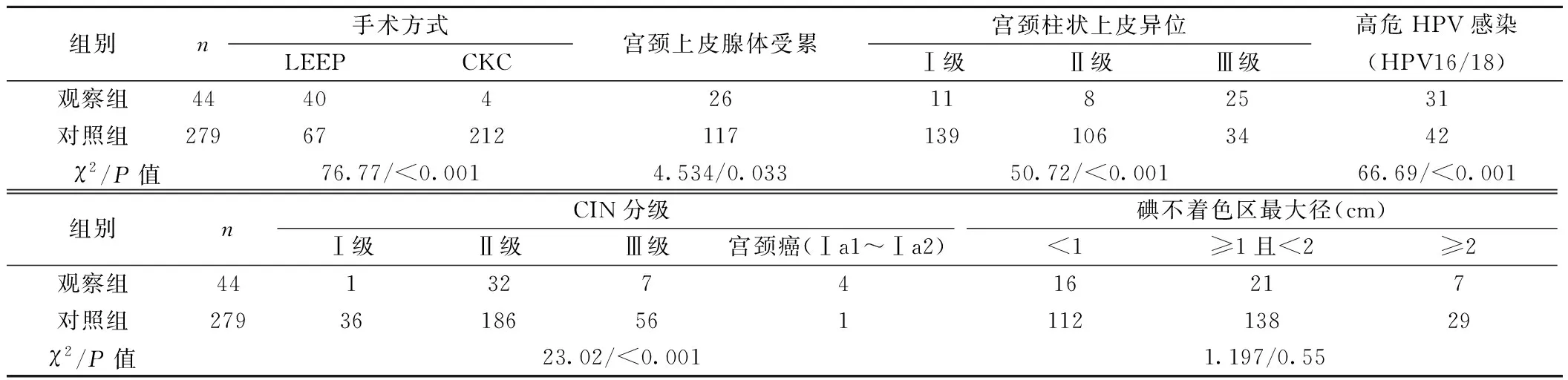
表2 两组子宫颈锥切阳性相关因素(n)
2.2子宫颈锥切阳性患者危险因素Logistic分析 采用Logistic多因素回归法对子宫颈锥切阳性患者危险因素进行分析,子宫颈锥切阳性为回归方程的因变量,将手术方式、宫颈上皮腺体受累、宫颈柱状上皮Ⅲ级异位情况、CIN分级、高危HPV感染5个相关因素为自变量,发现LEEP术、宫颈上皮腺体受累、宫颈柱状上皮Ⅲ级异位、宫颈癌(Ⅰa1~Ⅰa2期)、高危HPV感染是子宫颈锥切阳性的危险因素。见表3。

表3 子宫颈锥切阳性患者危险因素Logistic分析
2.3两组术后2年内随访复发率比较 观察组术后随访采用阴道镜活检辅助检查,术后6例(13.64%)复发,其中CINⅡ级3例,CIN Ⅲ级3例。对照组复发3例(1.08%),其中CINⅡ级2例,CIN Ⅲ级1例。观察组明显高于对照组(χ2=27.24,P<0.001)。见图1。

图1 两组术后随访复发率Kaplan-Meier曲线
3 讨 论
CIN病变属于癌前病变,近年来CIN有年轻化的趋势,老年人群由于激素水平下降伴随着身体免疫功能水平下降,更容易由于发生CIN后得不到诊断忽略治疗,而导致宫颈癌。
CIN手术治疗临床通常采用子宫锥切术,手术操作可以清除病变部位异常的上皮组织,对正常宫颈组织细胞损伤较小,传统CKC和LEEP术都可以达到良好的治疗效果,其中CKC术可以尽可能大地切除宫颈相关病变组织,切除标本可保持原始状态,但是存在手术时间长、术中出血量大、感染概率高、宫颈粘连等局限性。LEEP是通过电热效应切除病变组织,具有手术出血量小、术后恢复时间短等优点〔5〕,但是其切缘常出现电灼伤,对标本病理判断可能带来一定影响〔6〕。有学者指出,两种术式的治疗效果和预后差异无统计学意义〔7〕,都可以在治疗中加以使用。
不论采用何种手术方法,由于患者CIN病变常呈多点状分布,势必手术操作过程中会造成切除残留部分病灶而发生宫颈切缘阳性,研究指出,宫颈锥切术后宫颈切缘阳性患者残留病变的发生率高于切缘阴性患者,术后随访观察切缘阳性患者复发率也较高〔8〕。但也有学者指出,行LEEP术后的CIN切缘阳性与切缘阴性患者在病变持续存在及随访复发率差异无统计学意义〔6〕,提示行LEEP术的CIN患者切缘阳性并不代表手术治疗的失败,可能与LEEP术电热效应及切口愈合产生炎症反应减少切缘阳性患者病变持续存在有关。
有文献报道,对于行宫颈椎切术后切缘阳性发生率为14%~25%〔4,9〕,与本研究中宫颈锥切阳性率相近。影响宫颈锥切术切缘状态的影响因素很多,有年龄、绝经状态、累及腺体、吸烟、感染等因素〔10〕。有学者指出对于不同年龄的CIN患者通常采用不同宫颈锥切术式,对于高危病变和腺体累及程度较高,且无生育愿望的高龄女性常采用CKC术,对于年轻女性患者一般只采用LEEP〔9〕,但是切缘阳性患者的处理临床上尚未统一意见,也有学者指出,CKC术后残留率较LEEP低,术后效果较好〔9〕,本文提示对于高龄且无生育愿望的妇女行CKC术较为安全。高危型HPV感染为宫颈癌发病原因之一,对于CIN患者行HPV检测尤为重要,可以作为病变残留判定指标之一〔11〕,有文献指出,CIN患者LEEP术后合并高危HPV病毒感染易导致病灶残留,术前高载量HPV感染也会加大LEEP术对病灶清除的难度〔12〕,影响手术效果。
本研究说明锥切术切缘阳性患者复发率高于切缘阴性患者,切缘阳性患者术后持续性病变残留及复发风险加大,对患者预后带来了严重的影响,同样提示应该在手术中降低切缘阳性的发生,尽可能切除残留病灶。有文献指出,有20%左右的CIN患者行宫颈锥切术后随访过程中可发现病灶持续存在,严重者可进一步发展成为宫颈浸润癌〔13〕,在宫颈锥切术切缘阳性患者随访中应注意如果发生CIN复发的病例,根据病情酌情给予二次宫颈锥切术,特别对于年纪较轻且有生育需求的妇女具有积极的意义〔14〕,但是二次锥切术可能导致患者宫颈功能不全及宫颈粘连,手术医师应根据患者病情具体情况给予个体化治疗方案,术后给予密切随访,降低二次术后复发及癌变的风险〔15〕。

