去铁胺联合去铁酮对重型地中海贫血患儿血糖代谢的影响
周传恩,熊寿贵
(广东省珠海市妇幼保健院,广东 珠海 519000)
地中海贫血(thalassemia)是指基因缺陷导致血红蛋白成分改变的一种慢性进行性溶血性贫血,是常见的遗传性血液系统疾病。重型地中海贫血患儿需要长期输血[1],但长期输血会造成体内红细胞不断分解,铁质大量聚集,易出现铁过载,损伤多种器官和组织功能,进而引起心力衰竭、糖代谢紊乱等。因此,治疗重型地中海贫血临床一般建议配合除铁剂、脾脏摘除或干细胞移植等[2]。脾切除或栓塞虽可减轻患儿体内铁负荷,但会严重降低患儿的免疫功能;干细胞移植血液配型十分困难,且价格昂贵,易产生移植后排斥反应。除铁剂治疗是目前临床使用最广泛的方案,包括去铁胺(deferoxamine,DFO)和去铁酮(deferiprone,DFP)[3]。去铁胺疗效确切,但生物利用度低,消除半衰期短,患儿需长时间肌肉注射或静脉注射,易产生不良反应[4];去铁酮为口服去铁剂,临床经验较少,疗效一直存有争议[5]。本研究中探讨去铁胺联合去铁酮治疗重型地中海贫血的临床疗效及对血糖代谢的影响,为临床治疗提供新思路,现报道如下。
1 资料与方法
1.1 一般资料
纳入标准:符合《重型β地中海贫血的诊断和治疗指南》[6]中重型地中海贫血的诊断标准;经血红蛋白(HGB)分析和/或基因检查确诊;长期接受输血维持治疗,HGB>90 g/L;临床资料完整;本研究已获我院医学伦理委员会的审查批准,患儿家属或法定监护人签署知情同意书。
排除标准:合并急性感染、创伤或各种应激情况;合并肝肾功能严重损伤,不能耐受治疗;受试前服用影响糖代谢药物;精神障碍、智力异常;依从性差。
病例选择与分组:选择我院血液科2010年1月至2017年12月收治的重型地中海贫血患儿114例,按照随机数字表法将患儿分为DFO组(48例)和联合组(66例)。两组患儿一般资料比较,差异无统计学意义(P>0.05),具有可比性。详见表1。

表1 两组患儿一般资料比较
1.2 方法
所有患儿每2~4周输注浓缩红细胞每10 kg体质量 0.5 ~1.0 U。治疗前检测患儿空腹血糖(FBG)、血清铁蛋白(SF)、空腹胰岛素(FIns)。DFO 组患儿接受注射用甲磺酸去铁胺(商品名得斯芬,Novartis Pharma Stein AG,进口药品注册证号H20140678,规格为每支0.5 g)治疗,采用5 mL注射用水溶解0.5 g去铁胺,加入0.9%氯化钠注射液500 mL静脉滴注,1次/日,治疗12个月。联合组患儿在DFO组治疗基础上口服去铁酮片(商品名奥贝安可,ApotexInc.-Etobicoke Site,进口药品注册证号 H20140379,规格为每片 50 mg)75 mg /(kg·d),3次 /日,治疗12个月。
1.3 观察指标与疗效判定标准
样本收集和处理:所有受试者经过夜禁食8 h后,次日清晨取坐位,取肘静脉血,分三部分进行检测,分别送至我院检验科检测血糖水平,核医学科检测胰岛素水平,经离心取上清液,置-20℃保存备用。
实验室指标:采用Beckman AU480型全自动生化分析仪(德国Beckman coulter公司)检测 FBG。参照美国糖尿病学会 2003年制订的标准(FBG 5.6 mmol/L为正常值;FBG 5.6~7.0 mmol/L 为 FBG 受损;FBG≥7.0 mmol/L 为糖尿病)。
SF测定:距离上次输血2周以上测定SF值。采用Beckman DXI800型全自动化学发光仪(德国Beckman coulter)检测血清 SF值。500~999 ng/mL为Ⅰ期,1 000~2 499 ng/mL为Ⅱ期,2 500~4 999 ng/mL为Ⅲ期,≥5 000 ng/mL为Ⅳ期。
FIns测定:采用放射免疫分析法测定FIns。胰岛素抵抗指数(HOMA-IR)=FBG×FIns/22.5,其中 FIns≥2.69 U/mL时,考虑存在胰岛素抵抗。
疗效判定:显效,SF≤2 000 ng/mL且比治疗前降低 >500 ng/mL;显效,SF≤2 000 ng/mL 且比治疗前降低100~500 ng/mL;无效,SF>4 000 ng/mL且持续升高。
1.4 统计学处理
2 结果
结果见表2至表6。经单因素分析,经 DFO联合DFP治疗后血糖正常患儿年龄、平均病程、体质量指数(BMI)、治疗前血清SF水平均低于血糖受损患儿,差异有统计学意义(P < 0.05)。提示,年龄、病程、体质量指数及血清SF水平均可能影响DFO联合DFP治疗对重型地中海贫血患儿血糖的改善作用。

表2 两组患儿临床疗效比较[例(%)]
表3 两组患儿SF水平比较(s,ng/mL)
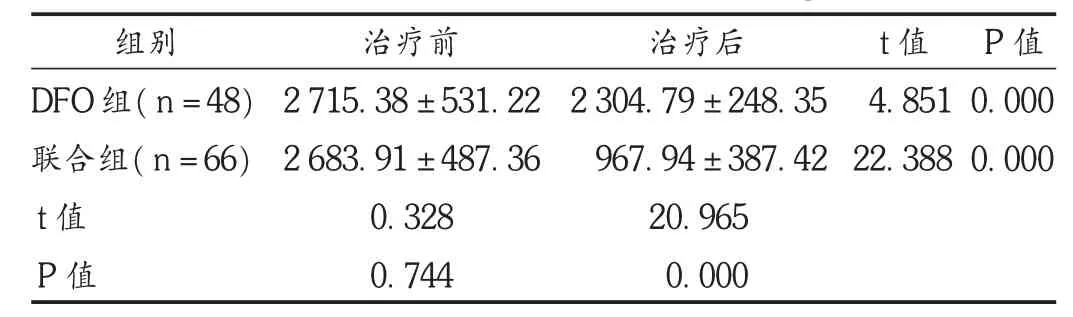
表3 两组患儿SF水平比较(s,ng/mL)
组别DFO 组(n=48)联合组(n=66)t值P值治疗前2 715.38 ± 531.22 2 683.91 ± 487.36 0.328 0.744治疗后2 304.79 ± 248.35 967.94 ± 387.42 20.965 0.000 t值4.851 22.388 P值0.000 0.000

表4 两组患儿血糖正常例数比较[例(%)]
3 讨论
地中海贫血是地中海地区临床常见的基因遗传性疾病,我国发病率相对较低,主要集中在广东和广西一带[7]。由于地中海贫血的发生与珠蛋白基因缺陷密切相关,因此缺乏有效的根治性方案,临床一般采取长期输血进行维持治疗或者进行脾切除或栓塞、干细胞/祖细胞移植治疗。脾脏是人体最大的免疫器官,尤其是患儿各器官系统尚未发育完全,摘除脾脏后易造成患儿免疫力低下易引发感染,且严重影响患儿的生长发育和生活质量[8]。目前,干细胞移植是公认的治疗地中海贫血的根治性方法,但治疗费用昂贵,且人类白细胞抗原(HLA)相合供者来源困难,而且术后排斥反应不可避免[9]。因此,目前临床多选择高输血配合除铁剂治疗。
表5 两组患儿血糖和胰岛素水平比较(s)
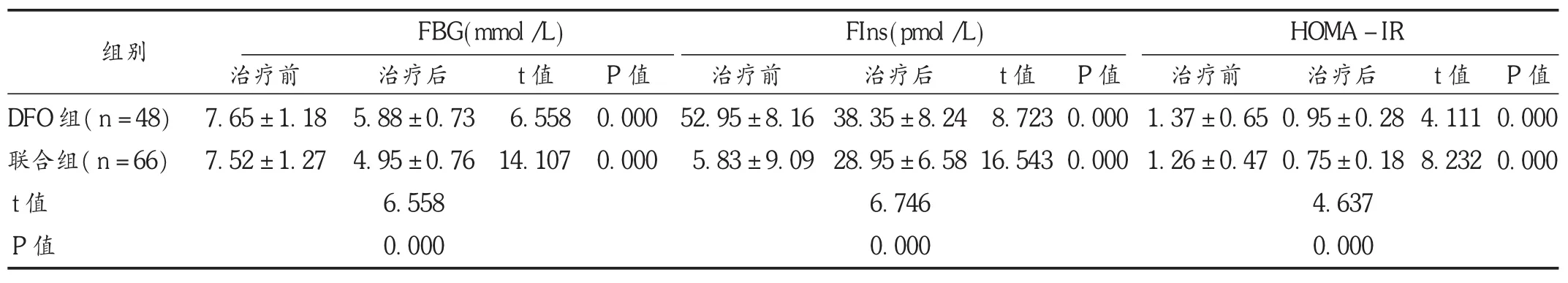
表5 两组患儿血糖和胰岛素水平比较(s)
组别 FBG(mmol/L) FIns(pmol/L) HOMA - IR DFO 组(n=48)联合组(n=66)t值P值治疗前7.65 ± 1.18 7.52 ± 1.27治疗后5.88 ± 0.73 4.95 ± 0.76 6.558 0.000 t值6.558 14.107 P值0.000 0.000治疗前52.95 ± 8.16 5.83 ± 9.09治疗后38.35 ± 8.24 28.95 ± 6.58 6.746 0.000 t值8.723 16.543 P值0.000 0.000治疗前1.37 ± 0.65 1.26 ± 0.47治疗后0.95 ± 0.28 0.75 ± 0.18 4.637 0.000 t值4.111 8.232 P值0.000 0.000

表6 影响联合组患儿治疗后血糖代谢的相关因素
地中海贫血患者血红蛋白成分遭到破坏,大量铁蛋白在心脏、肝脏、肾脏、胰腺等器官中蓄积,长期输血更增加了体内铁负荷量,从而导致多器官损伤及糖代谢紊乱[10]。机体内铁代谢与糖代谢密切相关,其中骨成形蛋白(BMP)是调控铁代谢的重要因子[11];铁过载时,与铁结合的转铁蛋白数量增多,通过与受体结合,激活BMP信号转导通路,上调铁调素的表达,使血清SF下降。BMP不仅能调控铁代谢,而且也是胰岛素分泌的重要调控因子[12]。因此,重型地中海贫血患儿铁过载易引发血糖代谢异常。
去铁胺和去铁酮是目前临床治疗铁过载的最常使用的除铁剂。去铁胺是长期输血的重型地中海贫血患儿一线除铁治疗药物,但生物利用度低,半衰期短,需每日长时间静脉滴注,因此依从性较差,且影响患儿的生活质量[13]。去铁酮是20世纪90年代初用于临床的小分子螯合剂,口服吸收利用度高,与Fe3+结合后可迅速清除体内的铁蛋白,同时可促使与转铁蛋白结合的铁离子代谢;给药方便,不良反应低,依从性较好[14]。目前,临床关于去铁酮的疗效一直存有争议,认为去铁酮对铁代谢的改善效果不明显[15]。本研究结果显示,联合组的总有效率、对血清SF水平的降低作用及对血糖代谢和胰岛素抵抗的改善作用均优于去铁胺单药治疗。通过单因素分析发现,患儿年龄、BMI、病程、血清SF水平都可能与血糖代谢密切相关。据推测可能是由于随着患儿年龄和体质量增加,血糖水平也普遍升高,更易引发糖代谢紊乱,因此,建议地中海贫血患儿尽早接受除铁治疗,且治疗期间尽量控制体质量。
综上所述,去铁胺联合去铁酮可有效改善重型地中海贫血患儿铁过载及血糖代谢紊乱,治疗效果优于去铁胺单药治疗,具有良好的临床推广价值。建议高量输血地中海贫血患儿尽早接受除铁治疗,且治疗期间尽量控制体质量,避免超重对血糖代谢造成的影响。
——忌食

