全胸腔镜二尖瓣成形术的临床应用研究▲
刘胜中 谭 今 向 波 蒋 露 魏大闯 曾富春 张晓慎 于 涛 黄克力* 左明良
(四川省医学科学院·四川省人民医院,1 心脏外科中心,2 心血管超声及心功能科,成都市 610072)
随着心脏瓣膜外科技术的不断提高,以及患者对生活质量要求的不断提升,越来越多的二尖瓣疾病患者接受二尖瓣成形手术治疗[1]。近二十年来,微创心脏外科发展迅速,尤其是右胸小切口或胸腔镜辅助右胸小切口心脏手术已在较多心脏中心开展,但能进行全胸腔镜心脏手术的中心相对较少[2-3]。2016年2月至2017年5月,20例二尖瓣疾病患者在四川省人民医院心脏外科中心接受了全胸腔镜二尖瓣成形术治疗,取得了良好的临床效果。现报告如下。
1 资料与方法
1.1 临床资料 全组20例患者,男6例,女14例,年龄13~71(45.10±14.91)岁;体重40~78(59.75±9.56)kg。心脏彩超提示先天性心脏病、继发孔型房间隔缺损5例,其中伴二尖瓣轻度关闭不全(中心性返流,Ⅰ级)3例,二尖瓣后叶P1~P2脱垂伴轻中度关闭不全(偏心性返流,Ⅱ~Ⅲ级)1例,二尖瓣前叶A3脱垂伴中度关闭不全(偏心性返流,Ⅲ级)1例;左心房黏液瘤3例,其中伴二尖瓣轻度关闭不全(中心性返流,Ⅰ级)2例,二尖瓣轻中度关闭不全(中心性返流,Ⅰ~Ⅱ级)1例;感染性心内膜炎、二尖瓣后叶穿孔伴P3赘生物形成、二尖瓣前叶A2~A3脱垂伴重度关闭不全(偏心性返流,Ⅳ级)1例;原发性二尖瓣退变或脱垂11例,其中中度关闭不全(偏心性返流,Ⅲ级,A2脱垂)1例,中重度关闭不全(偏心性返流,Ⅲ~Ⅳ级,后叶脱垂1例,A2~A3脱垂1例,A3脱垂1例)3例,重度关闭不全(偏心性返流,Ⅳ级,P2脱垂2例,A2脱垂3例)5例,重度关闭不全(中心性返流,Ⅳ级,瓣环扩大)2例;合并主动脉瓣轻度关闭不全1例;伴有三尖瓣关闭不全11例,其中轻度7例,中度3例,重度1例;伴有肺动脉高压11例,其中中重度3例。左心房内径(left atrial dimension,LAD)33~57(42.40±6.78)mm,左心室舒张末期内径(left ventricular end diastolic dimension,LVEDD)28~64(50.65±8.52)mm,左心室射血分数(ejection fraction,EF)48%~81%[(67.95±6.88)%],短轴缩短率(fractional shortening,FS)25%~50%[(38.00±5.36)%]。心电图提示窦性心律18例,其中窦性心动过缓4例,窦性心动过速1例,不完全性右束支传导阻滞4例,左前分支传导阻滞1例,频发室早1例,左室高电压2例;心房颤动2例。胸部X线片提示心影不同程度增大,双肺淤血或多血改变,肺动脉段明显膨隆3例。下肢股动、静脉血管彩超未见明显异常。9例50岁及以上患者常规行冠状动脉造影术,1例患者提示冠状动脉粥样硬化,前降支近段狭窄30%,回旋支近段狭窄40%。术前心功能(NYHA)Ⅱ级6例,Ⅲ级14例。合并高血压病1例,中度贫血2例。本研究经四川省医学科学院·四川省人民医院医学伦理委员会审核批准,所有患者自愿参加本研究并签署知情同意书。
1.2 手术方法 采用静吸复合麻醉,双腔气管导管插管;贴好体外除颤电极片,并放置经食道心脏彩超探头;取仰卧位,右侧肩部垫高20°~30°,右上肢悬吊在头架上。全身肝素化,右侧腹股沟韧带下缘纵行2.0~3.0 cm长小切口,分离股动、静脉(仅需游离血管前壁), 5-0 Prolene线荷包缝合,股动脉穿刺植入16~22F插管(Edwards),股静脉穿刺植入24~28F插管建立外周体外循环。左侧单肺通气,按张晓慎等[4]报道的方法分别在右前胸壁第3~5肋间隙戳3个1.0~4.0 cm孔(主操作孔、辅助操作孔、胸腔镜孔),各戳孔均使用切口保护套保护,在全胸腔镜下进行外科操作。进胸后,在膈神经前方切开心包,上至心包主动脉返折处,下达心包膈面并向上翘2.0 cm,使用缝线悬吊心包充分暴露升主动脉及心脏(通常膈神经侧心包悬吊4针,对侧悬吊2针)。用特制肾蒂钳经主操作孔套下腔静脉阻断带,并从胸腔镜孔引出;用小直角钳经辅助操作孔套上腔静脉阻断带,4-0 Prolene线荷包缝合上腔静脉,植入16F铁头直角上腔静脉插管,并经辅助操作孔引出。3-0 Prolene短针线荷包缝合升主动脉根部,插入冷灌针,并经辅助操作孔引出。降温至肛温32℃~34℃时,使用Chitwood阻断钳经辅助操作孔从横窦处阻断升主动脉,经主动脉根部顺灌停跳液进行心肌保护(间隔20 min灌注1次)。经房间沟切口进行二尖瓣手术操作,经右心房壁切口进行房间隔缺损修补、左心房黏液瘤切除及三尖瓣手术操作。
1.2.1 二尖瓣手术 主操作孔选择右侧锁骨中线外第4肋间隙,见图1。经房间沟切口进入左心房,并通过该切口放入左心引流管,使用心房拉钩拉开左心房壁,暴露二尖瓣,行心内探查,确认二尖瓣病变情况(瓣环、瓣叶、腱索、乳头肌);若二尖瓣赘生物形成,则先清除二尖瓣赘生物;若需要封闭左心耳者使用5-0 Prolene线连续双层缝闭左心耳内口。首先注水了解二尖瓣返流情况,需要加人工腱索的患者,先用Gore-Tex CV-4缝线带垫片缝至相应乳头肌上,再缝至对应瓣叶缘,打一活结,待加用成形环后根据试水情况,确认人工腱索长度后再打结固定(可调节人工腱索技术);瓣叶冗长者,使用5-0 Prolene缝线折叠瓣叶,尽量不切除瓣叶;瓣叶短小,对合缘不足者,取自体心包片,使用5-0 Prolene缝线与相应瓣缘缝合加宽瓣叶;交界脱垂伴返流,瓣环足够大者,使用5-0 Prolene缝线缝合封闭交界;荷包线间断缝合二尖瓣瓣环,测量瓣环大小,选用26~32 mm Edwards 4450或5200成形环,下环后缝线打结;术中需要反复多次注水观察二尖瓣闭合情况,根据瓣叶闭合情况制定后续手术方式,并确认成形效果。然后予以3-0 Prolene线连续双层缝合房间沟切口;同期行三尖瓣成形术患者,使用4-0 Prolene线悬吊右心房壁,然后切开右心房壁,心房拉钩拉开右心房壁,暴露三尖瓣,心内探查后,间断缝合三尖瓣瓣环,植入Edwards MC3成形环,并注水检查成形效果,4-0 Prolene线连续双层缝合右心房壁切口,开放上、下腔静脉阻断带。
1.2.2 房间隔缺损修补或左心房黏液瘤切除或三尖瓣手术 主操作孔选择右侧胸骨旁第4肋间隙,见图2。4-0 Prolene线悬吊右心房壁,然后切开右心房壁,先切除左心房黏液瘤(瘤体在胸腔内立即放人硅胶袋,通过主操作孔取出),4-0 Prolene线悬吊房间隔,充分暴露二尖瓣,通过房间隔缺损或房间隔切口行二尖瓣成形术;然后行三尖瓣成形术,通过三尖瓣瓣环缝线牵拉右心房壁暴露房间隔缺损(黏液瘤基底切除后造成房间隔缺损),采用自体心包片连续缝合修补房间隔缺损,4-0 Prolene线连续双层缝合右心房壁切口,开放上、下腔静脉阻断带。
1.2.3 结束 复温,心脏充分排气后,开放Chitwood阻断钳,冷灌针接管持续倒吸引,心脏复跳(需安置心脏临时起搏电极的患者,通常在心脏复跳前在右心室游离壁缝置心脏临时起搏导线阴极,然后在胸壁缝合阳极),心脏各切口彻底止血,辅助循环满意后,试停体外循环,经食道心脏彩超进行心内探查,确认二尖瓣成形效果(跨瓣压差、返流面积),若超声提示二尖瓣返流面积超过2.0 cm2,则重新转机阻断,进行二尖瓣成形术;之后再拔除胸内上腔静脉插管、冷灌针、股静脉插管,鱼精蛋白中和肝素后拔除股动脉插管。间断缝合心包切口;经胸腔镜孔放置引流管,缝合胸壁各孔及腹股沟处切口。术毕,用血液回收机回收创面渗血及体外循环机内余血,并回输体内。
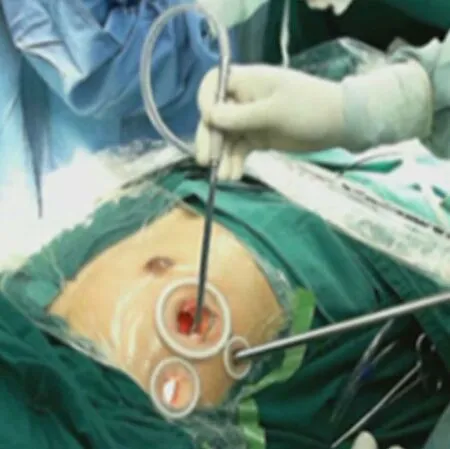
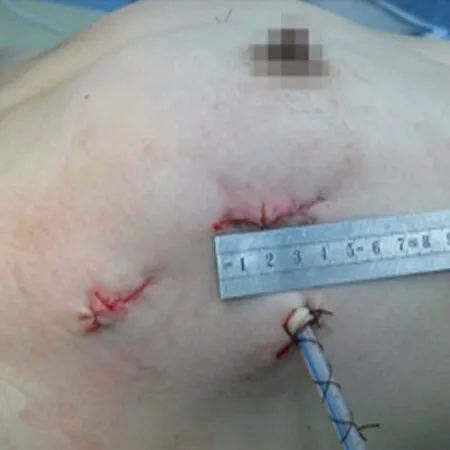
图1 二尖瓣手术入路

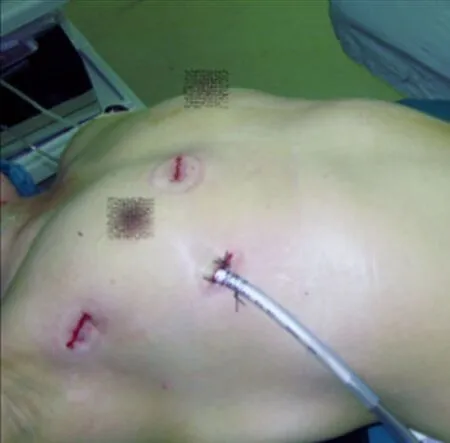
图2 房缺或左心房黏液瘤手术入路
1.3 随访 所有患者术后均通过门诊随访,了解心功能恢复情况,并口服华法林抗凝治疗6个月,定期检测凝血功能,维持国际标准化比值在1.8~2.2;术后3个月、6个月、12个月、18个月复查心脏彩超和心电图。随访截止时间为2017年9月。
1.4 统计学方法 应用SPSS 22.0软件进行统计分析,计量资料采用均数±标准差(x±s)表示,组间比较采用t检验;计数资料采用百分率(%)表示,组间比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结 果
2.1 手术情况 全组手术均顺利完成,无中转开胸。18例一次成形成功;2例患者成形后停机复查心脏彩超提示效果欠佳,二尖瓣返流面积分别为2.5 cm2和2.3 cm2,再次阻断后重新成形成功。术中所有患者均使用Edwards成形环,大小为26~32(28.30±1.75)mm;其余成形方法包括二尖瓣瓣叶折叠(4例)、交界缝合(3例)、人工腱索(10例)、心包补片(2例);同期行房间隔缺损修补5例、卵圆孔缝闭1例,三尖瓣成形10例(使用成形环9例,Kay′s成形1例)、右上肺静脉异位引流矫治(Warden手术)1例、左心房黏液瘤切除3例、二尖瓣赘生物清除1例、左心耳内口缝闭2例。
2.2 手术指标 患者手术时间200~370(259.50±48.88)min,体外循环时间88~219(148.15±41.17)min,主动脉阻断46~114(85.15±20.74)min;术中失血量50~200(132.50±56.84)mL,术后24 h胸腔引流量10~500(106.50±102.10)mL,胸腔引流管留置时间1~4(2.75±0.79)d,总输血量0~1200(206.00±202.70)mL(9例患者未输血,45%)。1例心包致密粘连患者术后引流量偏多,输入较多库血(1 200 mL);另有1例患者术后并发严重肺部感染、感染性休克,经联合抗感染后治愈。术后呼吸机辅助1~23(7.15±5.17)h,术后ICU停留18~47(26.50±9.62)h,术后住院7~28(9.70±4.51)d。全部患者无死亡,出院前复查心脏彩超提示二尖瓣未见明显狭窄或返流,无SAM现象。
2.3 随访结果 全组随访3~19(10.30±4.88)个月,无死亡。心功能恢复至Ⅰ级19例,Ⅱ级1例,较术前改善(P<0.05);随访心脏彩超提示二尖瓣轻度关闭不全1例,返流面积2.8 cm2,并伴有主动脉瓣轻度关闭不全;LAD和LVEDD比术前缩小(P<0.05)。见表1。

表1 患者手术前后指标比较 (n=20,x±s)
3 讨 论
二尖瓣成形术与二尖瓣置换术是治疗二尖瓣关闭不全的两种主要术式。目前普遍认为二尖瓣成形术能更好地保存左心室功能,减少心内膜炎、血栓栓塞和抗凝相关出血等并发症的发生,并可改善远期生存率,其在血流动力学、术后并发症和长期预后方面均优于置换术[5-7]。因此,二尖瓣成形术受到越来越多患者和心脏外科医生的青睐。传统的胸骨前正中入路行二尖瓣成形术,因其要锯开胸骨,破坏胸廓的稳定性,手术创伤大、失血多,术后恢复慢,且并发症发生率较高,已逐渐被微创二尖瓣成形术取代[8]。微创二尖瓣成形术包括胸骨部分切开、右胸小切口、胸腔镜辅助右胸小切口、全胸腔镜或机器人辅助、经皮介入二尖瓣成形术等。国外较多地进行机器人辅助二尖瓣成形术,国内由于经济水平相对落后和微创技术学习曲线相对较长的原因,大多进行右胸小切口或胸腔镜辅助右胸小切口二尖瓣成形术[9-11]。
二尖瓣成形的发展主要源于对二尖瓣结构的理解,以及外科技术的进步[12]。二尖瓣成形术的效果很大程度上取决于瓣膜功能不全的病因和病理结构,成人患者可修复的病变包括退行性、风湿性、功能性和感染性心内膜炎等[13-14]。退行性二尖瓣病变成形成功率高,且远期效果更好;风湿性二尖瓣病变因病理类型复杂多变,使其修复变得困难,且明显影响其远期效果。术者应根据二尖瓣病变的病因和病理结构变化,选择合适的成形技术。本组接受二尖瓣成形术的患者中退行性病变占55%(11/20),功能性病变占40%(8/20),感染性心内膜炎占5%(1/20)。未选择风湿性二尖瓣病变,与我们早期开展,经验相对不足有关。
二尖瓣成形术方法多样,手术需遵循两个基本原则:①恢复二尖瓣瓣叶良好的对合。经典的方法有矩形或三角形瓣叶部分切除、缘对缘缝合、腱索转移、人工腱索重建[15-16]。由于腔镜下进行瓣叶切和缝的操作相对较困难,通常我们采用相对简单的瓣叶交界缝合、瓣叶折叠、可调节人工腱索重建的方法来恢复瓣叶的良好对合。②矫正扩张的二尖瓣瓣环。瓣环成形是整个二尖瓣成形术的一部分,通常使用成形环来纠正瓣环扩张,增加瓣叶对合面积,并预防瓣环的进一步扩张。成形环可以是软环或硬环,全环或半环。研究表明,运用全硬环进行二尖瓣成形术,其远期效果更好[17-18]。本组20例均使用全硬环,平均大小为28.30 mm,平均随访10.30个月,除1例出现轻度二尖瓣关闭不全外,未见二尖瓣狭窄和SAM现象,成形效果良好。术后二尖瓣的病理性返流消失或明显减轻,使得LAD和LVEDD比术前缩小(P<0.05)。本组患者术后EF和FS较术前降低(P<0.05),可能和体外循环导致的术后早期心脏损害有关,但患者自身症状明显减轻,心功能较术前改善(P<0.05)。
无论采取哪种成形方法,精确的超声评估和良好的视野暴露是手术成功的关键[19-20]。本组患者术前超声均由彩超医生和外科医生共同完成,然后制订手术方案;术中再根据食道超声结果和手术探查所见,进一步优化成形方案;术毕通过TEE评价效果。患者通过外周血管建立体外循环,胸壁戳孔,全胸腔镜下进行二尖瓣成形术,不仅能为术者提供一个清晰放大的手术视野,精确地暴露二尖瓣瓣膜及瓣下结构,使二尖瓣成形手术得以顺利实施;而且切口为孔洞,不撑开肋骨,不破坏胸廓稳定性,术中平均失血仅132.5 mL,术后平均输血仅206 mL(45%患者未输血),术后恢复快(平均术后住院时间仅9.7 d),更好地诠释了心脏外科微创理念,符合现代健康发展方向[21]。
综上所述,全胸腔镜二尖瓣成形术已日趋成熟,创伤小,出血和输血少,并发症少,术后恢复快,安全可靠,效果确切,值得临床推广应用。
参 考 文 献
[1] Coutinho GF,Antunes MJ.Mitral valve repair for degenerative mitral valve disease: surgical approach, patient selection and long-term outcomes[J].Heart,2017,103(21):1663-1669.
[2] Chiu KM,Chen RJ.Videoscope-assisted cardiac surgery[J].J Thorac Dis,2014,6(1):22-30.
[3] Akowuah E,Burdett C,Khan K,et al.Early and Late Outcomes After Minimally Invasive Mitral Valve Repair Surgery[J].J Heart Valve Dis,2015,24(4):470-477.
[4] Zhang XS,Guo HM,Liu J,et al.Surgical incision in complete video-assisted mitral valve replacement[J].South China Journal of Cardiology,2014,15(2):99-105.
[5] McCluer RS,Cohn LH,Wiegerinck E,et al.Early and late outcomes in minimally invasive mitral valve repair:an eleven-year experience in 707 patients[J].J Thorac Cardiovasc Surg,2009,137(1):70-75.
[6] Lazam S,Vanoverschelde JL,Tribouilloy C,et al.Twenty-Year Outcome After Mitral Repair Versus Replacement for Severe Degenerative Mitral Regurgitation:Analysis of a Large,Prospective,Multicenter,International Registry[J].Circulation,2017,135(5):410-422.
[7] Altarabsheh SE,Deo SV,Dunlay SM,et al.Meta-Analysis of Usefulness of Concomitant Mitral Valve Repair or Replacement for Moderate Ischemic Mitral Regurgitation With Coronary Artery Bypass Grafting[J].Am J Cardiol,2017,119(5):734-741.
[8] Muneretto C,Bisleri G,Bagozzi L,et al.Results of minimally invasive, video-assisted mitral valve repair in advanced Barlow′s disease with bileaflet prolapsed[J].Eur J Cardiothorac Surg,2015,47(1):46-50.
[9] Navarra E,Mastrobuoni S,De Kerchove L,et al.Robotic mitral valve repair:a European single-centre experience[J].Interact Cardiovasc Thorac Surg,2017,25(1):62-67.
[10] 王怡轩,陈 思,刘金平,等.右胸小切口与标准胸骨正中切口在心脏瓣膜成形术中的比较研究[J].心血管外科杂志(电子版),2016,5(2):56-62.
[11] 赵 东,王春生,朱仕杰,等.41例电视胸腔镜辅助下微创二尖瓣成形术[J].复旦学报(医学版),2014,41(3):362-364,373.
[12] Ramlawi B,Gammie JS.Mitral Valve Surgery:Current Minimally Invasive and Transcatheter Options[J].Methodist Debakey Cardiovasc J,2016,12(1):20-26.
[13] 张 明,王 勇,童继春,等.二尖瓣成形术的临床应用[J].中国现代医学杂志,2013,23(7):68-71.
[14] Ito T,Maekawa A,Hoshino S,et al.Three-port (one incision plus two-port) endoscopic mitral valve surgery without robotic assistance[J].Eur J Cardiothorac Surg,2017,51(5):913-918.
[15] Borger MA,Kaeding AF,Seeburger J,et al.Minimally invasive mitral valve repair in Barlow's disease:Early and long-term results[J].J Thorac Cardiovasc Surg,2014,148(4):1379-1385.
[16] Ito T.TECHNIQUES IN MITRAL VAVLE REPAIR VIA A MINIMALLY INVASIVE APPROACH[J].Nihon Geka Gakkai Zasshi,2016,117(2):120-123.
[17] Venner C,Huttin O,Fiore A,et al.Treatment of Mitral Valve Regurgitation with an Open Rigid Annuloplasty Ring[J].J Heart Valve Dis,2016,25(3):332-340.
[18] Ryomoto M,Mitsuno M,Yamamura M,et al.Physiological mitral annular dynamics preserved after ring annuloplasty in mid-term period[J].Gen Thorac Cardiovasc Surg,2017,65(11):627-632.
[19] 杨智利,陈 莉,胡杨柳,等.食管超声心动图在人工腱索二尖瓣成形术的应用[J].中国现代医学杂志,2014,24(33):98-101.
[20] Greco E,Rose D,Irace F,et al.Optimizing the exposure in minimally invasive mitral surgery:a new left atrial retractor system[J].J Thorac Dis,2016,8(12):3728-3732.
[21] 黄国勇,黄爱兰,张学刚,等.完全胸腔镜下心脏手术的体外循环管理[J].微创医学,2017,7(4):364-366.

