化学发光微粒免疫分析技术检测血清人绒毛膜促性腺激素β亚基的性能评估
黄学强 李进贵
红寺堡区人民医院于2017年1月购进一台日本东曹AIA-2000 ST全自动化学发光免疫分析仪,该设备采用双波长,将检测信号和背景信号分开,使抗原抗体反应检测、B/F分离、酶反应荧光测定的全部工序都在同一杯中完成,将污染的可能性降到最低。该设备试剂按每人份独立冰冻干燥状态密封包装,试剂不易挥发失效,可避免交叉污染;因不存在试剂针,所以也不存在试剂间的交叉污染,可用于定量测定人血清和血浆中的病毒抗原、抗体等成分[1]。
本实验室根据原国家卫生部颁发的《医疗机构临床实验室管理办法》[2]和CNAS-CL02《医学实验室质量和能力认可准则》(ISO 15189:2012)[3]的要求,结合实际工作环境,对AIA-2000 ST全自动化学发光免疫分析仪的重复精密度、期间精密度、正确度、线性范围(可报告范围)和参考区间进行验证和评价,报告如下。
1 材料和方法
1.1 主要材料 日本东曹AIA-2000 ST全自动化学发光免疫分析仪;科大创新SC-3614型普通离心机;人绒毛膜促性腺激素β亚基(human chorionic gonadotropin β,β-HCG)检测试剂盒(荧光磁微粒酶免法),由东曹(上海)生物科技有限公司生产,试剂批号为HYR71A1,使用期限为2018年11月;G8U0015;G8U0035复合质控品(Level 1、Level 3水平);定标液(Cal 1、Cal 2)。
1.2 方法 按本室标准操作程序(standard operating procedure,SOP)对AIA-2000 ST仪器执行每日保养流程,在质控结果可受控、检测系统处于优良状态的条件下,进行实验操作[4]。
1.2.1 精密度验证
1.2.1.1 重复精密度 在条件稳定的情况下,按照常规程序在2 h内分别对高、低浓度的2个质控标本连续重复检测20次。记录检测结果,判断上述20个独立结果之间的一致程度。计算其重复精密度的变异系数(coefficient of variation,CV)和标准偏差(standard deviation,SD),得到重复性精密度。
1.2.1.2 期间精密度 在条件稳定的情况下,按照常规程序在2 h内分别对高、低浓度的2个质控标本(东曹复合质控Level 1、Level 3水平)各检测4次,连续检测5 d。记录检测结果,判断上述20个独立结果之间的一致程度。计算其期间精密度的CV值和SD值,得到重复性精密度。
1.2.2 正确度验证 评价仪器的测试结果与接受参考值之间的一致程度,采用定标液Cal 1、Cal 2的标本作为验证标本,通过实验室检测数据的偏倚验证和评价实验室检测结果的准确性。
1.2.3 生物参考区间验证 从我院选取20份体检合格的健康人群的标本作为验证标本,通过AIA-2000 ST检测系统进行测定,整理分析检测结果,并与厂家提供的参考区间进行比较。若所提供的标本中观察值在原始报告区间之外的标本≤2份,说明厂家提供的参考区间的实验报告是可以接受的,可以在临床使用[5]。本实验说明书的参考区间为<0.05 IU/L。
1.2.4 线性范围验证 用于验证线性范围的标本类型应与临床测试所用的标本类型相同或相似,所有标本均不应含有厂家所标定的干扰因素(如溶血、黄疸、脂血等)。选取高值和低值血清标本各1份〔尽量靠近试剂说明书的线性高值(H)和低值(L)〕,将H和L样品分别按5L、4L+1H、3L+2H、2L+3H、lL+4H、5H的比例配制混合成系列评价样品,每个浓度重复测定3次。将各浓度均值进行线性回归分析,判断测量值与预测值是否呈线性关系,从而保证该浓度范围检测结果的准确性。
2 结果
2.1 精密度验证结果 血清β-HCG的Level 1低浓度质控品CV批内=1.21%,CV期间=2.9%;Level 2高浓度质控品CV批内=3.78%,CV期间=3.8%。各项目实际CV<1/4上海市临床检验中心要求的实验室允许总误差(TEa),并且均低于厂家声明的CV值,说明精密度通过验证。见表1~2。
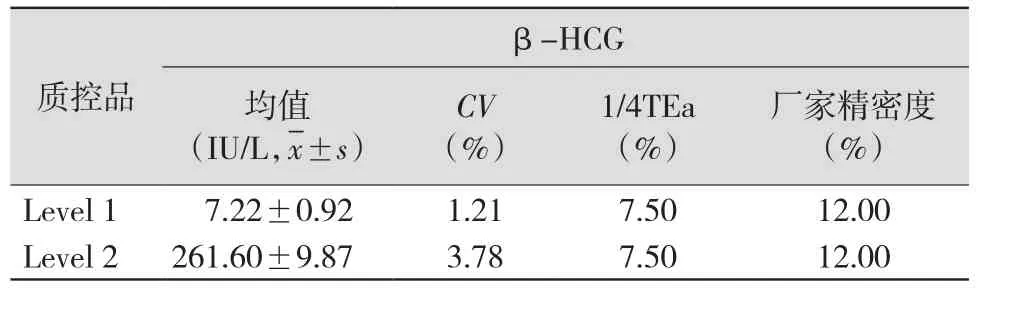
表1 两种不同浓度水平质控品的批内精密度验证结果
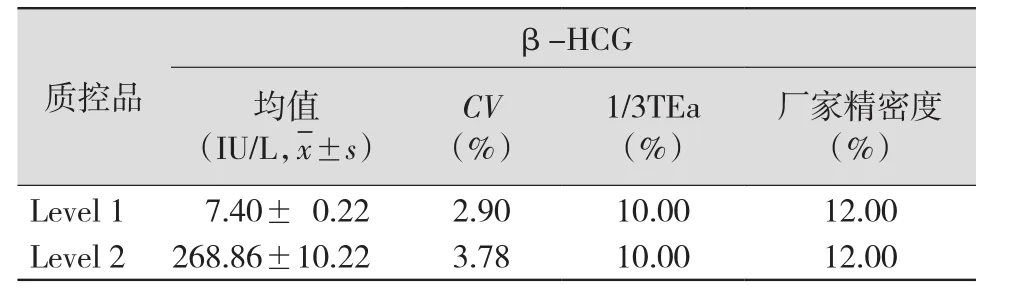
表2 两种不同浓度水平质控品的期间精密度验证结果
2.2 正确度验证结果 通过检测厂家提供的2份样本,计算实测值定标液Cal 1、Cal 2的偏倚,与偏倚范围比较,判断偏倚是否可以接受〔≤1/2TEa(15%)〕。检测结果均在要求范围内,表明准确度通过验证,见表3。
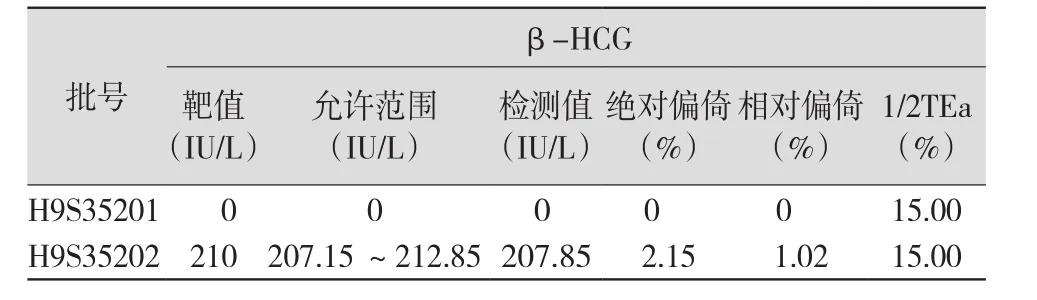
表3 两份不同批号样本的准确度验证结果
2.3 参考区间验证结果 我室20份标本的检测结果均在验证区间内(<0.5 IU/L),在厂家声明的参考区间之外的结果均为0,故本实验室参考区间通过验证。见表4。

表4 参考区间验证结果
2.4 线性范围验证结果 参考线性范围的要求,根据Y=0.996 3X-1.509 5计算,验证结果的斜率a为 1.00±0.05,相关系数 R2≥0.995,线性范围通过验证。见表5。
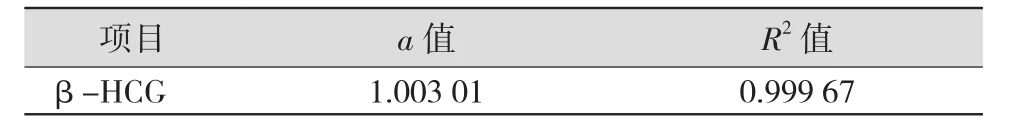
表5 线性范围验证结果
3 讨论
根据ISO 15189的相关要求,仪器设备项目在应用于临床之前,都需要对其检验方法和相关程序进行分析性能验证,内容应包括精密度、正确度、线性范围和参考区间。我院在2017年引进一台日本东曹AIA-2000 ST全自动免疫分析仪,厂家的性能参数是在其合适的环境下测定得到的,与本实验室实际的外部条件存在一定差异。因此本实验室在使用AIA-2000 ST进行日常检测前,必须要对其分析性能进行验证和评价[6]。
精密度是指在规定的条件下,重复检测样本的结果一致程度,主要评价仪器的重复性,是检测系统的基本分析性能指标之一。通过检测结果分析比较,AIA-2000 ST分析仪检测β-HCG的CV批内和CV批间均低于厂家要求的7.5%和10%;说明该仪器检测的重复性好。计算实测值的项目定标液Cal 1、Cal 2的偏倚,检测结果与靶值的相对偏倚为0%~1.02%;正确度≤15%,满足正确度验证结果的要求;线性范围验证结果表明β-HCG测量值与预期值的相关系数R2≥0.995,β-HCG所涉及的浓度范围(0.5~400 IU/L)呈线性关系,两者相关性较好,符合临床预期要求。若实际测量样本含量>400 IU/L,需要使用样本稀释模式对其进行稀释,然后再测量具体的含量。我们对收集的20例健康人群的血清标本进行了及时检测,要求其年龄、性别等均匀分布,对参考范围进行验证,得到AIA-2000 ST分析仪测定其β-HCG的数值均<0.5 IU/L,参考区间与厂家声明一致[7]。
综上所述,本实验对日本东曹AIA-2000 ST全自动免疫分析仪检测血清β-HCG的精密度、正确度、线性范围和参考区间进行验证和评价,各项结果与厂家声明的分析性能基本一致,能够为临床提供详细、可靠、准确的检测数据。
1 贺敏.孕酮化学发光免疫分析方法的建立[J].标记免疫分析与临床,2017,24(7):812-815.
2 中华人民共和国卫生部.卫生部关于印发《医疗机构临床实验室管理办法》的通知(卫医发[2006]73号)[EB/OL].http://www.nhfpc.gov.cn/zwgk/wtwj/201304/f4d5cbc861fd43bb928d6ea124f8 7a19.shtml.
3 中国合格评定国家认可委员会.CNAS-CL02医学实验室质量和能力认可准则(ISO 15189:2012)[EB/OL].https://www.cnas.org.cn/images/rkgf/sysrk/jbzz/2013/12/20/1C3A61EEC69A825B0FD01E CD986D9B78.pdf
4 孙庆燕,张娟,殷婧婧.肾素、醛固酮化学发光定量检测法的性能验证及其对原发性醛固酮增多症筛查作用探讨[J].中国实用医药,2018,13(1):74-75.
5 李家明,赖语扬,徐成坤,等.全自动血凝仪CA-7000性能及生物参考区间的验证与评价[J].实用检验医师杂志,2017,9(4):220-224.
6 朱为刚,曾劲峰,李彤,等.一种化学发光检测试剂在血液筛查中的应用评估[J].中国输血杂志,2016,29(6):581-583.
7 陈海明,王前明,赵元勋.日立7600全自动生化分析仪的分析性能验证[J].国际检验医学杂志,2015,36(20):2983-2986.

