基于决策树模型对我国6种保肝药物治疗药物性肝损伤的成本-效果分析
田艳平,崔向丽,刘丽宏,张长平(.首都医科大学附属北京朝阳医院药事部,北京 0000;.首都医科大学附属北京佑安医院药学部,北京 00069)
药物性肝损伤(drug-induced liver injury,DILI)是临床常见的药品不良反应之一。保肝治疗是药物性肝损伤治疗的一部分,保肝药物的种类较多,目前临床选择多以治疗经验为主,随着循证医学的发展,保肝药物治疗DILI的系统研究逐渐深入,多项系统评价表明保肝药物治疗DILI的疗效和安全性均较好。药物经济学(pharmacoeconomy,PE)是运用经济学原理和方法在药物治疗领域中的具体应用,是可从一系列用药方案中选择、判断出最优方案的有效工具[1]。本文通过构建PE评价模型,对临床常用的保肝药物注射剂进行PE分析,以期为临床选择具有成本-效果优势的保肝药物提供参考。
1 资料和方法
1.1 研究对象
参考国家基本医疗保险/工商保险和生育保险药品目录(2017年版),选择对于肝和胆治疗药中疗效肯定,且已普遍用于临床的6种保肝药物的注射剂,包括异甘草酸镁注射液(100 mg·次-1,qd,61.12元·d-1,正大天晴药业集团股份有限公司)、多烯磷脂酰胆碱注射液(465 mg·次-1,qd,38.36元·d-1,成都天台制药有限制药)、注射用还原型谷胱甘肽(1.2 g·次-1,qd,25.4元·d-1,重庆药友制药有限责任公司)、注射用复方甘草酸苷(100 mg·次-1,qd,46.7元·d-1,瑞阳制药有限公司)、注射用硫普罗宁(200 mg·次-1,qd,20.05元·d-1,悦康药业集团有限公司)、甘草酸二铵注射液(150 mg·次-1,qd,9.6元·d-1,正大天晴药业集团股份有限公司)。
1.2 文献检索
检索数据库包括:中文期刊全文数据库、维普数据库及万方数据库。检索时间为建库至2018年2月。检索关键词为药物性肝损伤、药物性肝损害、药物性肝炎、肝损伤、肝损害、异甘草酸镁、多烯磷脂酰胆碱、还原型谷胱甘肽、复方甘草酸苷、硫普罗宁、甘草酸二铵;匹配度为模糊。
1.3 文献纳入及排除标准
纳入标准:(1)以上6种药物治疗DILI的随机对照临床研究。(2)为保证成本核算的一致性,厂家和给药剂量均一致。(3)疗程为4周。(4)疗效判断标准[2]:显效:临床症状消失,血清生化指标恢复正常;有效:临床症状消失(或改善),血清生化指标较之前明显好转;无效:治疗后血清生化指标无明显变化或未达到上述显效。排除标准:(1)非RCT研究;(2)口服药物保肝治疗方案者;(3)联合用药治疗方案;(4)重复文献;(5)不符合上述入选标准。
1.4 文献筛选和质量评价
2名研究者分别单独根据本研究设定的纳入及排除标准筛选文献,如有分歧则请第3位研究者协商解决。根据Jadad改良法[3]对文献是否使用随机方法、盲法、基线相似性及失访退出等指标进行质量评分。先由2名研究者各自单独评分,然后互相核对,如有分歧,两人讨论或请第三方仲裁决定。其中随机、分配隐藏和双盲分别占2分;退出或失访描述为1分,未进行描述者为0分,总分在4分以下提示文献质量较低。
1.5 模型结构
决策树模型是经济学评价中最常见的决策模型,决策树模型属于静态模型[4],静态模型通常适用于病程较短的急性疾病或者病情不太复杂的疾病,能够反应事件与决策时间变化而产生的各种后果。本研究纳入的文献均为急性DILI,疗程较短,治疗方案逻辑简单,适合采用决策树模型进行分析。采用TreeAge Pro 2011软件进行决策树模型的构建,对6种保肝药物注射剂进行成本效果分析,基于文献资料的疗程确定本研究的模型跨度时间为4周,本研究决策树模型图如图1所示(□决策出发点;○状态点;△效果值)。
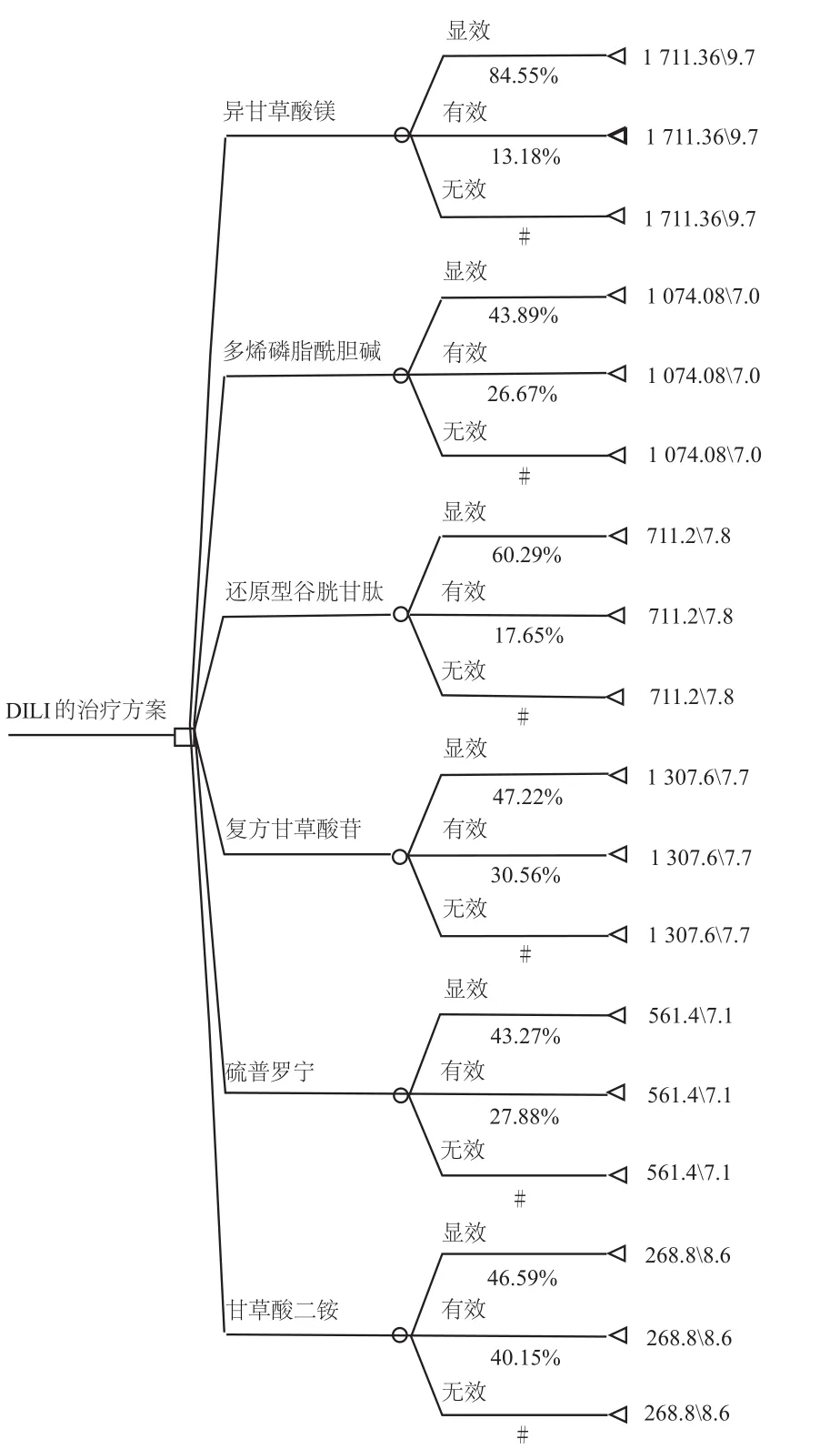
图1 决策树模型图Fig 1 Decision tree model structure
模型参数:(1)率值参数:检索共计14篇文献,病例总数944例[5-18],对文献中的显效率、有效率、无效率进行Meta分析,获得率值参数。(2)效果参数:治疗效果在PE评价中指的是疾病治疗的终末状态,患者在经过治疗后达到痊愈或病情稳定情况,若进行定量分析,则需对治疗结果加以赋值[19],本研究咨询了临床肝病专家和药物经济学研究者共同决定以治疗总有效率为基准[20]。(3)成本参数:本次研究从医疗系统角度出发,为避免数据偏差,本着经济学保守原则,本研究仅计算6种治疗方案的药品直接成本。由于本研究的时间较短,并未进行贴现处理。详见表1(率值参数来源于Meta分析,效果参数来源于专家意见,药品费用来源于北京市医药阳光采购综合管理平台实时药品价格)。

表1 模型参数Tab 1 Parameters used in the decision model
1.6 统计学处理
决策树模型的建立和分析采用TreeAge Pro2011软件。本研究采用成本-效果分析(cost-effectiveness analysis,CEA)和增量成本效果比(the incremental cost-effectiveness ratio,ICER)。CEA是药物经济学评价中的主要分析方法之一;ICER则是成本效果分析中最常用的分析指标,表示各种干预情况下获得单位效果值所需增加的费用。
2 结果
2.1 文献质量评价结果
参考Jadad改良法的评分标准,在纳入的14篇文献中,仅有2篇文献描述随机序列产生的方式[12-13],其余文献都没有清楚地描述随机序列的产生方式、如何分配隐藏的、是否进行了盲法、撤出与退出详细情况,因此这14项研究皆为低质量研究。
2.2 经济学评价结果
2.2.1 以效果为产出的CEA分析 结果显示,6种保肝药物注射剂对DILI效果均显著,经济学分析显示,6种治疗方案中,相比甘草酸二铵方案,复方甘草酸苷、多烯磷脂酰胆碱、硫普罗宁、还原型谷胱甘肽效果更低,成本更高,为绝对劣势策略,具体情况见图2。优势方案中,异甘草酸镁效果值(9.7)优于甘草酸二铵(8.6),异甘草酸镁CEA(176.43)高于甘草酸二铵(31.26),ICER为1 311.42。详见表2。

图2 成本-效果边界图Fig 2 Cost-effectiveness eff i ciency frontier

表2 以效果为产出的成本-效果分析结果Tab 2 Cost-effectiveness analysis of 6 groups based on effect values
2.2.2 以显效率为产出指标的成本-效果分析 患者肝功能的恢复情况会影响治疗的依从性,患者肝功能的各项指标完全恢复正常,将会促进患者足量足疗程的完成DILI的治疗方案,因此显效率作为DILI治疗方案的评估指标更具有临床意义,从表3可以看出,异甘草酸镁显效率最高(84.55%),CEA为2 024.08,ICER为4 122.67,详见表3。

表3 以显效率为产出的成本-效果分析结果Tab 3 Cost-effectiveness analysis of 6 groups based on excellence rate
2.3 敏感性分析
各种保肝药物的率值参数来源于文献的Meta分析结果,文献的纳入质量参差,显效率为影响率值参数的主要因素,因此本研究将每种治疗方案的显效率按“±10%”作为观察点,进行单因素灵敏度分析;另考虑药品价格下降是必然趋势,因此假定药品价格下降10%,进行单向敏感度分析。结果显示,显效率和药品价格2个参数对各治疗方案的成本效果排名没有影响,具体见表4 ~ 7。当药品成本下降10%,DILI治疗的显效率下降或上升10%后,敏感性分析结果与初始结果一致。

表4 以效果为产出指标的成本下降10%的敏感性分析结果Tab 4 Sensitivity analysis for a 10% reduction in costs of 6 groups based on effect values

表5 以显效率为产出指标的成本下降10%的敏感性分析结果Tab 5 Sensitivity analysis for a 10% reduction in costs of 6 groups based on excellence rate

表6 以显效率为产出指标的显效率下降10%的敏感性分析结果Tab 6 Sensitivity analysis for 10% reduction in excellence rate of 6 groups based on excellence rate
3 讨论
3.1 保肝药物治疗DILI机制
异甘草酸镁、甘草酸二铵以及复方甘草酸苷属于甘草酸类制剂,该类药物可改善各类肝炎所导致的血清转氨酶升高以及其他生化指标异常,明显减轻肝脏的病理损害[21],甘草酸能够改善对乙酰氨基酚引起的肝损伤。可以显著抑制对乙酰氨基酚所致的长链酰基肉碱水平的增加[22]。硫普罗宁分子中含有巯基,能降低肝细胞线粒体ATP酶的活性,升高细胞内ATP的含量,同时参与肝细胞的蛋白质、糖代谢,维持肝细胞内谷胱甘肽的浓度,抑制肝细胞线粒体过氧化脂质体形成,保护肝细胞膜[23]。还原型谷胱甘肽在对外源性物质的解毒,调节细胞增殖和凋亡、免疫功能等方面起着重要作用[24],外源性补充的还原型谷胱甘肽在酶催化下可直接与氧化损伤产生的自由基结合,从而抑制或减少自由基的产生,防止肝细胞持续损伤[25]。多烯磷脂酰胆碱作为肝细胞膜修复保护剂,调节肝脏的能量代谢、促进肝细胞的再生、减少氧应激和脂质过氧化、抑制肝细胞凋亡、降低炎症反应等,从多个方面保护肝细胞,促进肝脏组织的再生。

表7 以显效率为产出指标的显效率提高10%的敏感性分析结果Tab 7 Sensitivity analysis for 10% improvement in excellence rate of 6 groups based on excellence rate
3.2 保肝方案间的经济学比较分析
当多个方案进行经济学比较研究中,出现了效果较高、成本较高或效果较低、成本较低的情况下,无法直接判断方案的经济性,需要进行ICER的进一步的评价与分析,在此条件下需要引入成本效果阈值这一参数,也可以认为是增加一单位健康产出的最大支付意愿[26]。在6种治疗方案中,以效果为产出方案中,异甘草酸镁的疗效优于其他5种治疗方案;CEA异甘草酸镁最高,甘草酸二铵最低,与甘草酸二铵相比,异甘草酸镁的ICER为1 311.42。以显效率为产出计算,异甘草酸镁显效率最高,且成本-效果比低于多烯磷脂酰胆碱和复方甘草酸苷,与甘草酸二铵相比,硫普罗宁、复方甘草酸苷、多烯磷脂酰胆碱此三种药物为绝对劣势方案;甘草酸二铵、还原型谷胱甘肽、异甘草酸镁三种药物为优势方案。当增加一个单位健康产出的最大支付意愿值小于3 229.20元时,甘草酸二铵更具有经济性;当最大支付意愿值介于3 229.20元 ~ 4 122.67元时,还原型谷胱甘肽具有经济性;当最大支付意愿值大于4 122.67元时,异甘草酸镁具有较好的成本效果优势。因此临床医生在治疗DILI选择保肝药物时,可以根据患者个人意愿支付值来选择,呼吁医疗保健部门鼓励临床选择异甘草酸镁,并给予选择该药物的患者增加补贴,以提高整体的社会效益,对于经济条件有限、治疗预期低的患者,甘草酸二铵也可以作为一种选择。
敏感性分析是经济决策中常用的一种不确定性分析方法,对于经济学研究结果的可信度至关重要。本研究中药品的价格为影响结果敏感因素之一,随着医疗改革的深入开展,药品价格下降是必然趋势,因此,假定药品价格下降10%,对药品价格进行单因素敏感性分析;本研究纳入的文献参差,而显效率作为一个重要参数参与到成本-效果以及增量-成本效果的评价中,对显效率进行敏感性分析,将6种保肝药物的显效率分别增减10%作为观察点,进行单因素敏感性分析,经过灵敏度分析,药品价格和显效率对CEA和ICER的初始结果排序没有影响,说明了本研究结果的稳定性。
3.3 局限性
本研究存在的局限性:(1)本研究纳入的文献皆为中文文献,文献质量参差,故临床疗效的统计可能存在选择偏倚,通过单向敏感率分析来校正选择偏倚,以保证结果的可靠性;(2)本研究在成本核算方面,仅考虑了药物的直接成本,期待在以后的研究中,将考虑间接成本以及隐性成本在内的所有成本,同时从多个角度包括患者、医院以及医疗保险付费等方面来考虑药物经济学问题,希望未来开展更大规模、更精细的PE研究来评价保肝药物治疗DILI的疗效和经济性。
[1] 王爱华,唐红波,李心蕾,等.抗炎保肝药治疗药物性肝损伤的药物经济学评价[J].胃肠病学和肝病学杂志,2015,24(10):1232-1237.
[2] 杜世奇,焦栓林,秦建增,等.异甘草酸镁治疗慢性药物性肝损伤疗效分析[J].肝脏,2018,23(4):312-313.
[3] Jadad AR, Moore RA, Carroll D, et al. Assessing the quality of reports of randomized clinical trials: is blinding necessary?[J].Control Clin Trials, 1996, 17(1): 1-12.
[4] 李洪超.基于文献的药物经济学评价:方法和挑战[J].药学与临床研究,2016,24(2):188-191.
[5] 刘幸,陈洁.3种保肝药物治疗艾滋病人的药物性肝损伤的成本-效果分析[J].抗感染药学,2009,6(1):66-68.
[6] 王淮,龚天斌.3种常用改善肝功能药物治疗药物性肝损伤的效果比较[J].临床肝胆病杂志,2016,32(4):761-763.
[7] 杨松,张耀亭,殷建团.72例抗结核药物性肝炎的还原型谷胱甘肽治疗[J].临床肺科杂志,2006,11(6):765-766.
[8] 关荣,吴治龙.多烯磷脂酰胆碱联合还原型谷胱甘肽治疗化疗药物性肝损害的疗效观察[J].中国肿瘤临床与康复,2014,21(10):1181-1183.
[9] 郑于珠,张西,蒋莎莎,等.异甘草酸镁联合多烯磷酯酰胆碱治疗化疗药物性肝损害的临床疗效观察[J].中国医药指南,2013,11(23):668-669.
[10] 王新军,田丰.复方甘草酸苷治疗抗结核药物性肝炎的临床分析[J].中国社区医师,2012,14(7):85-86.
[11] 颜寒斌.甘草酸二铵联合硫普罗宁治疗抗结核药物所致中度肝损害的疗效观察[J].内蒙古中医药,2010,2:67-68.
[12] 路秀萍.还原型谷胱甘肽联合门冬氨酸钾镁治疗药物性肝炎临床观察[J].中国现代药物应用,2012,6(2):72-73.
[13] 杨惠卫,李冬雷,李润浦,等.抗痨药物致药物性肝损伤患者应用异甘草酸镁治疗的临床疗效[J].现代消化及介入诊疗,2016,21(4):578-580.
[14] 姜建国.异甘草酸镁注射液治疗药物性肝损伤的临床观察[J].中国医师进修杂志,2010,33(4):72-73.
[15] 聂琦,袁治,陶立轩,等.异甘草酸镁治疗抗结核药物性肝损害150例[J].实用药物与临床,2015,18(12):1488-1490.
[16] 张丽萍,刘幸,陈洁.三种保肝药物治疗结核病药物性肝损伤的成本-效果分析[J].中国民族民间医药,2010,19(7):46-47.
[17] 陈发明.用还原型谷胱甘肽联合多烯磷脂酰胆碱治疗急性药物性肝损害的效果研究[J].当代医药论丛,2015,13(15):163-164.
[18] 林跃平.复方甘草酸苷联合还原型谷胱甘肽治疗抗结核药所致肝损害的临床疗效分析[J].现代医药卫生,2011,27(9):1308-1309.
[19] 孔晓东.药物经济学:概念、方法和应用[J].国外医学·药学分册,1994,21(1):13-18.
[20] 陈婷,叶晓光.常用非酒精性脂肪性肝病药物治疗方案的药物经济学评价[J].肝脏,2017,22(9):794-799.
[21] Manns MP, Wedeyer H, SingerA, et al. Glycyrrhizin in patients who failed previous interferon alpha-based therapies: biochemical and histological effects after 52 weeks[J]. J Viral Hepat, 2012,19(8): 537-546.
[22] 甘草酸制剂肝病临床应用专家委员会.甘草酸制剂肝病临床应用专家共识[J].中华实验和临床感染病杂志(电子版),2016,10(1):1-9.
[23] 马俊,冯端浩.硫普罗宁治疗抗结核药致肝损害疗效的Meta分析与系统性评价[J].中国医院用药评价与分析,2011,11(5):390-393.
[24] Wang C, Wang W, Ma S, et al. Reduced glutathione for prevention of renal outcomes in patients undergoing selective coronary angiography or intervention[J]. J Interv Cardiol, 2015,28(3): 249-256.
[25] 张杨,沈素,程晟,等.223例注射用还原型谷胱甘肽临床使用情况分析[J].中国药物应用与监测,2017,14(3):173-176.
[26] 张楠,石学峰,吴晶.增量成本效果比在卫生技术评估中的应用[J].中国卫生政策研究,2012,5(2):64-68.

