经皮椎间孔镜联合动态固定与常规PLIF手术治疗腰椎退行性疾病的对比研究
王旭阳
(陕西省渭南市中心医院骨一科,陕西 渭南 714000)
经后路减压椎间植骨融合术 (posterior lumbar interbody fusion,PLIF)是治疗腰椎退行性疾病的经典手术方式,广泛应用于腰椎管狭窄症、腰椎间盘突出症等人群,其疗效确切,可达到充分减压和重建脊柱稳定性的效果[1]。但传统PLIF手术破坏了脊柱的正常生理结构,这种刚性融合固定方式丧失了手术节段的活动度,在后期易出现邻近节段退变(adjacent segment degeneration,ASD)、假关节形成等并发症,有研究报道其ASD发生率达到18.3%[2]。为了避免上述缺陷,近年来,以棘突间撑开装置(interspinal strutting device,IPD)为代表的动态非融合固定技术在在此类疾病手术中得以应用,在保障脊柱稳定性的同时,尽可能避免了传统刚性融合固定的弊端,其近期疗效已有较多文献予以肯定[3-4]。经皮椎间孔镜技术是进行髓核摘除、减压的最新微创手术,我科自2012年以来,尝试采用经皮椎间孔镜技术联合IPD治疗35例腰椎退行性疾病患者,经2年随访,近期疗效满意。现与同期行PLIF手术治疗的33例患者进行回顾性分组对比,以探讨其临床优劣。
1 临床资料
1.1 一般资料
回顾性分析2012-03-2015-03手术治疗的腰椎退行性疾病患者68例,其中男38例,女30例;年龄41-67岁,平均50.3岁;腰椎间盘突出症41例,腰椎管狭窄症27例;手术节段:L3-421例,L4-547例。根据手术方式的不同,将其分为两组:A组采用经皮椎间孔镜技术联合IPD(采用In-Space棘突间动力装置)治疗,共35例;B组采用PLIF手术治疗,共33例。两组患者的性别、年龄、疾病类型、手术节段等一般资料比较,差异均无统计学意义(P>0.05),见表1。

表1 两组腰椎退行性疾病患者的一般资料比较
1.2 选择标准
纳入标准:①腰椎退行性疾病患者,经术前X线、CT和MRI检查,有神经根管、中央管及椎间孔狭窄者;②患者有明确的腰背痛、伴一侧或两侧下肢放射痛,或间歇性跛行症状;③患者经3个月以上的保守治疗,无明显改善;④经其他微创手术治疗后,无效或再次复发者;⑤随访时间满足2年以上者。
排除标准:①拟手术节段有结核、肿瘤或感染等;②有腰椎峡部裂、伴有MeyerdingⅠ度以上的腰椎滑脱者;③有棘突或椎板发育异常者;④既往有腰椎手术史或外伤史者。
1.3 手术方法
两组患者均由同一组医师进行手术。A组:患者取俯卧位,以芬太尼辅助镇静;于G臂机透视确定手术间隙后,于后正中线旁开12-14 cm作进针点,局部麻醉后,作7 mm微切口,以10-20°角度将穿刺针穿刺进入病变间隙的纤维环处,G臂机透视见18号穿刺针侧位处于椎间隙后1/4处、正位处于椎间隙上关节突外侧缘处为佳。以22号穿刺针向椎间盘内注射造影剂和亚甲蓝,进行椎间盘造影和疼痛复制试验。经穿刺针置入导丝,沿导丝插入逐级扩张导管,经环锯扩孔建立工作通道,并确保工作套管插入纤维环2-3 cm处。插入椎间孔镜,摘除突出染色的髓核及周围组织,探查松解行走神经根与出口神经根,以射频热凝进行止血、纤维环皱缩成形后,拔除外套管。将椎间孔镜切口扩大至16 mm,侧位透视下插入导针,平行于终板垂直进入棘突间。透视确认导针位置处于棘突之间、且尽量靠近腹侧、处于小关节之上,正位透视见导针超过中线2 cm为宜。沿导针插入逐级扩张导管直至紧密接触棘突上下缘。在G臂机透视引导下,置入合适型号的In-Space棘突间动力装置系统,并通过2孔定位中线,将位置调整良好并打开侧翼。经G臂机再次透视确认位置良好、棘突间撑开满意后,冲洗切口,留置负压引流管,缝合切口,术毕。典型病例的手术前后影像学资料见图1-4。

图1:腰4-5突出症术前MRI;图2:术前CT片;图3-4:术后2年正侧位X线片,见椎间隙与椎间孔高度维持良好,内固定位置较佳,未见邻近节段退变加重
B组:患者全麻,取俯卧位,经透视确认手术节段后,作后正中切口,逐层分离肌肉、软组织,直至显露手术节段的椎板、棘突和小关节突,置入椎弓根钉,经G臂机透视确认螺钉位置良好。将手术节段棘突咬除,作全椎板减压,并将手术节段的上位椎体下关节突切除,作神经根管减压。彻底摘除手术节段髓核组织,对终板进行处理后,将术中切除的自体骨修剪成骨粒并填充入椎间融合器,将填满自体骨粒的融合器置入椎间前2/3处。安装好纵向连接杆并固定之,冲洗切口,置负压引流管,逐层缝合切口,术毕。
两组患者术后均以抗生素静脉滴注3-5 d;术后2 d内视引流情况拔除引流管。其中A组患者术后绝对卧床3 d,1个月后可去除腰围恢复正常活动;B组患者绝对卧床7 d,3个月后可去除腰围。
1.4 观察指标
(1)围手术期:对比两组患者的手术时间、术中出血量、住院时间和并发症情况。(2)分别采用视觉模拟评分(visual analogue scale,VAS)对患者腰腿痛进行评价,采用日常功能障碍指数(Oswestry disability index questionnaire,ODI)进行腰椎功能恢复的评价;评价时间为患者术前、术后3个月、1年和2年。(3)随访期间,测量患者手术和上邻节段的活动度(range of motion,ROM)。
1.5 数据处理
2 结果
2.1 手术情况
68例患者均顺利完成手术,其中B组2例出现硬脊膜撕裂,予以术中修补、术后改头低脚高体位等对症处理后好转;1例出现椎间隙感染,予以持续抗感染治疗3个月康复;2例患肢无力,均予以保守治疗6个月后恢复。A组中未见明显的围手术期并发症发生。两组患者的手术时间无显著性差异(P>0.05);但与B组患者相比,A组的术中出血量更少、住院时间更短,差异有统计学意义(P<0.05),见表2。
表2 两组腰椎退行性疾病患者的围手术期指标对比(±s)

表2 两组腰椎退行性疾病患者的围手术期指标对比(±s)
组别 例数 手术时间(min) 术中出血量(ml) 住院时间(d)A 组 35 115.2±17.4 53.7±9.2 7.6±1.5 B 组 33 119.6±21.3 351.9±41.8 11.2±3.6 0.935 41.178 5.438 0.353 0.000 0.000
2.2 VAS评分、ODI指数对比
两组患者术后3个月、1年和2年,其腰痛、腿痛VAS评分和ODI指数均较术前显著降低(P<0.05);A组术后3个月的腰痛VAS评分显著低于B组,差异有统计学意义(P<0.05),见表3内容。
2.3 腰椎活动度对比
与术前相比,两组患者术后2年的手术节段腰椎活动度均显著受限(P<0.05);且B组的上邻节段腰椎活动度较术前显著增加(P<0.05)。与B组相比,A组术后2年的手术节段活动度保持较好,且上邻节段活动度亦无显著增加(P<0.05),具体见表4。
表3 两组腰椎退行性疾病患者手术前后的VAS评分、ODI指数对比(±s)

表3 两组腰椎退行性疾病患者手术前后的VAS评分、ODI指数对比(±s)
注:与本组术前相比,*P<0.05;与B组相比,#P<0.05
组别 疗效指标 术前 术后3个月 术后1年 术后2年A组(35例)腰痛 VAS(分)6.18±0.51 2.43±0.62*#2.21±0.38*1.62±0.37*腿痛 VAS(分)7.63±0.74 2.68±0.72*2.27±0.55*1.94±0.33*ODI指数(%)64.25±8.57 19.24±6.38*20.16±5.02*20.47±6.14*B组(33例)腰痛 VAS(分)6.05±0.71 3.14±0.55*2.16±0.41*1.65±0.40*腿痛 VAS(分)7.58±0.94 2.73±0.62*2.29±0.46*1.96±0.26*ODI指数(%)63.91±7.46 19.38±5.27*20.24±6.18*20.35±5.71*
表4 两组腰椎退行性疾病患者手术前后的腰椎活动度对比(°,±s)
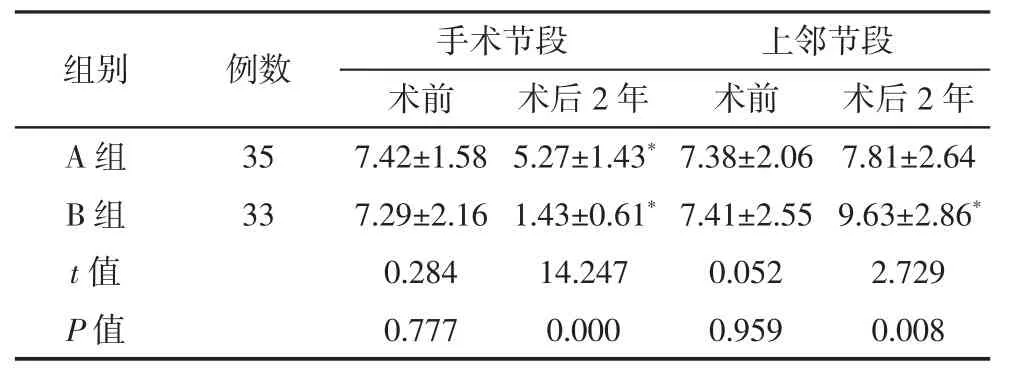
表4 两组腰椎退行性疾病患者手术前后的腰椎活动度对比(°,±s)
注:与本组术前相比,*P<0.05
组别 例数 手术节段 上邻节段术前 术后2年 术前 术后2年A 组 35 7.42±1.58 5.27±1.43*7.38±2.06 7.81±2.64 B 组 33 7.29±2.16 1.43±0.61*7.41±2.55 9.63±2.86*t值 0.284 14.247 0.052 2.729 P值 0.777 0.000 0.959 0.008
2.4 腰椎手术结局
随访期间,A组1例于术后1年再次复发,2例棘突骨折,均改行PLIF手术后好转;1例In-Space内固定器向后脱落,但未引起不良症状,总发生率为11.4%。B组1例融合失败,但未引起临床症状,未予处理;1例出现螺钉断裂,予以取出,总发生率为6.1%。两组随访期间的并发症总发生率对比,虽然A组略高于B组,但差异无统计学意义(X2=1.759;P>0.05)。
3 讨论
椎间孔镜技术是目前治疗腰椎退行性疾病的最新微创手术,仅需7-8 mm的手术切口即可建立工作通道,且经后外侧入路,避免了传统后正中入路对脊柱后柱结构的破坏,同时亦仅需局部麻醉即可开展,降低了神经根损伤的概率。孔镜技术最初应用于腰椎间盘突出症,但随着该技术的不断开展,目前已较成熟地用于腰椎管狭窄症等其他腰椎退行性疾病,并取得较好疗效[5]。
IPD是脊柱动态非融合技术的一种,通过将退变节段的棘突间隙撑开,并防止过度后伸,增加椎管横截面和椎间孔高度、椎间隙高度,减轻椎间盘和小关节的负荷,并控制异常活动,最大限度保持退变节段的活动度。目前,多数IPD装置在置入时需要破坏腰椎后方韧带结构和部分棘突骨质,术后有内固定松动、移位和棘突骨折等风险[6],而本研究所采用的In-Space棘突间动力装置,有如下明显优势:①可通过外侧入路置入,在操作过程中无需对棘突旁肌肉进行剥离、牵开操作,且无需切除棘突骨质,棘间韧带仅需穿孔即可,较好地保留了棘上、棘间韧带,有利于保留脊柱的后方解剖结构稳定性,术后失败概率亦明显减少[7]。本研究A组35例术后仅1例再次复发,2例棘突骨折,1例In-Space装置向后脱落,其发生率仅11.4%,显著低于相关文献报道的其他IPD装置。②In-Space装置可直接在原有的孔镜通道中微创置入,创伤性更小。
本研究基于In-Space装置的设计特点和安置条件,首先利用椎间孔镜技术进行减压操作,待孔镜操作完成后,将原切口扩大至16 mm,基于微切口即实现了In-Space装置的置入安装过程,与传统PLIF手术相比,其微创优势明显。本文中,采用本术式的A组手术出血量、住院时间均显著低于B组(P<0.05),也证实了这一点;另外,其术后腿痛VAS评分、ODI指数均与B组相近(P>0.05),提示其疗效与PLIF手术相近。在腰椎活动度对比中,A组手术节段术后腰椎活动度显著优于B组(P<0.05),得到了较好的保留;且其上邻节段腰椎活动度于术后并未见显著增加(P>0.05),而PLIF手术的B组却增加明显。上述结果均体现了微创孔镜技术联合In-Space棘突间动力装置治疗腰椎退行性疾病的优势所在。
[1]万仲贤,陈泽,李强,等.PLIF手术对退变性腰椎滑脱症脊柱骨盆参数影响及疗效分析[J].颈腰痛杂志,2016,37(5):416-420.
[2]管俊杰,石志才.后路腰椎椎间融合术对邻近节段退变的影响[J].脊柱外科杂志,2011,09(2):83-87.
[3]Ghiselli G,Wang JC,Bhatia NN,et al.Adjacent segment degeneration in the lumbar spine.J Bone Joint Surg (Am),2004,86-A(7):1497-1503.
[4]Rahm MD,HaII BB.Adjacentsegment degeneration after lumbar fusion with instrumentation:a retrospective study[J].J Spinal Disord,1996,9(5):392-400.
[5]王作伟,菅凤增,王兴文,等.经皮椎间孔镜技术治疗腰椎间盘突出症:椎间孔入路和椎板间入路的对照研究[J].中华神经外科杂志,2016,32(12):1214-1219.
[6]郑召民.棘突间固定装置应用10年再思考 [J].中国脊柱脊髓杂志,2014,24(10):870.
[7]农鲁明,周栋,高共鸣,等.In-Space经皮棘突间撑开系统治疗腰椎不稳症的初步效果分析[J].中华骨科杂志,2013,33(1):26-31.
——壮肾

