防风薄层色谱指纹图谱的建立及其方法学研究
廖华丽,丁冬梅,李 清
(1广东省食品药品职业技术学校药学系,广州 510663;2沈阳药科大学药学院;*
防风为伞形科植物防风Saposhnikoviadivaricata(Turcz.)Schischk.的干燥块根[1]。防风始载于《神农本草经》,列为草部上品[2]。《中国药典》2015年版收载的正品防风,习称关防风或北防风,产地主要是黑龙江、内蒙古、吉林、辽宁、河北、山东等省区[3],具有祛风解表、胜湿止痛、止痉的功能,主治感冒头痛、风湿麻痹、风疹瘙痒、破伤风[1]。防风作为大宗药材,临床应用安全有效,在众多中药复方制剂中发挥重要作用,例如,防风通圣丸[4]、玉屏风散[5]、痛泻要方[6]等。然而,由于防风存在的历史悠久,防风引种情况普遍,故而产地多,加之各地习用品众多,同名异物普遍存在,例如云防风[7]、水防风[8]、川防风、西北防风[9],它们在化学组成上有一定的差别[10],给临床用药的安全有效造成障碍。为此,已有文献报道它们的薄层色谱鉴别,但因没有化学对照品[11]、仅用两个成分作对照[1,12]或者所得到的色谱条带不够多,指纹性不强[13],难以达到准确鉴别的目的。本实验同时采用对照药材和五个成分的化学对照品,采用高效薄层色谱,可达到准确鉴别的目的,为防风药材的质量控制提供参考依据。
1 仪器与材料
1.1 仪器
ZF-1三用紫外分析仪(上海精科实业有限公司)、数码相机(佳能)、TDZ4-WS低速台式离心机(湖南湘仪实验室仪器开发有限公司)、BP210S电子天平(德国Satorius公司)、KH200B型超声波清洗器(昆山禾创超声仪器有限公司)、HPX-16085H-3恒温恒湿箱(上海新苗医疗器械制造有限公司)、AB135-S十万分之一天平(METTLER TOLED仪器有限公司)。
1.2 试药
甲醇、乙醇、甲酸、环己烷、乙酸乙酯、无水乙醇、硫酸、二氯甲烷均为分析纯,硅胶G预制板TLC、HPTLC(山东青岛海洋),硅胶G预制板(德国默克公司),以上薄层板均为20 cm×10 cm规格。升麻素苷(纯度93.9%)、5-O-甲基维斯阿米醇葡萄糖苷(纯度96.4%)、升麻素(纯度>98%)、亥茅酚苷(纯度>98%)、防风对照药材,以上对照品均购自中国药品生物制品检定所,紫花前胡苷(纯度>98%)购自成都曼斯特生物科技有限公司。
1.3 药材
本研究收集了不同产地的防风共15批,经沈阳药科大学中药学院贾英教授鉴定为防风科植物防风Saposhnikoviadivaricata(Turcz.)Schischk.的干燥块根。样品1-3号产地是内蒙古,4-6号产地是黑龙江,7,8号产地是辽宁,9-11号产地是吉林,12,13号产地是河北,14号产地是安徽,15号产地是甘肃。所有样品经干燥、粉碎之后通过80目筛再提取制样,13号样品用于薄层方法开发。
2 方法与结果
2.1 防风药材薄层色谱条件的考察
2.1.1 提取方法考察 在本人前期研究的基础之上[14],选择甲醇、85%甲醇、乙醇和85%乙醇作为超声提取溶剂进行考察,结果85%乙醇作为提取溶剂,条带清晰,且乙醇安全无毒,故选用85%乙醇为提取溶剂。通过单因素循环考察不同固液比(1 ∶5,1 ∶10,1 ∶20)、不同提取时间(10,20,30 min),所得色谱图见图1-3,以特征条带清晰不展宽、背景颜色浅为评价指标,结果表明用10倍量85%的乙醇室温条件下超声提取20 min时得到的色谱图最好。

1.CRS;2.甲醇;3. 85%甲醇;4.乙醇; 5. 85%乙醇 (17 ℃, 57%)
图1 提取溶剂的考察
Figure 1 Investigation of extraction solvents
1.CRS;2.固液比1 ∶5;3.固液比1 ∶10;4.固液比1 ∶20 (17.5 ℃, 59%)
图2 提取固液比考察
Figure 2 Investigation of volume of solvent
1.CRS;2.提取10 min;3.提取20 min;4.提取30 min (17 ℃, 48%)
图3 提取时间考察
Figure 3 Investigation of time of extraction
2.1.2 点样量 用定量点样管分别取2,5,8,10 μl供试品溶液,于同一高效薄层色谱板上各点成10 mm宽的条度,按照“2.3防风高效薄层色谱鉴别”中所述方法操作。所得色谱图见图4。
对照品溶液(CRS)展开显示5条色带,从下往上,依次为升麻苷、5-O-甲基维斯阿米醇苷、紫花前胡苷、亥茅酚苷和升麻素。结果显示,随着点样量的增加,供试品中升麻苷、5-O-甲基维斯阿米醇葡萄糖苷、紫花前胡苷、亥茅酚苷和升麻素相应条带逐渐清晰。但是,当点样量达到8 μl时会出现条带展宽,分离度下降。所以,点样量选择5 μl。
2.1.3 点样宽度 用定量点样管取5 μl供试品溶液,分别点2,4,6,8,10 mm宽的条带于同一高效薄层色谱板上,按照“2.3防风高效薄层色谱鉴别”中所述方法操作。所得色谱图见图5。
结果显示,所有的薄层条带在365 nm紫外灯下相似。随着点样宽度的增加,条带愈发集中、清晰,能够彼此有效分离。所以,点样宽度选择10 mm。

a.升麻苷;b.5-O-甲基维斯阿米醇苷;c.紫花前胡苷;d.亥茅酚苷;e.升麻素;1.CRS; 2. 2 μl; 3. 5 μl; 4. 8 μl; 5. 10 μl (17 ℃, 57%)图4 点样量的考察Figure 4 Investigation of volume of application
2.1.4 展开过程 分别取5 μl对照品溶液、对照品药材溶液(BRM)和供试品溶液,分别点样于A、B、C、D4块高效薄层色谱板上,将这4块高效薄层板分别放置在装有展开剂Ⅰ:二氯甲烷-甲醇-甲酸(16 ∶4 ∶1)或展开剂Ⅱ:环己烷-乙酸乙酯(2 ∶1)的层析缸中,并按照表1所示方法展开,展开结束后,以10%硫酸-乙醇溶液为显色剂,晾干后在365 nm下检视,结果见图6。

1. 2 mm; 2. 4 mm; 3. 6 mm; 4. 8 mm; 5. 10 mm (19.5 ℃, 49%)图5 点样宽度的考察Figure 5 Investigation of band width
表1四块高效薄层色谱板展开过程
Table1Developingprocessofthefourhighperformancethinlayerchromatographyplates

薄层板展开过程 展开结果 A展开剂Ⅰ:8 cm极性大的黄酮类成分升麻苷、5-O-甲基维斯阿米醇葡萄糖苷、紫花前胡苷、亥茅酚苷和升麻素得到有效分离,但薄层色谱板上部极性小的物质的条带不能彼此有效分离B展开剂Ⅱ:8 cm极性大的黄酮类成分升麻苷、5-O-甲基维斯阿米醇葡萄糖苷、紫花前胡苷、亥茅酚苷和升麻素的RF值几乎都为0C展开剂Ⅰ:5 cm,展开剂Ⅱ:8 cm极性大和极性小的成分都能得到有效分离,且没有溶剂效应D展开剂Ⅱ:8 cm,展开剂Ⅰ:5 cm第二次展开的溶剂前沿会影响色带的观察,且薄层色谱板上部极性小的物质的条带分离不如板C
结果表明,单独使用展开剂A和展开剂B都不适合,所以二者都应该被包含在展开过程中。为了使薄层板下部的黄酮类物质得到有效分离且不与溶剂前沿过近,薄层板在展开剂Ⅰ中的展开距离减少至5 cm。D板出现了较为明显的溶剂效应,而C板色谱中的升麻苷、5-O-甲基维斯阿米醇葡萄糖苷、紫花前胡苷、亥茅酚苷和升麻素均得到有效分离,且没有溶剂效应。所以C板的展开过程是合理的。
2.1.5 展开距离 分别取5 μl对照品溶液、对照品药材溶液和供试品溶液,分别点样于A、B、C、D4块高效薄层色谱板上,将这4块高效薄层板分别按照表2展开距离进行展开,先放置在装有展开剂Ⅰ的层析缸中展开,取出薄层板,干燥,把薄层板置于装有展开剂Ⅱ的层析缸中展开。展开结束后,以10%硫酸-乙醇溶液为显色剂,晾干后在365 nm下检视,结果见图7。考虑到各物质的分离效果以及展开过程所需时间,在展开剂Ⅰ中展开5 cm,在展开剂Ⅱ中展开8 cm是最为合理的展开距离。
2.2 色谱鉴定的方法学验证
2.2.1 专属性 分别取5 μl供试品溶液、防风对照药材标准溶液(0.10 g/ml 85%乙醇)和浓度适宜的各对照品溶液,点条带于同一高效薄层色谱板上,按照“2.3防风高效薄层色谱鉴别”中所述方法操作。所得色谱图见图8。
所得色谱显示,供试品溶液色谱中的RF值为0.09的浅蓝色条带,RF值为0.15的亮蓝色条带,RF值为0.18的强紫色条带,RF值为0.22的浅黄色条带和RF值为0.30的亮蓝色条带,它们所呈现的颜色和位置分别与升麻苷、5-O-甲基维斯阿米醇葡萄糖苷、紫花前胡苷、亥茅酚苷、升麻素对照品条带一致。供试品溶液色谱中的所有条带与防风对照药材标准溶液色谱中条带一致。

A.展开剂Ⅰ,上行展开8 cm B.展开剂Ⅱ,上行展开8 cm C.展开剂Ⅰ,上行展开5 cm;展开剂Ⅱ,上行展开8 cm D.展开剂Ⅱ,上行展开8 cm;展开剂Ⅰ,上行展开5 cm 1. CRS; 2. BRM; 3. 供试品溶液(17 ℃, 48%)图6 展开过程的考察Figure 6 Investigation of developing process
表2四块高效薄层板的展开距离
Table2Developingdistanceofthefourhighperformancethinlayerchromatographyplates

薄层板展开距离 展开结果 A展开剂Ⅰ:4 cm,展开剂Ⅱ:7 cm极性大的黄酮类成分升麻苷、5-O-甲基维斯阿米醇葡萄糖苷、紫花前胡苷、亥茅酚苷和升麻素不能得到有效分离B展开剂Ⅰ:5 cm,展开剂Ⅱ:8 cm极性大和极性小的成分都能得到有效分离,且时间合理C展开剂Ⅰ:6 cm,展开剂Ⅱ:10 cm极性大和极性小的成分都能得到有效分离,但消耗时间太长,不合理D展开剂Ⅰ:7 cm,展开剂Ⅱ:12 cm极性大和极性小的成分都能得到有效分离,但消耗时间太长,不合理

A.展开剂Ⅰ,上行展开4 cm;展开剂Ⅱ,上行展开7 cm B.展开剂Ⅰ,上行展开5 cm;展开剂Ⅱ,上行展开8 cm C.展开剂Ⅰ,上行展开6 cm;展开剂Ⅱ,上行展开10 cm D.展开剂Ⅰ,上行展开7 cm;展开剂Ⅱ,上行展开12 cm1. CRS; 2. BRM; 3. 供试品溶液(13 ℃, 60%)图7 展开距离的考察Figure 7 Investigation of developing distance
2.2.2 稳定性 稳定性实验使用供试品溶液,把供试品溶液分别在室温下保存不同时间(0,1,2,3 d)后进行。取5 μl供试品溶液,点样于同一高效薄层色谱板上,按照“2.3防风高效薄层色谱鉴别”中所述方法操作。所得色谱图表明,供试品溶液在3 d内具有稳定性。

1. 升麻苷; 2. 5-O-甲基维斯阿米醇苷; 3. 紫花前胡苷; 4. BRM; 5-7. 供试品; 8. 亥茅酚苷; 9. 升麻素(17.5°, 46%)图8 专属性考察Figure 8 Investigation of specificity
2.2.3 耐用性
2.2.3.1 不同硅胶板 取5 μl对照品溶液、对照药材溶液和供试品溶液,分别点样于普通薄层色谱板和高效薄层色谱板上,按照“2.3防风高效薄层色谱鉴别”中所述方法操作。所得色谱图结果见图9。
结果表明,高效薄层色谱板条带窄、清晰、分离度好,国产普通薄层色谱条带宽,分离度差。
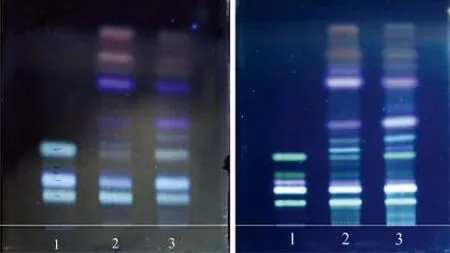
A. 普通薄层板 B. 高效薄层板1. CRS; 2. BRM; 3. 供试品溶液(19 ℃, 55%)图9 不同细度硅胶薄层板的考察Figure 9 Investigation of different thin layer plates of silica gel
2.2.3.2 荧光剂 取5 μl对照品溶液、对照药材溶液和供试品溶液,分别点样于不含荧光剂的薄层板HPTLC Silica gel 60和含荧光剂的薄层板HPTLC Silica gel 60 F254,按照“2.3防风高效薄层色谱鉴别”中所述方法操作。所得色谱图表明荧光剂对薄层条带没有显著的影响。
2.2.3.3 不同厂家高效薄层板 取5 μl对照品溶液A、对照品溶液B和供试品溶液,分别点样于不同厂家的高效薄层板上,按照“2.3防风高效薄层色谱鉴别”中所述方法操作。所得色谱图结果表明,HPTLC(默克)板条带窄、清晰、分离度好,HPTLC(青岛海洋)条带宽(见图10)。
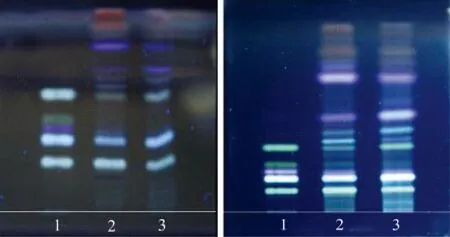
A. 青岛海洋,中国 B. 默克,德国1. CRS; 2. BRM; 3. 供试品溶液(19 ℃,55%)图10 不同厂家高效薄层板的考察Figure 10 Investigation of different manufactories of the HPTLC precoated plates
2.2.3.4 不同展开温度 取点样后的高效薄层色谱板,分别在不同温度下展开(12,19,25 ℃),相对湿度(RH%)为55%,展开过程按照“2.3防风高效薄层色谱鉴别”中所述方法操作。结果表明,该方法对不同温度的适应性较好。
2.2.3.5 不同展开湿度 取点样后的高效薄层色谱板,分别在不同湿度下展开(30%,55%,80%),温度为19 ℃,展开过程按照“2.3防风高效薄层色谱鉴别”中所述方法操作。结果表明,该方法对不同湿度的适应性较好。
2.3 防风高效薄层色谱鉴别
2.3.1 对照品溶液(CRS)的制备 分别取升麻苷、5-O-甲基维斯阿米醇苷、紫花前胡苷、亥茅酚苷和升麻素对照品适量,精密称定,加入甲醇溶解制成浓度分别为400.0 μg/ml, 300.0 μg/ml,10.00 μg/ml, 400.0 μg/ml和500.0 μg/ml的对照品溶液。摇匀,备用。
2.3.2 对照药材溶液(BRM)的制备 取防风对照药材粉末约1 g适量置于锥形瓶中,加入85%乙醇10 ml,超声提取20 min,离心取上清液,得浓度为100 mg/ml的防风对照药材溶液。
2.3.3 供试品溶液的制备 称取防风药材粉末约1 g适量置于锥形瓶中,加入85%乙醇10 ml,超声提取20 min,离心取上清液,得浓度为100 mg/ml的供试品溶液。
取上述防风混合对照品、对照药材、供试品,照薄层色谱法(《中国药典》2015版一部附录ⅥB)试验。取混合对照品、对照药材、供试品各5 μl,分别点于同一硅胶G薄层板上,以二氯甲烷-甲醇-甲酸(16 ∶4 ∶1)、环己烷-乙酸乙酯(2 ∶1)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液显色剂,晾干,置紫外灯(365 nm)下观察。供试品色谱中,在与对照药材和对照品相应位置上,均显示相同颜色的荧光斑点,并可见其他条带,呈现出指纹特征(见图11,12)。

1. CRS; 2. BRM; 3-9. 供试品1-7(17.5 ℃,46%)图11 防风药材的薄层色谱图Figure 11 Thin layer chromatogram of sample 1-7
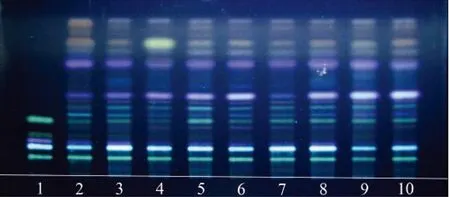
1. CRS; 2. BRM; 3-10. 供试品8-15(21 ℃, 54%)图12 防风药材的薄层色谱图Figure 12 Thin layer chromatogram of sample 8-15
3 讨论
3.1 薄层色谱条件考察
本试验详细考察了薄层鉴别的条件,色谱系统考察了点样量、点样宽度、展开系统和展开距离,色谱鉴定的方法学验证中考察了专属性、稳定性和耐用性(不同硅胶板,荧光剂,不同厂家高效薄层板,不同展开温度及不同展开湿度)的影响。最终确定防风高效薄层鉴别方法为:点样量为5 μl,条带宽10 mm,展开板为HPTLC Silica G60(Merck)。展开系统为展开剂Ⅰ:二氯甲烷-甲醇-甲酸(16 ∶4 ∶1),5 cm;展开剂Ⅱ:环己烷-乙酸乙酯(2 ∶1),8 cm。以10%硫酸乙醇溶液为显色剂,紫外灯365 nm下检视,对防风进行了鉴别。且不同粒径的硅胶板对实验结果有明显差别。荧光物质的有无,不同厂家的高效薄层板,以及不同温度和湿度对对照品溶液和供试品溶液的色谱条带没有显著影响。
3.2 鉴别指标的选择
本试验以升麻苷、5-O-甲基维斯阿米醇苷、紫花前胡苷、亥茅酚苷和升麻素为指标进行薄层鉴别。在《中国药典》2015年版中,防风薄层鉴别仅选择了升麻苷、5-O-甲基维斯阿米醇苷两种成分进行鉴别指认,不具有专属性。因此,本研究增加了紫花前胡苷、亥茅酚苷和升麻素三种活性成分作为指标成分,提高了薄层鉴别的专属性。
3.3 提取条件的选择
《中国药典》2015年版中薄层供试品溶液制备过程较复杂,需将超声提取后的溶液过滤,蒸干复溶。本试验考察了不同的提取溶剂、溶剂倍量和提取时间,最终选择以10倍量85%乙醇作为提取溶剂,超声20 min,滤过作为供试品溶液。简化了供试品溶液的制备过程,有利于大批量防风的薄层鉴别。
3.4 展开条件的选择
《中国药典》2015年版展开系统为三氯甲烷-甲醇(4 ∶1),三氯甲烷为第二类溶剂,有动物致癌性,且得到的条带颜色浅,数目少。对展开系统进行优化,得到最佳条件为:二次展开,展开剂Ⅰ:二氯甲烷-甲醇-甲酸(16 ∶4 ∶1),展开剂Ⅱ:环己烷-乙酸乙酯(2 ∶1)。且采用高效薄层色谱,与普通薄层鉴别或者单纯一次展开所得结果相比,本试验所得高效薄层色谱条带清晰,相似成分分离度好,呈现出指纹性[15]。该方法操作简单、重现性好,可作为防风药材定性鉴别的一种方法,为防风药材的质量控制提供参考依据。
参考文献:
[1] 国家药典委员会.中华人民共和国药典一部[M].北京:中国医药科技出版社,2015:149-150.
[2] 《图解经典》编辑部.神农本草经[M].长春:吉林科学技术出版社,2017:112-113.
[3] 李洪兵.中药材防风的开发利用[J].中外健康文摘,2012,9(18):19-20.
[4] 尹浣姝,宋新波,刘晓明,等.防风通圣丸质量标准研究[J].现代中药研究与实践,2011,25(1):52-54.
[5] Hong Min, Wang Xinzhi, Wang Liang,etal. Screening of immunomodulatory components inYu-ping-feng-san using splenocyte binding and HPLC[J].J Pharm Biomed Anal,2011,54:87-93.
[6] Yan Zhixiang, Yang xinghao, Wu Jianbo,etal. Qualitative and quantitative analysis of chemical constituents in traditional Chinese medicinal formula Tong-Xie-Yao-Fang by high-performance liquid chromatography/diode array detection/electrospray ionization tandem mass spectrometry[J]. Anal Chim Acta, 2011, 691:110-118.
[7] 林玉萍,杨艳,虎春艳,等.云防风的化学成分研究[J].云南中医学院学报,2014,27(3):22-24.
[8] 王成章,张崇禧.防风国内外研究进展[J].人参研究,2008,(1):35-41.
[9] 王建华,楼之岑.防风类中药原植物的调查鉴定[J].中药通报,1988,13(1):9-10.
[10] 高咏莉.生药防风的化学成分与药理作用研究进展[J].山西医科大学学报,2004,35(2):216-218.
[11] 杨敏聪.防风与一种伪品防风的鉴别[J].海峡药学,2007,19(5):56-57.
[12] 黄兰芷,王曙宾.连防感冒颗粒中防风薄层鉴别方法改进[J].中南药学,2007,5(2):149-150.
[13] 肖水庆,李丽,杨滨,等.防风化学成分研究[J].中国中药杂志,2001,26(2):117.
[14] Liao Huali, Li Qing, Liu Ran,etal. Fingerprint analysis and multi-ingredient determination using a single reference standard for saposhnikoviae radix[J]. Anal Sci, 2014, 30(12), 1157-1163.
[15] Yamunadevi M, Wesely EG, Johnson M. Chromatographic finger print analysis of steroids in Aerva lanata L by HPTLC technique[J]. Asia-Pac J Trop Biomed, 2011, 1: 428-433.

