有上腹部手术史患者行腹腔镜胆囊切除术的体会
朱卫安,张 竞,钟发明
(武义县第一人民医院,浙江 金华,321200)
以往传统开腹胆囊切除术是治疗有上腹部手术史的胆囊结石合并胆囊炎的金标准,腹腔镜胆囊切除术(laparoscopic cholecystectomy,LC)则被认为是有风险、激进的方式[1]。但随着腹腔镜技术的发展,有上腹部手术史患者行LC的尝试越来越多[2],而目前国内对于有上腹部手术史及无手术史患者行LC的对比研究较少。有上腹部手术史患者行LC最主要的障碍在于腹腔内粘连造成的技术性难度增加,如存在穿刺Trocar过程中损伤腹壁粘连器官的风险、难以获得足够的术野、腹腔内粘连造成解剖变异等,这些因素均可增加术中出血或胆管损伤的风险[3]。但充分的术前准备、细致的操作、丰富的LC经验会使越来越多的外科医生在面对有上腹部手术史的患者时不再犹豫。本研究目的是对有上腹部手术史的患者行LC的安全性与可行性进行探索。
1 资料与方法
1.1 临床资料 本回顾性研究经武义县第一人民医院伦理委员会批准,获得受试者知情同意。选取研究对象为2015年8月至2017年8月我院收治的慢性胆囊炎合并胆囊结石,并由经验丰富的术者(年LC量超过150例的操作者)行LC的患者,其中57例有上腹部手术史,2例术后发现胆总管结石被排除,入组55例(观察组);无手术史的患者根据性别、年龄、体重、ASA分级等变量相同或相似配对选择55例作为对照组,两组患者均由同一术者主刀手术。入组标准:(1)慢性胆囊炎并胆囊结石;(2)无严重心肺脑功能障碍,可耐受手术;(3)上腹部手术史组术前均仅有一次手术史;(4)患者同意入组。排除标准:(1)急性胆囊炎;(2)有多次上、下腹部手术史;(3)患有精神疾病。观察组患者42~69岁,上腹部手术与本次手术间隔6~52个月。对照组患者39~71岁。两组患者术前临床资料差异无统计学意义(P>0.05),见表1。观察组中前次手术史包括41例胃大部切除术,7例脾切除术,3例肠修补术,3例粘连松解术,1例胰体尾切除术。

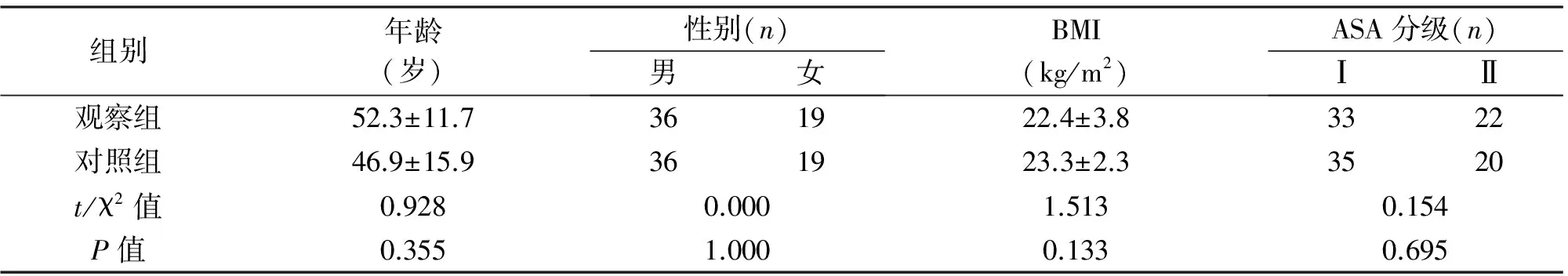
组别年龄(岁)性别(n)男女BMI(kg/m2)ASA分级(n)ⅠⅡ观察组52.3±11.7361922.4±3.83322对照组46.9±15.9361923.3±2.33520t/χ2值0.9280.0001.5130.154P值0.3551.0000.1330.695
1.2 术前准备 观察组术日晨清洁灌肠,留置导尿管。两组患者术前禁饮4 h、禁食12 h,术前留置胃管,术前30 min予以抗生素预防感染。
1.3 手术方法 常规四孔法行LC,脐下为观察孔,对照组直接穿刺Trocar,观察组于脐下距原手术瘢痕3 cm以上采用Hasson法直视下切开腹膜后置入Trocar,并用布巾钳钳夹以免漏气及Trocar脱出。置入腹腔镜探查腹腔粘连情况,其余三孔在腹腔镜监视下选择无脏器与腹壁粘连处穿刺Trocar。钝锐结合法分离影响胆囊切除的粘连,充分暴露手术视野,常规切除胆囊。如腹腔内解剖不清,无法充分暴露术野或术中出现难以控制的出血应及时中转开腹。
1.4 观察指标 患者出院后通过电话及门诊复查方式进行随访,观察两组手术时间、术后住院时间、住院费用、中转开腹率、术后并发症、术中出血量。
1.5 统计学处理 两组计量资料比较采用t检验,计数资料比较采用χ2检验,通过SPSS 19.0软件进行数据处理,P<0.05为差异有统计学意义。
2 结 果
手术均顺利完成,无死亡病例。对照组手术时间、术中出血量、住院费用优于观察组,差异有统计学意义(P<0.05)。两组中转开腹率、术后住院时间、术后并发症发生率差异无统计学意义(P>0.05)。两组患者无术中副损伤,观察组术后发生出血1例,对照组术后胆漏1例,均经内科保守治疗治愈。见表2。

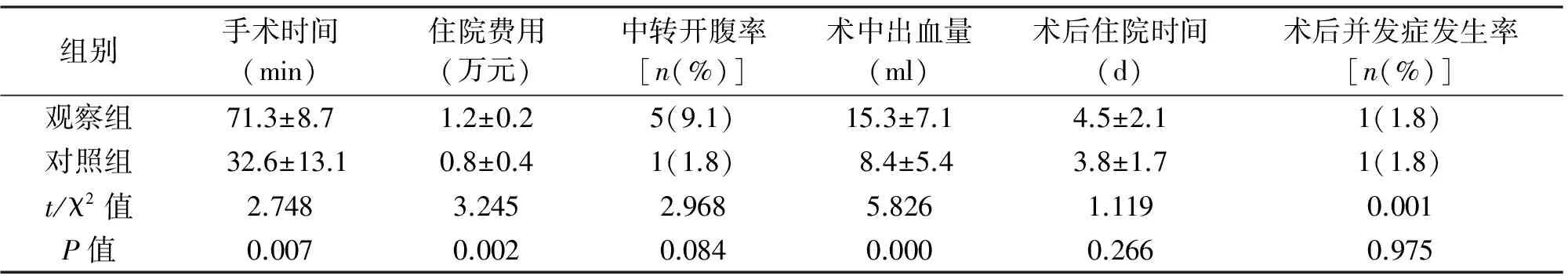
组别手术时间(min)住院费用(万元)中转开腹率[n(%)]术中出血量(ml)术后住院时间(d)术后并发症发生率[n(%)]观察组71.3±8.71.2±0.25(9.1)15.3±7.14.5±2.11(1.8)对照组32.6±13.10.8±0.41(1.8)8.4±5.43.8±1.71(1.8)t/χ2值2.7483.2452.9685.8261.1190.001P值0.0070.0020.0840.0000.2660.975
3 讨 论
传统开放手术增加了患者的痛苦与经济负担[4],LC是治疗胆囊结石合并胆囊炎的金标准,其适应证也在不断扩展。LC开展初期,腹腔严重粘连曾一度被认为是LC的禁忌证[5],但随着腹腔镜技术、设备的迅速发展,现已不再是LC的绝对禁忌证。本研究目的是评价有上腹部手术史患者行LC的安全性与可行性。本研究中,观察组手术时间更长、术中出血量更多、住院费用更高,因为有上腹部手术史的患者粘连解剖需细致,并需要更多的手术器械、耗材及药物,这些因素增加了操作时间及医疗成本,同时因术中分离粘连过程中创面更大,需游离的组织更多,造成术中出血量增多。
LC中转开腹主要是为避免胆道、胃肠道损伤及难以控制的出血,及时中转开腹可使手术关键区域得到充分暴露[6]。研究证明,有上腹部手术史患者行LC时胆囊床及分离粘连导致的创面出血不但会造成术中失血量增加,还会引起术野不清,增加手术并发症的发生风险[7]。有上腹部手术史患者第一穿刺孔的选择极为关键。国内有学者报道,有上腹部手术史患者术前应行超声检查,判断有无粘连,从而指导术者决定第一穿刺孔部位[8]。本研究中常规选择远离手术瘢痕3 cm以上处,应用Hasson法直视下切开腹膜后置入Trocar,并用布巾钳钳夹,以免漏气及Trocar脱出。这样操作不但安全,而且可获得良好的视野及操作空间,降低了术中副损伤、术后出血、胆漏、胆道狭窄等并发症的发生风险,同时降低了中转开腹率[9]。一旦第一穿刺孔成功建立,可选择右侧肋缘下无粘连处穿刺第二枚Trocar,依次于剑突下腹腔无粘连处、右中腹穿刺第三枚、第四枚Trocar。腹内粘连程度取决于原有切口位置,一般而言,右侧肋缘下切口导致的粘连较严重,但因为临床有上腹部手术史的患者多以胃大部切除术、脾脏切除术为主,粘连区域主要位于中线、左上腹,肝下间隙广泛粘连的程度较轻。因此我们认为这是造成两组住院时间、出血量、中转开腹率、术后并发症无明显差异的原因之一。
成功建立Trocar后,了解胆道手术的解剖规律显得尤为重要[10]。临床上较常见的上腹部手术史患者行LC的粘连部位主要包括:肝膈面与腹壁粘连,胃窦、网膜与腹壁、右肝下间隙的粘连,结肠与右肝下间隙的粘连,十二指肠球部、降部与肝门区粘连等[11]。肝脏膈面与腹壁的粘连多无需松解,因其可提供自然的暴露右肝下间隙的反作用力,更利于手术操作;胃窦、网膜与右肝下间隙的粘连,通过超声刀仔细松解是十分安全的。结肠与右肝下间隙的粘连,可用腔镜电剪刀及吸引器钝锐结合法分离,无需过度分离,仅能暴露胆囊及胆囊三角区域即可。十二指肠球部、降部与肝门区的粘连则可作为找寻胆囊三角的解剖标志,因为胆囊三角多位于此粘连的深部,应用锐利剪刀及吸引器钝性松解即可取得较好效果。根据经验,慢性胆囊炎合并胆囊结石患者松解此部分粘连后会很容易地找到胆囊动脉及胆囊管。胆囊三角因粘连导致解剖不清的患者,可选择逆行切除或胆囊大部切除术,以减少术中副损伤的发生。遵循以上方法解剖粘连,会保证手术的安全性,这也是两组住院时间、中转开腹率、术后并发症差异无统计学意义的另一个重要原因。
如果粘连严重难以进入胆囊切除区域或出现难以控制的出血等,应及时中转开腹。虽然本研究中观察组中转开腹率高于对照组,但差异无统计学意义;两组均无术中胆管、胃肠道损伤病例及术中大出血死亡病例。本研究选取的均为慢性胆囊炎合并胆囊结石患者,未纳入急性胆囊炎合并胆囊结石的患者,这是本研究局限性之一;另一个局限性在于观察组患者前次手术主要为胃大部切除术,无既往行胆囊三角区手术的患者,因此我们以后的研究方向是有胆囊三角区手术史的患者行LC的安全性分析。
LC应用于有上腹部手术史的患者已有多年,但与无上腹部手术史患者行随机对照的研究仍较少,我们的研究结果是积极的。本研究结果表明,有上腹部手术史患者行LC是相对安全、可行的;有上腹部手术史患者需行胆囊切除时,LC是可选择的治疗方式。
参考文献:
[1] Geraci G,D'Orazio B,Rizzuto S,et al.Videolaparoscopic cholecystectomy in patients with previous abdominal surgery.Personal experience and literature review[J].Clin Ter,2017,168(6):e357-e360.
[2] Spaziani E,Di Filippo AR,Orelli S,et al.The influence of residents in the outcome of elective laparoscopic surgery:a prospective study comparing a teaching hospital and a private community hospital in Italy[J].Clin Ter,2017,168(1):e28-e32.
[3] Utsumi M,Aoki H,Kunitomo T,et al.Preoperative Risk Factors for Conversion of Laparoscopic Cholecystectomy to Open Cholecystectomy and the Usefulness of the 2013 Tokyo Guidelines[J].Acta Med Okayama,2017,71(5):419-425.
[4] 卢先州,牛国梁,王辉,等.有上腹部手术史的腹腔镜胆囊切除术探讨[J].现代生物医学进展,2012,12(1):120-122.
[5] 李琴,韩晓东,张弘玮,等.术前超声预测腹腔镜胆囊切除术手术难度的分析[J].腹腔镜外科杂志,2013,18(1):52-56.
[6] Chang SK,Wang YL,Shen L,et al.A randomized controlled trial comparing post-operative pain in single-incision laparoscopic cholecystectomy versus conventional laparoscopic cholecystectomy[J].World J Surg,2015,39(4):897-904.
[7] Choi SB,Han HJ,Kim WB,et al.The efficacy of subcostal-approach laparoscopic cholecystectomy in patients with previous midline incisions:comparative analysis with conventional laparoscopic cholecystectomy[J].J Laparoendosc Adv Surg Tech A,2014,24(12):842-845.
[8] Sultan AM,El Nakeeb A,Elshehawy T,et al.Risk factors for conversion during laparoscopic cholecystectomy:retrospective analysis of ten years' experience at a single tertiary referral centre[J].Dig Surg,2013,30(1):51-55.
[9] 刘煜,张文涛,马艳波.腹腔镜胆囊切除术后并发症的诊治及预防研究进展[J].腹腔镜外科杂志,2017,22(11):875-878.
[10] 杨富财,薛菊存,李建忠.胆囊替代定位点在腹腔镜胆囊切除术中的应用[J].腹腔镜外科杂志,2015,20(4):287-289.
[11] Huang Y,Feng Q,Wang K,et al.The safety and feasibility of laparoscopic common bile duct exploration for treatment patients with previous abdominal surgery[J].Sci Rep,2017,7(1):15372.

