内淋巴囊肿瘤的影像学表现及鉴别诊断
耿 悦 沙 炎
内淋巴囊肿瘤 (endolymphatic sac tumor,ELST)起源于内耳内淋巴囊系统的一种罕见的具有局部侵袭性的低度恶性肿瘤,又称内淋巴囊低度恶性腺癌、乳头状内淋巴囊瘤[1]。本文报道5例经组织病理学证实的ELST病例,并复习相关文献,总结其影像学表现、诊断及鉴别诊断要点,旨在提高对该罕见肿瘤的认识。
方 法
1.一般资料
回顾性分析我院2015-2017年经病理证实的ELST病例5例5耳,男1例,女4例,年龄43±12岁。临床症状包括4例耳鸣伴听力下降,1例眼睑闭合障碍,5例均不伴von Hippel-Lindau综合征,病程约2个月~3年。
2.扫描方法
CT检查采用Siemens Somatom Definition Edge 64排扫描仪,以听眦线为扫描基线,管电压120kV,管电流250mAs,矩阵512× 512,FOV均为250mm,层厚2mm,间距2mm。
MRI检查采用 Siemens Magnetom Verio 3.0T MRI扫描仪及12通道头线圈。常规行横断面TSET1WI(TR 384ms,TE 9.1ms);横断面及冠状面压 脂 TSE-T2WI(TR 4000ms,TE 99ms),矩 阵640×592,FOV 220mm×220mm,层厚6mm,层间距0.6mm。横断位及冠状位T1WI增强扫描;钆喷酸葡胺0.1mmol/kg,静脉注射速率2ml/s;动态增强,每间隔8~10秒扫描一次,共20次。RESOLVE-DWI(TR 4700ms,TE 66ms);频带宽度723 Hz/Px,矩阵192×192,FOV 240mm×240mm,激励次数1,b值0、1000s/mm2,扩散方向3,TA 2.55 分钟。
结 果
5例肿瘤均呈不规则浅分叶状,瘤体最小者约1cm×1.2cm×1.5cm,最大者约2cm×2.2cm×3.5cm,其中3例位于左侧,2例位于右侧。病灶中心均位于内听道与乙状窦之间的颞骨岩部中后缘,其中4例不同程度向后侵入颅后窝、桥小脑角区,引起相应结构受压偏移;4例向外累及中耳腔、乳突气房,伴2例半规管及面神经管乳突段受累;4例向下累及颈静脉孔区附近并侵犯颅底;1例向前累及内听道后壁。
1、CT平扫表现
肿块密度不均,边界欠清,实质内见较多细针状高密度骨样结构,5例肿块后缘均见不规则薄层钙化缘。骨破坏区主要位于颞骨岩部中后缘,呈“蜂窝状”溶骨性骨质破坏,破坏区边缘似“地图样”或“虫蚀样”(图1A)。
2、MRI表现
T1WI、T2WI平扫肿块均呈不均匀混杂信号(以小脑灰质信号作参考),实质部分T1WI以等信号为主,T2WI以高信号为主,内见不规则条索、斑片状长T1 、短T2低信号区,肿块边缘可见短T1 、长T2高信号影,脂肪抑制像仍为高信号(图1B、C),较大肿块内可见点、条状血管流空影,肿块DWI轻度受限(图1D),4例侵犯颅后窝、桥小脑角区,肿块与受压脑组织间见低信号脑膜相隔,周围伴脑脊液影。T1WI增强显示肿块实性部分呈明显不均匀强化(图1E)。其中2例行动态增强检查,动态增强曲线为速升缓降型(图1F)。
讨 论
1、临床及病理学特点
内淋巴囊起源于胚胎期的原始神经外胚层,是内淋巴管远侧膨大而形成的盲端,用于维持内耳内淋巴的吸收平衡。内淋巴囊可分为近侧段(皱襞部)及远侧段两部分,近侧段走行于岩骨中后缘的骨性凹陷切迹内,被认为是ELST的发生部位[2]。ELST是一种罕见的具有局部侵袭的低度恶性肿瘤,好发于40岁左右的成年人,以中年女性多发[3],可伴有von Hippel-Lindau综合征。本组病例中女性多于男性,平均年龄约43岁,与文献报道相符。ELST生长缓慢,病程常为数月至数年,其临床表现主要取决于肿瘤的大小和生长方向,以单侧听力损失最为常见,其机制可能是由于内耳Corti器破坏导致了内淋巴管阻塞和积水[4]。当肿瘤侵犯内耳迷路及中耳乳突时,可出现不同程度的前庭功能障碍,涉及面神经管时可导致面神经麻痹。在组织学上,ELST是由相互交错的乳头状及腺样结构组成,部分区域呈囊性扩张,间质中血管丰富,免疫组化表现为CK、CK8/18、EMA及Vimentin阳性[5]。
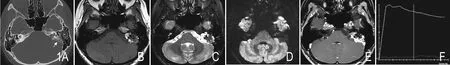
图1 女,31岁,左侧耳鸣伴听力下降3年余。A.CT示左侧颞骨岩部中后缘“蜂窝状”溶骨性骨质破坏,伴软组织病灶,其后缘不规则薄层钙化缘(箭头),其内见较多细针状骨样结构。B、C.MR平扫示左侧桥小脑角区浅分叶状软组织肿块,T1WI、T2WI均呈混杂信号,边缘见短T1、长T2高信号影,脂肪抑制像仍为高信号。D.DWI肿块弥散轻度受限。E、F.MR增强扫描,肿块不均匀明显强化,动态增强曲线为速升缓降型。
2、影像学表现及鉴别诊断
CT上,ELST表现为侵蚀颞骨岩部的浅分叶状软组织肿块,伴“蜂窝状”溶骨性骨质破坏,其中心位于内听道和乙状窦之间岩骨中后缘前庭导水管外口区,即内淋巴囊的解剖部位所在,具有一定特征性。肿块密度不均,边界欠清,实质内见较多细针状高密度骨样结构,可能是肿瘤浸润包埋所残存的死骨。有研究认为[6],肿瘤后缘见不规则薄层钙化缘是诊断ELST的重要依据,其为颞骨膨胀的骨质边缘,反映了此病慢性生长的过程,本组5例病例后缘均可见薄层不规则钙化缘。随着疾病的进展,肿瘤可向上侵及岩骨上缘,向下延伸至颈静脉孔区并侵犯中颅底,向前外累及内听道、迷路、中耳腔、乳突气房及面神经管,并向颅后窝、桥小脑角区扩展,引起相应结构受压偏移。MRI上,肿块T1WI、T2WI均呈混杂信号,边缘可见短T1、长T2高信号影,脂肪抑制图像上仍表现为高信号,为诊断ELST的可靠依据[6],其可能是富血管肿瘤内部亚急性出血的产物,包括正铁血红蛋白、胆固醇结晶及蛋白类物质等。肿块内长T1、短T2的低信号区域可能为残存骨质以及含铁血黄素沉积所致[7]。较大肿块内部常可见血管流空征。本组4例病例侵犯颅后窝、桥小脑角区,肿块与脑组织间可见脑膜及脑脊液相隔,呈明显脑外肿瘤的特点。ELST的血供丰富,主要由颈外动脉分支和小脑前下动脉供血[8],增强扫描肿块实质部分呈明显强化,其信号强度与血管相当,术前栓塞有助于手术切除。病变的动态强化方式,在一定程度上反映了组织的血管生物学特性[9],本组2例病例的动态增强曲线均呈速升缓降型,可符合ELST低度恶性肿瘤的特性。
ELST需要与其他侵犯颞骨岩部的常见肿瘤鉴别[10]:①脑膜瘤:肿瘤沿着硬脑膜方向生长,常引起相邻骨组织增生硬化或轻度吸收破坏,增强扫描呈明显均质强化,可见“脑膜尾征”。而ELST为不均质强化,骨质破坏明显。②颈静脉球瘤:源于颈静脉孔的颈静脉球瘤可侵及岩骨、桥小脑区,局限性虫蚀样破坏颅底骨质,但病灶的中心起源部位低于ELST,MRI成像中典型的颈静脉球瘤可见“盐-胡椒”征。③听神经瘤:病灶以内听道、桥小脑区为中心,邻近骨质呈受压或轻度吸收改变,很少引起颞骨溶骨性破坏。④横纹肌肉瘤:好发于儿童及婴幼儿,颞骨及颅底骨质破坏更加广泛,并向深部结构浸润生长,增强扫描明显强化,但程度低于ELST。
[1]Richard S, David P, Marsot-Dupuch K, et al. Central nervous system Hemangioblastomas, endolymphatic sac tumors, and von Hippel-Lindau disease. Neurosurg Rev, 2000, 23:1-22
[2]Bambakidis NC, Rodrigue T, Megerian CA, et al. Endolymphatic sac tumor metastatic to the spine: case report. J Neurosurg Spine, 2005,30:68-70
[3]Heffner Dk. Low-grade adenocarcinoma of probably endolymphatic sac origin: a clinicopathologic study of 20 cases. Cancer, 1989,64:2292-2302
[4]Bae CW, Cho YH, Chung JW, et al. Endolymphatic Sac Tumors :Report of Four Cases. J Korean Neurosurg Soc, 2008, 44:268-272
[5]傅海燕, 王家耀. 内淋巴囊肿瘤四例临床病理观察及鉴别诊断.中华肿瘤防治杂志, 2014, 21:1553-1556
[6]Mukherji SK, Albernaz VS, Lo WW, et al. Papillary endolymphatic sactumors: CT, MR imaging, and angiographic Findings in 20 patients. Radiology, 1997, 202:801-808
[7]林 青, 戴建平, 罗 麟, 等. 乳头状内淋巴囊瘤的影像学表现. 中华放射学杂志, 2002, 36 : 817-821
[8]岳云龙, 陈孝柏, 金延方. 内淋巴囊肿瘤的影像学表现(附两例报告并文献复习). 临床放射学杂志, 2007, 26:869-871
[9]闵庆华, 杨 军, 邵康为, 等. 乳腺良恶性病变的动态增强MR信号强度分析. 中国医学计算机成像杂志, 2009, 15:133-137
[10]戴媛媛, 沙 炎, 张 放, 等. 表现为搏动性耳鸣的颞骨占位性病变的影像学诊断. 中华医学杂志, 2013, 93:2617-2621

