紫杉醇脂质体与紫杉醇联合替吉奥一线治疗晚期胃癌的疗效观察
蔡 娟,左学良,赵文英,叶晓兵
(皖南医学院第一附属医院 弋矶山医院 1.肿瘤内科;2.胃肠外科,安徽 芜湖 241001)
胃癌是全球发病率第五位、病死率第三位的恶性肿瘤[1]。在我国,胃癌的发病率及病死率均居所有恶性肿瘤的第三位[2],因早期缺乏特异性临床症状,大部分胃癌患者在确诊时已属晚期,甚至失去手术治疗的机会。对于晚期胃癌,化疗是主要的治疗手段,但是目前仍无标准化疗方案。胃癌化疗的药物有氟尿嘧啶类(5-氟尿嘧啶、替加氟、卡培他滨、替吉奥)、铂类(奥沙利铂、顺铂)、紫杉醇类、蒽环类等。对于晚期胃癌的化疗方案,药物的选择目前仍然存在较多争议,三药联合较两药联合化疗的疾病缓解率短期内可能会有所提高,但中位生存时间(overall survival,OS)并没有延长,而且很多患者不能耐受三药联合的毒副反应[3]。
紫杉醇类药物是将紫杉醇溶于无水乙醇与聚氧乙烯代蓖麻油同比例组成的混合液,而聚氧乙烯代蓖麻油进入人体代谢后可导致组胺释放,容易引起严重的变态反应,使用前必须进行预处理,给临床应用带来不便。紫杉醇通过脂质体作为载体具有更有效的抗肿瘤作用,提高疗效并且减轻药物毒副反应。替吉奥是一种氟尿嘧啶衍生物的口服化疗药,它的主要成分是替加氟(FT)和吉美嘧啶(CDHP)及奥替拉西(OXO),对胃癌治疗效果明显。我们通过比较紫杉醇脂质体联合替吉奥组与紫杉醇联合替吉奥组一线治疗晚期胃癌的疗效和毒副作用,寻求相对优化的治疗方案。
1 资料与方法
1.1 临床资料 分析2012年10月~2017年10月在弋矶山医院肿瘤内科收治的52例初治或复发晚期胃癌患者的临床资料,年龄32~80岁,中位年龄63岁,其中男性32例,女性20例。分为2组:紫杉醇脂质体联合替吉奥组(27例)与紫杉醇联合替吉奥组(25例)。所有病例均经病理组织学证实,根据AJCC(第8版)胃癌临床分期标准,均为Ⅳ期。病理类型:中分化腺癌18例(35%),低分化腺癌27例(52%),印戒细胞癌7例(13%)。患者体力状况评分(eastern cooperative oncology group,ECOG)评分≤2分;重要脏器(肝脏、肾脏、心脏)功能无明显异常;无消化道出血、梗阻、穿孔等倾向;有可评价病灶;预计生存超过3个月。患者临床病理特征见表1。
表1 52例晚期胃癌患者临床病理特征

临床特征n紫杉醇脂质体+替吉奥组紫杉醇+替吉奥组χ2P性别0.6240.430 男321814 女20911年龄/岁0.1050.746 <60221210 ≥60301515ECOG评分0.0030.957 0~1分211110 2分311615疾病状态0.0170.897 术后复发1587 晚期371918分化程度0.6220.733 中分化腺癌18810 低分化腺癌271512 印戒细胞癌743转移部位0.2390.625 11789 ≥2351916
1.2 治疗方案 紫杉醇脂质体联合替吉奥组化疗方案:紫杉醇脂质体(南京绿叶药业有限公司生产,30 mg/支),用法:135 mg/m2,d1,加入5%葡萄糖注射液500 mL持续静脉滴注3 h;替吉奥(山东齐鲁制药有限公司生产,20 mg/粒),用法:体表面积<1.25 m2,替吉奥 40 mg/次,2次/日;体表面积1.25~1.5 m2,替吉奥 50 mg/次,2次/日;体表面积>1.5 m2,替吉奥 60 mg/次,2次/日;早、晚餐后30 min各口服1次,d1~14,停药1周,每3周为1个化疗周期,根据患者身体耐受情况化疗6周期,至少化疗2周期,如病情进展或不能耐受则停止化疗。紫杉醇联合替吉奥组化疗方案:紫杉醇(北京双鹭药业股份有限公司,30 mg/支)。抗过敏处理:化疗前12 h、6 h各使用地塞米松20 mg口服,前30 min使用异丙嗪肌肉注射及西咪替丁静推。所有患者化疗前常规给予5-羟色胺受体拮抗剂止吐,化疗后如出现Ⅲ度以上骨髓抑制,予粒细胞集落刺激因子等对症处理。
1.3 观察指标
1.3.1 采用实体瘤通用疗效评价标准(response evaluation criteria in solid tumors,RECIST)[4],分为完全缓解(CR)、部分缓解(PR)、病情稳定(SD)、病情进展(PD)。以总有效率(RR)=(CR+PR)/患者数×100%,疾病控制率(DCR)=(CR+PR+SD)/患者数×100%。2个周期治疗结束后,两组患者进行影像学和肿瘤标记物检查评估临床疗效。
1.3.2 不良反应 采用NCI CTC 3.0毒性评价标准分为0~Ⅳ级。
1.4 统计学方法 采用SPSS 18.0软件进行数据分析,计数资料及组间比较使用χ2检验或Fisher确切概率法,以P<0.05为差异有统计学意义。
2 结果
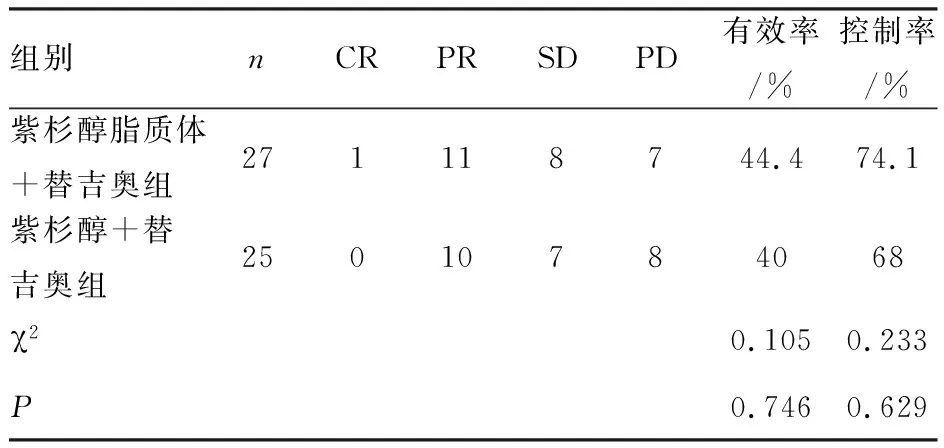
2.1 近期疗效 52例患者经治疗后,仅有1例行紫杉醇脂质体联合替吉奥化疗的患者达到了CR,21例病情评估为PR,两组有效率和疾病控制率差异无统计学意义,见表2。
表2 两组患者临床疗效的比较
组别nCRPRSDPD有效率/%控制率/%紫杉醇脂质体+替吉奥组271118744.474.1紫杉醇+替吉奥组25010784068χ20.1050.233P0.7460.629
2.2 毒副反应 52例患者化疗后均出现不同程度的毒副反应(见表3),予积极对症处理后症状好转,无治疗相关的死亡病例。两组主要毒副反应为骨髓抑制、关节肌肉疼痛、胃肠道反应等,在紫杉醇脂质体联合替吉奥组中,恶心、呕吐发生率(25.9%)与关节肌肉疼痛发生率(18.9%)较紫杉醇联合替吉奥组(56%和52%)降低(P<0.05)。
表3 两组患者化疗后主要毒副作用的比较

毒副反应紫杉醇脂质体+替吉奥组(n=27)紫杉醇+替吉奥组(n=25)Ⅰ~Ⅱ度Ⅲ~Ⅲ度发生率/%Ⅰ~Ⅱ度Ⅲ~Ⅲ度发生率/%χ2P中性粒细胞减少11455.6125680.8490.357血红蛋白减少9448.1103520.0770.781血小板减少6022.270280.2310.631转氨酶异常5018.540160.0160.900恶心、呕吐6125.995564.8770.027腹泻3011.130120.1160.738口腔黏膜炎5122.261360.2310.631关节肌肉疼痛5018.5112526.4300.011脱发13151.9141600.3490.555
3 讨论
胃癌是我国常见恶性肿瘤,与饮食、Hp感染等密切相关[5]。目前晚期胃癌在国际上仍然没有标准的化疗方案,一线化疗疾病缓解率约40%~70%,患者中位生存时间仅为11~14个月[6]。晚期胃癌患者或因胃切除,或因长期胃部不适等导致营养状况较差,不能耐受三药联合化疗的毒副反应,因此两药联合化疗越来越被推广。紫杉醇与氟尿嘧啶类药物的联合化疗方案是晚期胃癌常用的治疗方案之一,两类药物具有协同抗肿瘤治疗作用,一线化疗有效率约43%[7]。
紫杉醇脂质体是使用脂质体磷脂双分子层包封难溶于水的紫杉醇,使其具有更好的组织内分布与缓释作用,增加肿瘤靶向性及疗效,降低药物毒副作用[8]。研究发现在小鼠模型中,紫杉醇脂质体耐受剂量及抗肿瘤效应比普通紫杉醇明显增高[9]。
Chen等[10]报道使用紫杉醇脂质体联合替吉奥治疗胃癌患者,有效率为25%,疾病控制率达到87.5%。日本一项Ⅱ期的临床研究结果显示紫杉醇和氟尿嘧啶类药物联合一线治疗晚期胃癌患者,有效率达到了43%,无疾病进展时间为6.8个月,中位生存时间达到16.2个月,但是骨髓抑制及肌肉疼痛发生率较高[7]。我们的研究结果也与之相似,两组的疾病缓解率分别为44.4%和40%,控制率分别为74.1%和68%,但是在毒副反应方面,紫杉醇脂质体组较紫杉醇组具有优势,胃肠道反应和关节肌肉疼痛的发生率降低,患者生活质量得到提高,化疗毒副作用能够耐受。在本研究中,两组患者贫血的发生率较高,考虑与长期上消化道慢性失血有关,给予纠正贫血等支持治疗,待患者一般状况明显改善后再行化疗。
综上所述,紫杉醇脂质体可以在提高抗肿瘤治疗效果的同时,减少药物毒副反应。而且紫杉醇脂质体在应用前无需大剂量、反复使用激素预处理,是禁忌使用大剂量激素患者的理想选择,尤其在老年患者中耐受良好,值得临床推广使用。但是紫杉醇脂质体较贵,经济因素也需要考虑,因此临床治疗时,需综合考虑患者病情、身体状况及经济条件等实施个体化的治疗方案。
【参考文献】
[1] TORRE LA,BRAY F,SIEGEL RL,etal.Global cancer statistics,2012[J].CA:a cancer journal for clinicians,2015,65(2):87-108.
[2] Cancer Genome Atlas Research Network.Comprehensive molecular characterization of gastric adenocarcinoma[J].Nature,2014,513(7517):202-209.
[3] OHTSU A,YOSHIDA S,SAIJO N.Disparities in gastric cancer chemotherapy between the East and West[J].J Clin Oncol,2006,24(14):2188-2196.
[4] THERASSE P,ARBUCK SG,EISENHAUER EA,etal.New guidelines to evaluate the response to treatment in solid tumors.European Organization for Research and Treatment of Cancer,National Cancer Institute of the United States,National Cancer Institute of Canada[J].J Natl Cancer Inst,2000,92(3):205-216.
[5] YAN S,LI B,BAI ZZ,etal.Clinical epidemiology of gastric cancer in Hehuang valley of China:a 10-year epidemiological study of gastric cancer[J].World J Gastroenterol,2014,20(30):10486-10494.
[6] ROTH AD,FAZIO N,STUPP R,etal.Docetaxel,cisplatin,and fluorouracil;docetaxel and cisplatin;and epirubicin,cisplatin,and fluorouracil as systemic treatment for metastaticd gastric carcinoma:a randomized phase Ⅱ trial of the Swiss Group for Clinical Cancer Research[J].J Clin Oncol,2007,25(22):3217-3223.
[7] MATSUBARA J,SHIMADA Y,KATO K,etal.Docetaxel,cisplatin,and fluorouracil;docetaxel and cisplatin;and epirubicin,cisplatin and fluorouracil as systemic treatment for metastaticr gastric carcinoma:a randomized phase Ⅱ trial of the Swiss group for clinical cancer Research.Phase Ⅱ study of bolus 5-fluorouracil and leucovorin combined with weekly paclitaxel as first-line therapy for metastaticd gastric cancer[J].Oncology,2011,81(5-6):291-297.
[8] KOBAYASHI M,TSUBURAYA A,NAGATA N,etal.A feasibility study of sequential paclitaxel and S-1 (PTX/S-1) chemotherapy as postoperative adjuvant chemotherapy for metastaticd gastric cancer[J].Gastric Cancer,2006,9(2):114-119.
[9] YOSHIZAWA Y,KONO Y,OGAWARA K,etal.PEG liposomalization of paclitaxel improved its in vivo disposition and anti-tumor efficacy[J].Int J Pharm,2011,412(1-2):132-141.
[10] CHEN L,CHEN Q,ZHUANG Z,etal.Effect of the weekly administration of liposome-Paclitaxel combined with S-1 on metastaticd gastric cancer[J].Jpn J Clin Oncol,2014,44(3):208-213.

