CaO2投加量及投加方式对剩余污泥厌氧发酵产生短链脂肪酸的影响
桂肖山,徐 闯,王泽茜,平 倩,李咏梅
CaO2投加量及投加方式对剩余污泥厌氧发酵产生短链脂肪酸的影响
桂肖山,徐闯,王泽茜,平倩,李咏梅*
(同济大学环境科学与工程学院,污染控制与资源化研究国家重点实验室,上海 200092)
以污水处理厂剩余活性污泥作为研究对象,在中温条件下,按照不同投加量和投加方式投加过氧化钙(CaO2)进行预处理,考察其对污泥发酵产酸和产甲烷的影响,以期确定CaO2最佳投加量和投加方式.结果表明,在(35±1)℃条件下,投加CaO2可提高剩余污泥发酵液pH值,从而促进有机物的快速溶出.在同样投加剂量条件下,一次性投加比多次投加更有利于污泥的溶解以及短链脂肪酸的积累.当一次性投加0.2g CaO2/g VSS时,发酵液中乙酸浓度在第7d达到最高值(169mg COD/g VSS),同时乙酸在6种主要酸中所占比例达到最大(71.0%).与一次性投加方式相比较,多次投加CaO2对产甲烷的抑制作用较小,不利于SCFAs的积累.
过氧化钙;剩余污泥;厌氧发酵;投加量;投加方式
目前,世界范围内应用最为广泛的污水处理方法是活性污泥法.活性污泥工艺历经100多年的研究和应用,演变出多种各具特色的运行方式,但各种运行方式都难以避免大量剩余污泥的产生[1].据估算,我国城市污水处理厂每年排放的污泥量(干重)大约为900万t,占我国总固体废弃物量的3.2%,而且年增长率大于10%[2],其处理处置费用通常占污水处理总成本的20%~50%[3].剩余活性污泥的处理和处置成本较高,是污水处理厂操作运营的主要难题之一.剩余活性污泥中有机物含量高,若能对其进行回收利用,将节约成本并达到污泥减量化、资源化的目的[2-4].厌氧发酵是目前应用最为广泛的剩余活性污泥处理方法之一.剩余活性污泥厌氧发酵一般包括水解、产酸、产甲烷三个阶段.增强水解和产酸的效果并抑制产甲烷过程,可以达到累积挥发性短链脂肪酸(包括乙酸、丙酸、异丁酸、丁酸、异戊酸、戊酸)的目的[5].挥发性短链脂肪酸可作为外加碳源应用于污水处理厂的生物反硝化脱氮和生物除磷过程,并取得良好的效果,从而为缓解我国城市尤其是南方城市污水处理厂碳源不足的问题提供可行方案[2-6].
过氧化钙(CaO2)是一种白色或浅黄色固体粉末,在潮湿介质中可缓慢释放出O2(式1).其溶解于水生成H2O2和Ca(OH)2(式2),理论上1g CaO2可释放出0.47g H2O2和1.03g Ca(OH)2[7]. H2O2和Ca(OH)2都具有促进污泥溶解,提高厌氧发酵速率的功能,而且H2O2通过产生羟基自由基等活性氧自由基还可以氧化污泥中的难降解有机物[8].近年来对于剩余污泥预处理的研究表明,采用CaO2既可促进剩余污泥厌氧发酵的水解和产酸阶段,并有效抑制其产甲烷阶段,亦可降解多种吸附在污泥表面的有毒难降解有机物,从而提高污泥发酵液的质量[8-9].
2CaO2+2H2O®O2+2Ca(OH)2(1)
CaO2+2H2O®H2O2+Ca(OH)2(2)
本研究以CaO2作为添加剂对剩余污泥进行预处理,研究不同CaO2投加量和投加方式对厌氧发酵的影响,重点考察其对于剩余污泥产生短链脂肪酸的影响,以期确定有利于污泥产酸的最佳CaO2投加量和投加方式.
1 材料与方法
1.1 剩余污泥来源与性质
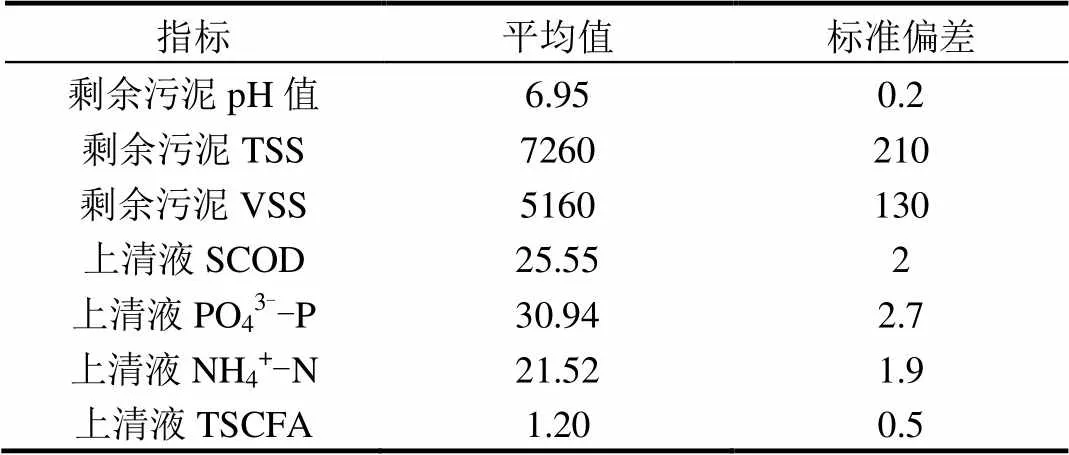
表1 剩余活性污泥及上清液初始性质
注:除pH值外,其余指标单位均为mg/L.
剩余活性污泥取自上海曲阳污水厂回流泵房,经沉淀浓缩24h后,弃去上清液,并过1mm´1mm的筛网以除去其中的杂质颗粒.浓缩污泥经离心后取上清液分别测定pH值、NH4+-N、PO43--P、总短链脂肪酸(TSCFA)、总悬浮固体(TSS)、挥发性悬浮固体(VSS)等指标.剩余污泥初始性质如表1.
1.2 CaO2投加量和投加方式对剩余污泥厌氧消化的影响试验
为分别探究相同投加方式下不同投加量、相同投加量下不同投加方式对污泥厌氧消化的影响,共设置8组实验,同时设不投加CaO2组作为对照,如表2所示.
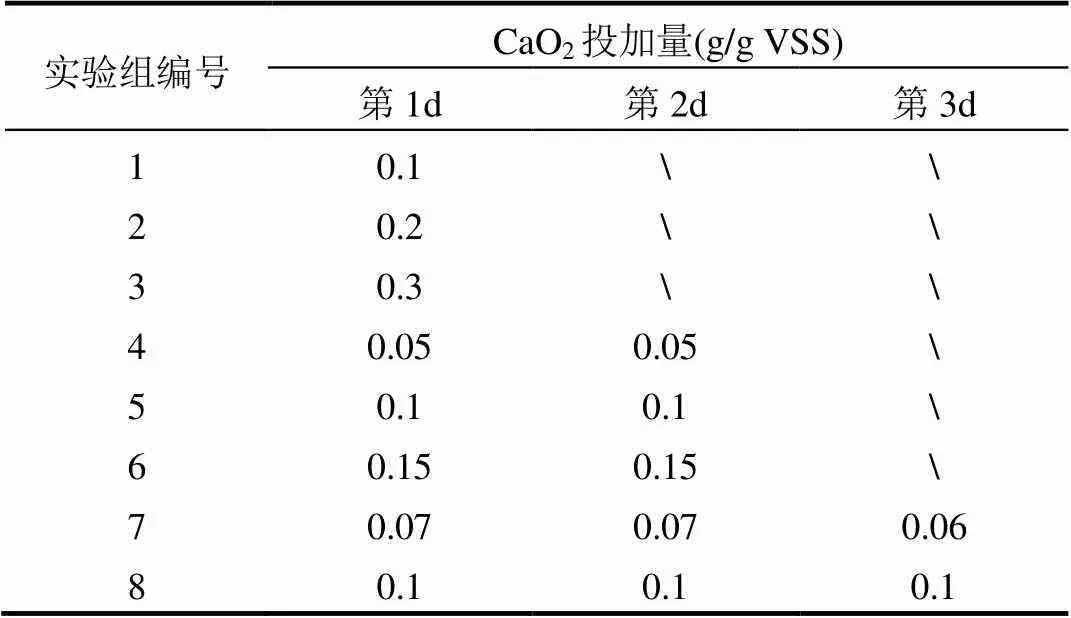
表2 不同实验组CaO2投加量与投加方式
在每组试验中,取450mL剩余活性污泥于600mL盐水瓶中,按表2投加CaO2,盐水瓶上方的空气通过氮吹去除,使用橡胶塞封口以维持厌氧环境,每组实验设置两个平行,放置在恒温摇床(35±1)℃中进行厌氧发酵,转速设置为120r/min.定期取样测定厌氧发酵气体中CH4含量及污泥上清液中的pH值、SCOD、SCFAs、NH4+-N的含量.
1.3 分析测试方法
pH值的测定使用Cyberscan510型pH计(Eutech, Singapore),在泥水混合物取样前将探头伸入盐水瓶中测定.泥水混合物取样后以10000r/min离心15min,取上清液测定SCOD、NH4+-N,上清液经0.45μm滤膜过滤至1.5mL气相小瓶中,加入0.1μL3%的磷酸溶液后测定SCFAs. TSS、VSS、SCOD、NH4+-N采用国家标准方法测定[10].SCFAs采用气相色谱仪(Agilent GC6890)测定[11].CH4含量采用装配有热导池检测器的GC-14B气相色谱仪测定[11].
2 结果与讨论
2.1 污泥发酵液pH值的变化
加入CaO2后,8个实验组发酵液的pH值整体呈现出先升高后下降趋势,pH值至第13d达到稳定,且最终pH值皆在7.1~7.5之间(图1).这是由于加入CaO2后,CaO2与水反应产生Ca(OH)2,使pH值迅速上升,之后由于厌氧发酵产酸作用,pH值逐渐下降,直至酸碱度达到平衡,pH值趋于稳定.从总体趋势来看,CaO2投加量越大,pH值变化越大.原因为随着CaO2投加量增加,污泥中产生的Ca(OH)2的量也等量增加,因此pH值增加.对照组由于未进行预处理,不能快速有效地破坏细胞壁,水解产酸速度相对较慢,因此pH值只在发酵初期略微下降,发酵5d后则在6.75附近波动.
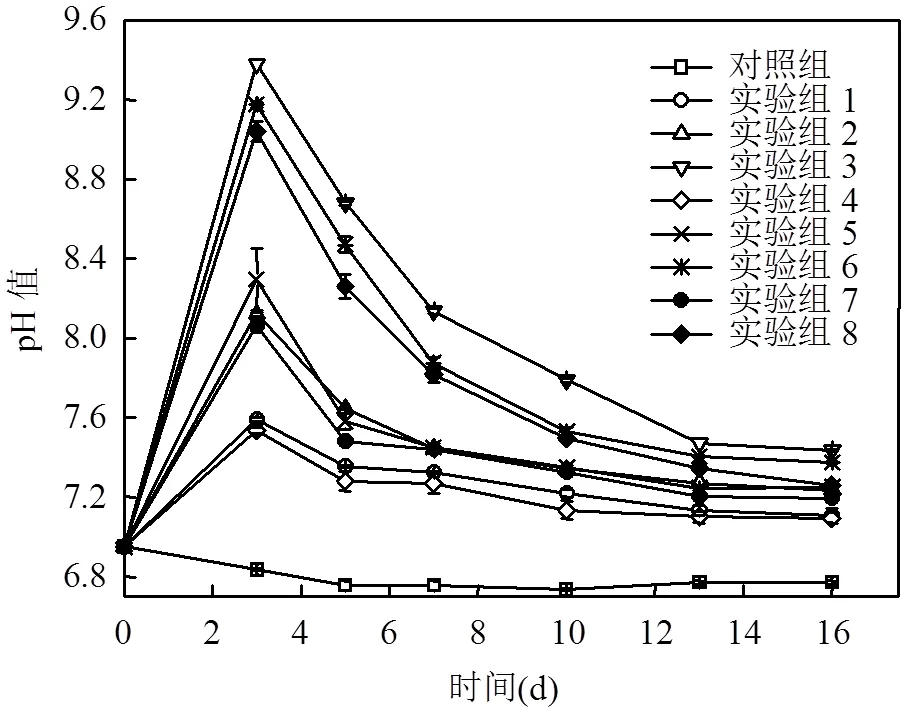
图1 不同CaO2投加量和投加方式下污泥发酵液pH值的变化
2.2 污泥发酵液SCOD的变化
由图2可见,发酵液中SCOD变化趋势受不同CaO2投加量和投加方式的显著影响. 16d内CaO2投加量较大(0.2~0.3g/g VSS)时发酵液中的SCOD明显高于CaO2投加量较少(0.1g/g VSS)时的SCOD浓度.当CaO2投加量较大时,SCOD在3d内呈快速上升趋势,之后10d内保持缓慢上升趋势,10d后开始下降.
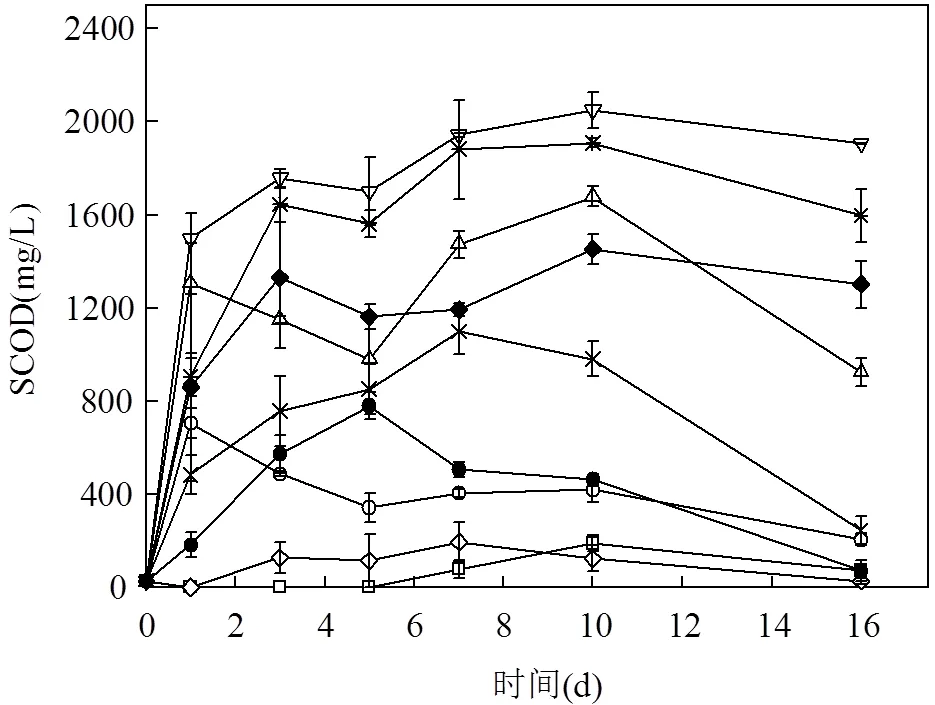
图2 不同CaO2投加量和投加方式下污泥发酵液SCOD的变化

这是由于发酵液中SCOD累积量由其产生速率及消耗速率决定. CaO2投加3d内,较强碱性发酵液使得剩余活性污泥的水解进程加快,促进分解污泥的胞外聚合物(EPS)[12-13].EPS的分解使得污泥细胞暴露在碱性pH值环境中,此时,碱预处理生成的OH·可进一步促进污泥细胞壁、细胞膜、细胞核等细胞器的分解[13].同时,投加的CaO2与水反应生成的H2O2可促进污泥水解进程[14],从而使其SCOD迅速上升.而CaO2投加量较小时, SCOD在前3d积累,此后变化趋势较为缓和,10d后开始下降.此趋势可能的原因是过低的CaO2投加量不足以提供碱性环境及氧化剂,故发酵液中SCOD的积累和消耗速率都比较低. Neyens[14]及Tokumura等[15]研究显示,剩余污泥厌氧发酵液中SCOD来自于细菌胞内物质及EPS,较强碱条件下污泥细胞颗粒被破坏,从而释放出胞内物质[14];而根据Yu等[16]的研究,胞外聚合物中含有大量水解酶,因此随着投加的CaO2促进溶解胞外聚合物,水解酶被大量释放至发酵液中[9],从而加快其中SCOD的积累过程.图2还表明,同样CaO2投加量下,一次性投加产生的SCOD量最大,投加分次越多,产生的SCOD量越少.
2.3 污泥发酵液中NH4+-N的变化
实验显示,随着时间的推移,污泥发酵液中的NH4+-N浓度整体呈现出上升趋势(图3).高剂量、一次性投加CaO2的实验组发酵液中NH4+-N浓度高于低剂量、分次投加CaO2的发酵液中NH4+-H浓度.发酵时间达16d时,一次性投加0.3g CaO2/g VSS的条件下,发酵液中NH4+-N浓度最高,为271mg/L;对照组发酵液NH4+-N浓度最低,为168mg/L.因此CaO2溶于水产生的较强碱性和强氧化剂共同作用促进了污泥水解发酵以及NH4+-N的产生和释放.污泥发酵液中的氨氮后续需要进一步处理或资源化利用.
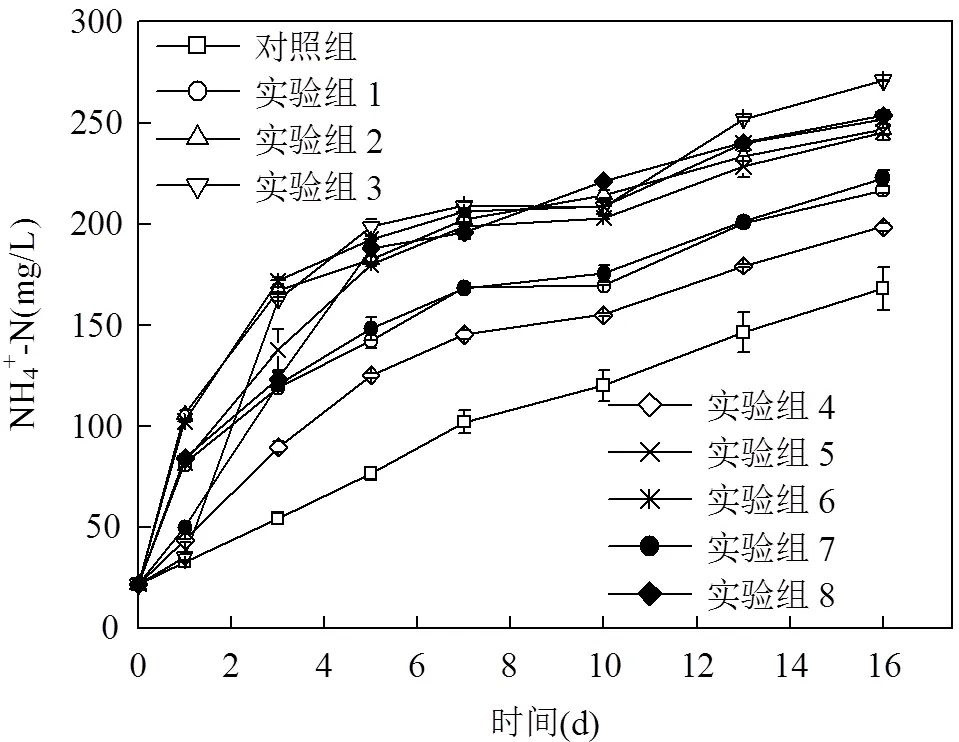
图3 不同CaO2投加量和投加方式下污泥发酵液NH4+-N的浓度变化
2.4 污泥发酵液TSCFA和CH4产量的变化
不同CaO2投加量和投加方式对污泥发酵液TSCFA的影响如图4所示.各组TSCFA产生量在发酵初期迅速增大,在5~8d后开始下降(图3~图5).当CaO2投加量一定、而投加次数不同时,一次投加在前7d产生的TSCFA高于多次投加的情形,而7d之后TSCFA浓度下降幅度也明显快于多次投加CaO2时发酵液中TSCFA浓度.根据前面的分析,一次投加CaO2时短时间内产生的H2O2和Ca(OH)2更多,较强的碱性和氧化性有利于破坏细胞壁,促进污泥水解产酸[17-18],而同样CaO2投加量分多次投加会使条件更温和,污泥SCOD降低,从而产酸量也减少.
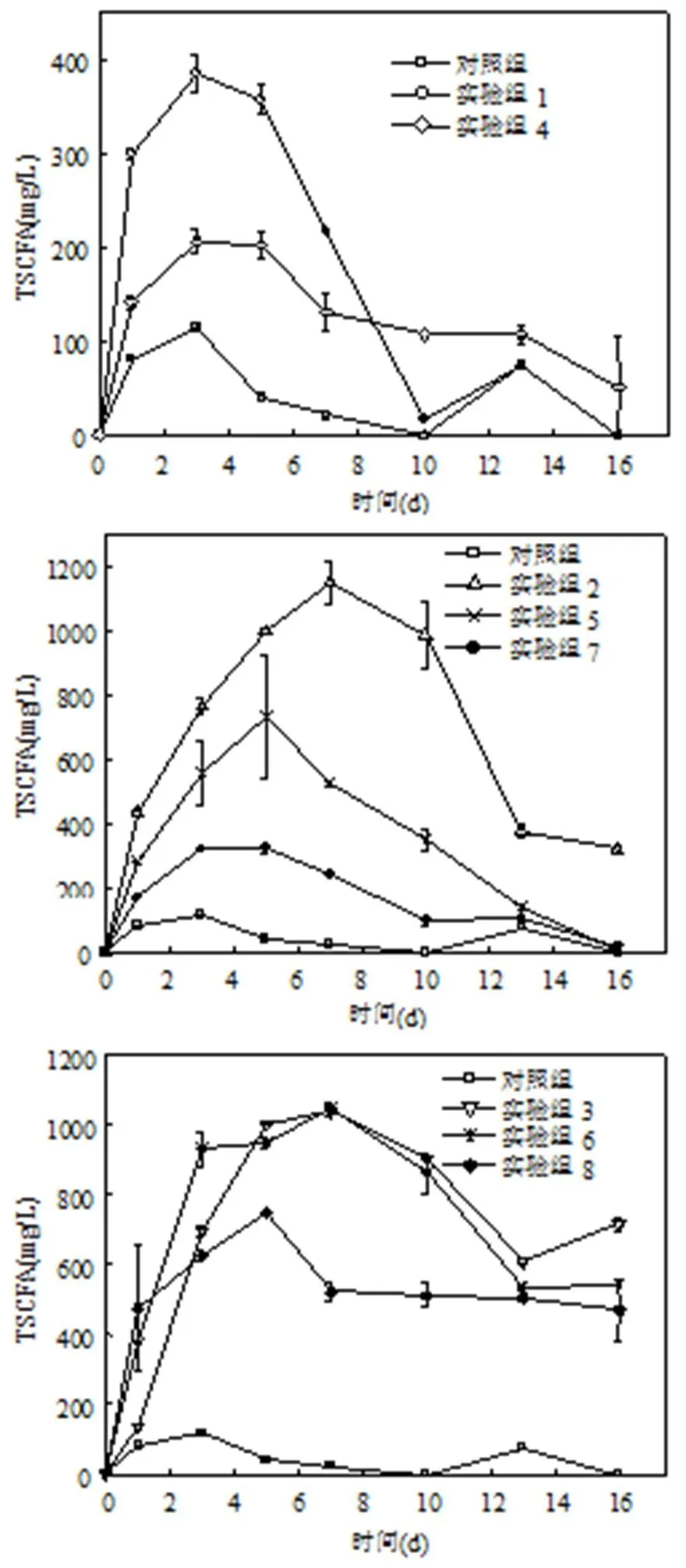
图4 不同CaO2投加量和投加方式时污泥发酵液中TSCFA的变化
(a)投加量为0.1g CaO2/g VSS,(b)投加量为0.2g CaO2/g VSS, (c)投加量为0.3g CaO2/g VSS
当一次投加时,CaO2投加量为0.2g/g VSS和0.3g/g VSS的实验组发酵液中TSCFA浓度大大高于投加量为0.1g/g VSS实验组及对照组,而投加0.2g/g VSS的发酵液在5~10d中产生的TSCFA高于CaO2投加量为0.3g/g VSS的发酵液.特别是当一次性投加0.2gCaO2/g VSS时,发酵液中TSCFA的浓度在第7d达到所有实验组的最高值1152mg/L.这是由于投加0.2和0.3g/g VSS时发酵液初始pH值较大,有利于破坏污泥絮体和细胞壁并促进有机物的降解[15,17,19],从而促进水解过程产生的氨基酸和单糖转化为SCFA[18].根据前面对于pH值变化的分析,投加0.3g CaO2/gVSS时发酵液的碱性过强.Chen等[5]的研究表明,强碱性环境下产酸菌的活性和水解酶及产酸酶的活性受到抑制,继而阻碍了TSCFA的积累过程,因此投加0.3g CaO2/gVSS时TSCFA的产生量反而小于投加0.2g CaO2/ gVSS的实验组.所以投加0.2g CaO2/g VSS产生的碱性和氧化性较合适,为产酸菌提供了更好的环境.
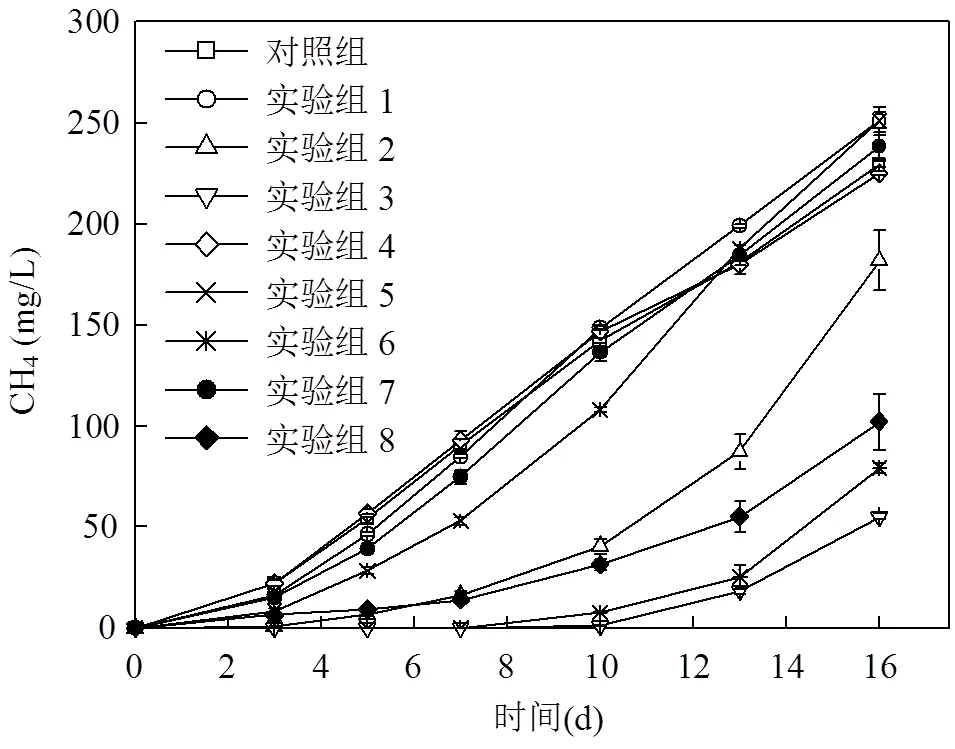
图5 不同CaO2投加量和投加方式下污泥发酵产生CH4的变化
各组污泥发酵过程中CH4产生量与对应上清液pH值及其TSCFA产生量呈现出较紧密的关联性.投加CaO2后,低剂量、分次投加CaO2的实验组CH4产量明显高于高剂量、一次性投加CaO2的实验组CH4产量(图5).对照图1中各组发酵液pH值变化趋势可知,采取高剂量、一次性投加CaO2的实验组在1~10d内造成污泥发酵上清液pH值较高,强烈抑制了甲烷菌的活性,而在投加后10~16d,CH4产生速率才开始显著增加,这是由于CaO2投加10d后,pH值降至7.8以下,有利于甲烷菌的恢复,且此阶段发酵液中积累了较多TSCFA,因此CH4转化速率加快,进而造成TSCFA的消耗,对应图4中TSCFA在产CH4受抑制时呈现持续增加趋势,而在CH4产量上升时呈下降趋势.
2.5 污泥发酵液中各种短链脂肪酸的变化
为了确定最合适的CaO2投加量和投加方式,选取一次投加0.1g CaO2/g VSS,一次投加0.2g CaO2/g VSS,两次投加0.2g CaO2/g VSS,一次投加0.3g CaO2/g VSS四种投加方式,结合对照组进行各种SCFA产量分析.如图6所示,乙酸是产量最高的酸,丙酸和异戊酸居于其次.和对照组各种SCFA产量相比,四种投加方式都使得发酵液中各种SCFA产量大幅度提升,其中以乙酸积累量最为显著.另一方面,不同CaO2投加方式都造成乙酸在5~7d内迅速积累,投加0.1g CaO2/g VSS和0.2g CaO2/g VSS分两次投加时发酵液5d之后乙酸含量迅速降低;一次性投加0.2g CaO2/g VSS时,发酵液中乙酸含量在7~16d保持较缓和的下降速度,而投加0.3g CaO2/g VSS时,乙酸浓度几乎没有下降,此现象与该条件下甲烷产量很低相对应,说明投加0.3g CaO2/g VSS时严重抑制了利用乙酸的甲烷菌活性.作为一种结构简单的小分子脂肪酸,乙酸可被甲烷菌直接分解生成CH4和CO2气体[20],而由于投加高剂量CaO2产生的高pH值环境对于甲烷菌活性有很强的抑制作用,故一次性投加过高剂量CaO2会抑制甲烷菌,使得乙酸在发酵液中积累.不同CaO2投加方式中,一次投加0.2gCaO2/g VSS时,发酵液中乙酸浓度在第7d达到所有组别中的最高值,为169mg COD/g VSS(818mg/L),且乙酸在6种主要酸中所占比例同时达到最大,为71.0%.
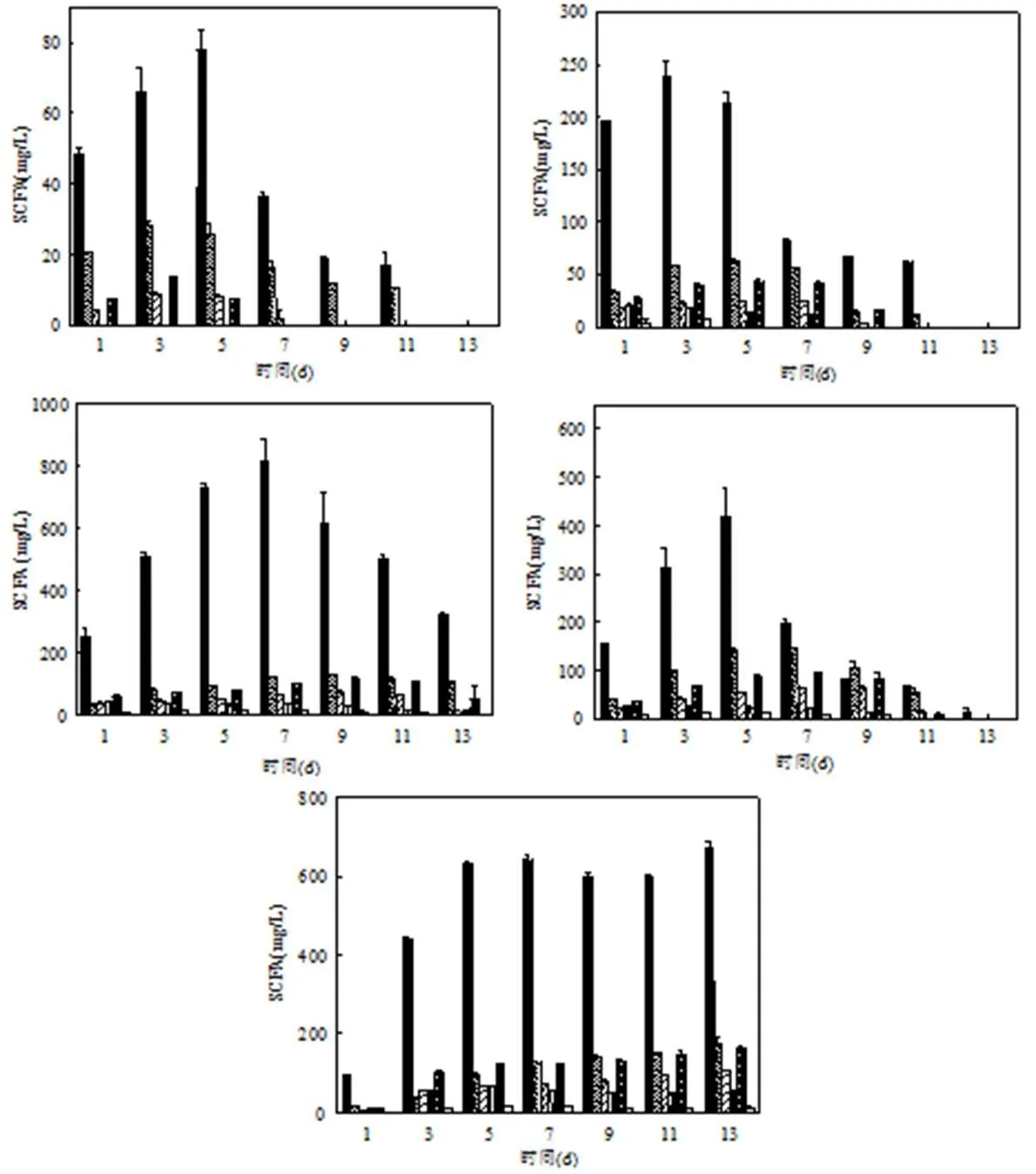
图6 不同CaO2投加量和投加方式下污泥发酵液中各种SCFA的变化
(A:乙酸; P:丙酸; iso-B:异丁酸; n-B:正丁酸; iso-V:异戊酸; n-V:正戊酸) (a) 对照组, (b) 一次投加0.1g CaO2/g VSS, (c)一次投加0.2g CaO2/g VSS, (d)两次投加0.2g CaO2/g VSS,(e)一次投加0.3g CaO2/g VSS

肖本益等人[21]对于初始VSS为6190mg/L, SCOD为113.7mg/L的剩余污泥采用6mol/L NaOH进行碱处理,得到发酵液中VFA浓度约为38.8mg COD/g VSS (240mg/L).本研究中投加CaO2可同时产生强氧化物质H2O2[14],且瞬时产生的OH·可有效破坏污泥细胞EPS和细胞器[13],故相比普通碱预处理法中只能依靠碱性破坏污泥结构和促进厌氧发酵,CaO2的投加明显提升了污泥的产酸能力.且按照一次性0.2gCaO2/g VSS的投加方式有利于获取产量大、乙酸含量高的酸性发酵液.
3 结论
3.1 加入CaO2后,污泥pH值快速上升,3d后随着TSCFA的产生呈下降趋势,13d后稳在7.1~ 7.5.
3.2 CaO2显著促进剩余污泥在中温条件下(35±1)℃的水解产酸,表现为污泥发酵液SCOD、NH4+-N及TSCFA明显升高.
3.3 与一次性投加CaO2相比,多次投加CaO2使得发酵液pH值及氧化性变化幅度更加缓和,相对温和的条件不利于SCFAs的积累.
3.4 投加CaO2使污泥厌氧发酵产生的SCFAs中乙酸含量最高、浓度变化幅度最大.投加方式为一次性投加0.2g CaO2/g VSS时,发酵液中乙酸浓度在第7d达到最高值(169mg COD/g VSS),同时乙酸在主要酸中所占比例达到最大,为71.0%.
[1] 代学民,王 霞,马云霞,等.浅谈活性污泥法的发展和演变[J]. 河北建筑工程学院学报, 2004,22(2):25-27.
[2] 裴晓梅,余志亚,朱洪光.我国厌氧发酵处理城市污水剩余污泥研究进展[J]. 中国沼气, 2008,26(1):25-29.
[3] 周爱娟.预处理促进剩余污泥发酵制取短链脂肪酸的效能及机制研究[D]. 哈尔滨:哈尔滨工业大学, 2014.
[4] 张万钦,戚丹丹,吴树彪,等.不同预处理方式对污泥厌氧发酵的影响[J]. 农业机械学报, 2014,45(9):187-198.
[5] Chen Y, Jiang S, Yuan H, Zhou Q, Gu G. Hydrolysis and acidification of waste activated sludge at different pHs [J]. Water Research, 2007,41(3):683-689.
[6] 张玲玲,陈 立,郭兴芳,等.南北方污水处理厂进水水质特性分析 [J]. 给水排水, 2012,48(1):45-49.
[7] Northup A, Cassidy D. Calcium peroxide (CaO2) for use in modified Fenton chemistry [J]. Journal of Hazardous Materials, 2008,152(3):1164-1170.
[8] Zhang A, Li Y. Removal of phenolic endocrine disrupting compounds from waste activated sludge using UV, H2O2, and UV/H2O2oxidation processes: Effects of reaction conditions and sludge matrix [J]. Science of The Total Environment, 2014, 493:307-323.
[9] Li Y, Wang J, Zhang A, Wang L. Enhancing the quantity and quality of short-chain fatty acids production from waste activated sludge using CaO2as an additive [J]. Water Research, 2015,83:84-93.
[10] 国家环境保护总局《水和废水监测分析方法》编委会.水和废水监测分析方法(第四版) [M]. 中国环境科学出版社, 2002.
[11] Wang J, Li Y. Synergistic pretreatment of waste activated sludge using CaO2in combination with microwave irradiation to enhance methane production during anaerobic digestion [J]. Applied Energy, 2016,183:1123-1132.
[12] Jin Y, Li H, Mahar R B, Wang Z, Nie Y. Combined alkaline and ultrasonic pretreatment of sludge before aerobic digestion [J]. Journal of Environmental Sciences, 2009,21(3):279-284.
[13] Xiao B, Liu C, Liu J, Guo X. Evaluation of the microbial cell structure damages in alkaline pretreatment of waste activated sludge [J]. Bioresource Technology, 2015;196(Supplement C): 109-115.
[14] Neyens E, Baeyens J, Creemers C. Alkaline thermal sludge hydrolysis [J]. Journal of Hazardous Materials, 2003,97(1–3): 295-314.
[15] Tokumura M, Katoh H, Katoh T, et al. Solubilization of excess sludge in activated sludge process using the solar photo-Fenton reaction [J]. J. Hazard. Mat., 2009,162(2/3):1390-1396.
[16] Yu G-H, He P-J, Shao L-M, He P-P. Toward understanding the mechanism of improving the production of volatile fatty acids from activated sludge at pH 10.0 [J]. Water Research, 2008, 42(18):4637-4644.
[17] Erden G, Filibeli A. Ozone oxidation of biological sludge: Effects on disintegration, anaerobic biodegradability, and filterability [J]. Environmental Progress & Sustainable Energy, 2011,30(3):377-383.
[18] Luo J, Feng L, Chen Y. Stimulating short-chain fatty acids production from waste activated sludge by nano zero-valent iron [J]. Journal of Biotechnology, 2014,187:98-105.
[19] Wang Y, Wei Y, Liu J. Effect of H2O2dosing strategy on sludge pretreatment by microwave-H2O2advanced oxidation process [J]. Journal of Hazardous Materials, 2009,169(1–3):680-684.
[20] Liu Y, Li X, Kang X, et al Short chain fatty acids accumulation and microbial community succession during ultrasonic-pretreated sludge anaerobic fermentation process: Effect of alkaline adjustment [J]. International Biodeterioration& Biodegradation, 2014,94(36):128-133.
[21] 肖本益,刘俊新.不同预处理方法对剩余污泥性质的影响研究[J]. 环境科学, 2008,29(2):2327-2331.
Effects of the dosage and dosing methods of CaO2on the production of short-chain fatty acids produced during anaerobic fermentation of waste activated sludge.
GUI Xiao-shan, XU Chuang, WANG Ze-qian, PING Qian, LI Yong-mei*
(State Key Laboratory of Pollution Control and Resources Reuse, College of Environmental Science and Engineering, Tongji University, Shanghai 200092, China)., 2018,38(5):1785~1791
CaO2was added under mesophilic conditions for the pretreatment of waste activated sludge (WAS) obtained from wastewater treatment plants (WWTP). The effects of CaO2dosage and dosing methods on the acidification and methane production during anaerobic fermentation were evaluated. The aim was to find the optimum dosage and dosing method of CaO2for obtaining short chain fatty acids (SCFAs) from WAS. The results indicated that at (35±1)℃, CaO2addition could remarkably increase pH of the supernatant, thus accelerating the release of organic matters. Given the constant dosage, the once-and-for-all dosing of CaO2could enhance the solubilization of WAS and the accumulation of SCFAs much more effectively than multiple dosing of CaO2. When CaO2was dosed at 0.2g/g VSS for once, the acetic acid concentration witnessed its highest level (169mg COD/g VSS) on day 7 and accounted for 71.0% of the total SCFAs, eclipsing all the other acids. Compared with the once-and-for-all dosing method, multiple dosing of CaO2resulted in less accumulation of SCFA due to weaker inhibition of methane production.
CaO2;waste activated sludge;anaerobic fermentation;dosage;dosing methods
X703
A
1000-6923(2018)05-1785-07
2017-10-09
国家自然科学基金资助项目(51578392);2015年国家大学生创新项目(0400107139)
* 责任作者, 教授, liyongmei@tongji.edu.cn
桂肖山(1997-),男,安徽芜湖人,同济大学环境科学与工程学院环境工程系本科学生,主要从事污水处理与资源化研究.

