门脉高压症的检查选择与病因诊断*
陈世耀,黄晓铨,曾晓清
门脉高压症(portal hypertension,PHT)的定义为门静脉与下腔静脉压力差大于5 mmHg。由于门脉压力增加导致的全身内脏动脉血管扩张,高动力循环状态伴发门体侧支循环形成,加速相关并发症的发生。其常见的并发症包括食管胃静脉曲张破裂出血、脾功能亢进症、难治性腹水、肝性脑病、自发性细菌性腹膜炎等。一般认为食管胃静脉曲张破裂出血在肝静脉压力梯度(hepatic venous pressure gradient,HVPG)大于12 mmHg时出现。当HVPG大于20 mmHg时,其出血和死亡风险增加5倍[1]。门脉高压及其相关并发症是目前肝硬化最严重的临床问题和死亡原因,严重影响患者预后及生活质量,死亡率高,消耗巨大的社会医疗资源,给患者家庭带来巨大的经济负担[2]。
1 病例介绍
50岁女性,因腹胀1月就诊,不伴有呕血、黑便、牙龈出血、皮肤瘀斑等。既往体健,无中药等药物服用史,无烟酒嗜好。实验室检查提示血红蛋白121 g/L,血小板 85×109/L,白细胞 2.9×109/L;肝肾功能、肝炎病毒标记物和自身抗体等实验室检查指标均为阴性,JAK2、骨髓穿刺包括BCR-ABL等相关基因检查全部为阴性。超声检查提示肝内钙化灶,胆囊壁毛糙,肠系膜上静脉局部囊状扩张,脾肿大,脾静脉迂曲扩张并延伸至右上腹;腹部CT检查提示胃大弯侧和脾门多发迂曲血管团;脾肿大,脾内后缘实质强化欠均匀,考虑缺血性改变可能,胰腺萎缩,下腹部和盆腔少量积液;门脉CTV检查提示门脉高压、脾静脉闭塞、脾门多发迂曲的血管与腹腔内血管和门静脉相交通(图1a、1b);胃镜检查提示孤立胃底大弯巨大曲张静脉团(图1c),超声胃镜提示腔外血管池融合(图1d);超声弹性成像提示肝右叶弹性硬度值正常。
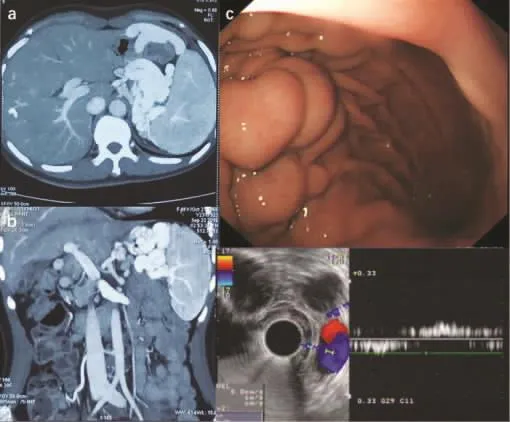
图1 相关检查表现
2 门脉高压症的临床表现和诊断
门脉高压的主要原因是肝硬化导致的肝窦阻力增加,导致HVPG升高。然而,部分非肝硬化导致的门脉高压(non-cirrhotic PHT,NCPH) 患者HVPG正常或仅是轻度升高,显著低于门脉压力。
2.1 临床表现 很多非肝硬化门脉高压症患者往往在出现并发症后才受到关注和诊断,其中最常见且最凶险的并发症是门脉高压伴食管胃静脉曲张破裂出血。少数以巨脾、脾功能亢进症等作为首诊原因。肝硬化门脉高压症患者容易发展成为难治性腹水,而约50%非肝硬化性门脉高压症患者有腹水,由极高的门脉压力引起,在病因去除后腹水很容易消失。肝性脑病在肝硬化患者中较常见,而在非肝硬化门脉高压患者中较少发生[3]。尽管非肝硬化门脉高压引起的肝肾综合征和肝肺综合征非常罕见,但是也有研究指出约10%非肝硬化性门脉高压患者同时合并肺部疾病[4]。
2.2 实验室检查 肝硬化引起的门脉高压及其肝脏损害可以出现肝功能、凝血功能、糖和脂肪酸代谢指标的异常。丙氨酸氨基转移酶(ALT)是反映肝细胞损害及坏死程度的特异性指标,但不能反映肝脏储备功能。即使是失代偿期肝硬化,在无进一步的肝细胞坏死时,ALT仍可维持在正常水平。另一个氨基转移酶的指标天冬氨酸氨基转移酶(AST)与ALT的比值可以帮助判断肝硬化的原因,如AST/ALT大于3对酒精性肝病的诊断有提示意义[5]。Child-Turcotte-Pugh评分被广泛应用于手术和肝硬化预后的评估。无论是否肝硬化门脉高压,血小板计数结合脾脏大小是门脉高压继发脾功能亢进症的表现。在非肝硬化性门脉高压患者脾肿大伴血小板减少是预后不良的指标[6]。肝纤维化标志物能够直接评价肝组织内细胞外基质(ECM)的代谢情况,包括I型和III型前胶原和IV型胶原、透明质酸、层黏蛋白等糖蛋白及基质金属蛋白酶和金属蛋白酶组织抑制物。与肝纤维化形成、门脉高压发生相关的细胞因子有TGF-β1等。FibroTest是一组检测肝纤维化的生化标志物,结合GGT、胆红素、结合珠蛋白、载脂蛋白A1和α2巨球蛋白含量,并根据受试者年龄和性别调整,在诊断肝纤维化和肝硬化方面有较高的准确性。一项对16项肝纤维化和13项肝硬化研究的Meta分析发现,FibroTest对于排除慢性乙型肝炎相关的肝硬化有较好的价值,门脉高压的血清学标志物在不同原因的门脉高压中其敏感度和特异度也有所不同[7]。门脉压力升高将会增加内脏血管压力,引起肾素-血管紧张素-醛固酮(RAAS)系统激活和抗利尿激素分泌,导致水钠潴留,进一步加重门脉高压。肝硬化门脉高压伴随系统炎症状态,有研究提示代偿期肝硬化患者血清IL-1β、IL-1R、Fas-R和VCAM-1水平与肝静脉压力梯度显著相关[8],但对于非肝硬化性门脉高压患者的系统炎症变化情况尚未有研究报道。非肝硬化门脉高压一般不伴肝功能损伤,但是长期的门脉压力增高也可能造成继发肝脏损伤,引起肝硬化。肝后因素引起的门脉高压存在淤血肝脏损害,肝前因素引起的门脉高压也可能因为长期过量向肝血流的影响导致继发性改变。
2.3 影像学检查 影像学检查关注肝脏质地和血管走向,包括肝脏超声、肝脏CT和门脉血管CTV、肝脏MRI、超声弹性成像等,在协助门脉高压的诊断和治疗方案选择上发挥了越来越重要的作用。
腹部超声检查是最简便、安全的手段,可以作为门脉高压的首选检查及随访工具。门脉系统超声检查可以明确肝脏质地形态、判断门脉血管内径、门脉血流速度、发现门静脉和肝静脉血栓。超声检查发现门脉高压的征象特异度高,但是敏感性一般,特别是对于代偿期肝硬化的诊断。因此,当超声检查没有出现门脉高压的特异性征象时,不能排除门脉高压的诊断。只有当门体侧支循环形成(如脐静脉开放、脾肾分流等侧枝循环形成)和门脉系统血流由三相波转变为双向波或单相波时对门脉高压诊断才有更高的特异性[9]。超声弹性成像肝脏硬度检测(LSM)可作为早期门脉高压的无创筛查工具。有研究指出,当LSM大于20 kpa时,诊断门脉高压的特异度为92.3%;当LSM大于13 kpa时,诊断门脉高压的敏感度为94%[10]。通过脾脏大小与血小板比值联合LSM时,诊断门脉高压的敏感度和特异度可同时超过80%[11]。超声弹性成像测量肝脾硬度也可协助非肝硬化性门脉高压的病因诊断,在特发性门脉高压症患者,LSM一般轻度升高,与门脉高压的表现不符,而脾脏硬度(SSM)与门脉压力升高相一致,从LSM与SSM的比值可以协助鉴别特发性门脉高压与隐源性肝硬化[12]。
门脉高压的CT和MRI表现征象包括门脉主干增粗或扩张,侧枝血管扩张扭曲,平扫期可以为团状或结节状软组织影,脾肿大、腹水、脾肾分流或胃肾分流形成。门脉系统血管CTV可评估门脉高压的严重程度,血管重建可视化门脉系统血管及其侧支血管走向、分布情况,根据侧支循环部位的多少和范围的大小、曲张血管的程度初步预测门脉高压的严重程度;CTV可以明确食管胃静脉曲张腔外血管形态,评估内镜治疗的危险分级和出血风险,准确判断门体分流情况,为内镜治疗和介入治疗选择提供个体化诊疗指导和随访依据。
2.4 内镜检查 与肝硬化门脉高压食管胃静脉曲张多为GOV I型或II型略有不同,特发性门脉高压引起的静脉曲张以孤立型的胃静脉曲张更为常见,且可能存在十二指肠等异位曲张静脉,很少合并门脉高压性胃病。针对病因治疗是最有效的方法。在无法解除病因时,内镜下食管套扎治疗及胃组织粘合剂治疗是有效的措施。对于粗大静脉不适合内镜下治疗的患者,可以行经颈静脉门体分流术(TIPS)以降低门脉压力。
3 门脉高压的病因
门脉高压病因以肝病最为常见。由于各种原因的肝脏损伤导致肝纤维化、硬化结节形成、血管阻塞,引起门脉压力升高,占门脉高压的90%。肝病的病因东西方国家存在明显的差异,中国作为乙型肝炎和血吸虫等感染的高发区,上世纪大量感染乙型肝炎病毒和血吸虫的患者,成为我国肝硬化门脉高压的主要人群。但是,近年来,我国肝病的病因也逐渐发生变化,血吸虫病导致的肝硬化患者显著减少,由于药物和疫苗接种,使乙型肝炎肝硬化也明显下降,而药物性、酒精性、自身免疫性、胆汁淤积性、非酒精性脂肪性肝炎等引起的肝硬化患者开始增多。自2000年开始,国内外对非酒精性脂肪肝的关注增多,越来越多证据表明,之前的隐源性肝硬化大部分是由于非酒精性脂肪性肝炎引起的[13]。特发性门脉高压是门脉高压的少见情况,这类患者不伴随肝脏组织学病变或者门脉阻塞,其发病原因尚不明确,可能与慢性感染、免疫异常和基因遗传等有关。
非肝硬化门脉高压包括肝前和肝后问题。肝前性门脉高压包括门静脉血栓形成、肝外门静脉阻塞、先天性血管畸形、骨髓增殖性疾病导致的血液流量增加等原因;肝后性门脉高压包括肝内小静脉闭锁、肝静脉阻塞、肝静脉下腔静脉阻塞(布加综合征)、缩窄性心包炎、长期右心功能不全导致的慢性淤血肝病性门脉高压等需要注意鉴别,诊断较为困难。明确病因,针对病因进行治疗是减缓门脉高压进展的关键,同时对患者的治疗措施选择有重要的指导价值。
影像学检查可以用于门脉高压的病因诊断。肝炎肝硬化门脉高压患者影像学表现以肝内血流动力学障碍为基础,肝内有多种性质的结节,肝脏形态和轮廓改变,各叶比例失调,局部肝叶萎缩、左叶和尾叶代偿性增大。通过MRI检查可以鉴别肝硬化结节的良恶性。增强CT上可表现为血管床缩小、闭塞或扭曲、血管受到再生结节挤压、肝内门静脉、肝静脉和肝动脉小支三者间失去正常的关系。血吸虫病性肝硬化的影像学表现可以看到血吸虫虫卵沉积在汇管区门静脉小分支内,周围可出现肉芽肿性反应,门脉小分支管腔变窄,血流受阻,肝脏可出现线状、网状、蟹足状、地图状钙化,汇管区扩大伴门脉分支扭曲扩张,门脉血管壁、结直肠壁钙化增厚。对于非肝硬化性门脉血栓引起的肝前性门脉高压,CT片上可以看到门脉血管充盈缺损及门脉海绵样变形成。胰源性门脉高压患者是由于脾静脉向门静脉回流受阻引起的,在门脉血管CTV可以表现为脾门处曲张静脉,胃后-胃短静脉及胃网膜静脉增粗迂曲,胃底胃体静脉曲张,很少出现食管静脉曲张。脾脏由于淤血可以增大,但是肝脏的形态大小一般无异常。Buddi-Chiari综合征是由于肝静脉先天发育异常,肝静脉血栓性疾病,肿瘤压迫等引起下腔静脉肝段和肝静脉阻塞,CTV门脉期可看到下腔静脉、肝静脉狭窄、梗阻或栓塞;肝脏尾叶增大,以尾叶为中心的区域强化明显,肝外周区域强化下降,延迟强化和分布不均,肝内外侧支血管开放形成,肝内可见强化增生结节。
肝穿刺活检病理学检查是肝硬化门脉高压病因诊断的金标准。随着影像学技术的进步、血清学标志物的发展,越来越多的患者可以通过无创检测明确门脉高压的病因并评估病情进展。接受肝穿刺活检的患者在近10年里显著下降[14,15]。通过血清病毒标记物、自身抗体等实验室检测及超声和CT等影像学检查等,结合患者的既往病史,包括饮酒史、输血史、药物服用史、疫区接触史、肥胖等,可明确大部分患者的病因。对于无法明确门脉高压病因的,通过肝穿刺活检病理学检查仍然是必要的,非肝硬化门脉高压通过肝穿刺病理学检查也能从中获得有诊断价值的信息。
当患者出现脾功能亢进症、食管胃静脉曲张、腹水等临床表现,需高度怀疑有门脉高压症。通过实验室检查、肝脏硬度、CTV、胃镜和HVPG等检查明确门脉压力和门脉高压病因。对于以上检查仍不能明确病因的患者可考虑行肝穿刺(图2)。本文介绍的这例门脉高压患者,在排除了肝硬化性门脉高压症后,考虑为非肝硬化PHT,最终接受了TIPS治疗后病情好转。
【参考文献】
[1]Procope B,Tantau M,Bureau C.Are there any alternative methods to hepatic venous pressure gradient in portal hypertension assessment.J Gastrointest Liver Dis,2013,22(1):73.
[2]Garcia-Tsao G,Abraldes JG,Berzigotti A,et al.Portal hypertensive bleeding in cirrhosis:Risk stratification,diagnosis,and management:2016 practice guidance by the American Association for the study of liver diseases. Hepatology,2017,65(1):310-335.
[3]Hillaire S,Bonte E,Denninger MH,et al.Idiopathic non-cirrhotic intrahepatic portal hypertension in the West:a re-evaluation in 28 patients.Gut,2002,51(2):275-280.
[4]De BK,Sen S,Sanyal R.Hepatopulmonary syndrome in noncirrhotic portal hypertension.Ann Intern Med,2000,132(11):924.
[5]O’shea RS,Dasarathy S,McUllough AJ,et al.Alcoholic liver disease.Hepatology(Baltimore,Md.),2010,51(1):307-328.
[6]Feld JJ,Hussain N,Wright EC,et al.Hepatic involvement and portal hyper-tension predict mortality in chronic granulomatous disease.Gastroenterology,2008,134:1917-1926.
[7]Salkic NN,Jovanovic P,Hauser G,et al.FibroTest/Fibrosure for significant liver fibrosis and cirrhosis in chronic hepatitis B:a meta-analysis.Am J Gastroenterol,2014,109(6):796.
[8]Buck M,Garcia-Tsao G,Groszmann RJ,et al.Novel inflammatory biomarkers of portal pressure in compensated cirrhosis patients.Hepatology,2014,59(3):1052-1059.
[9]Berzigotti A,Piscaglia F.Ultrasound in portal hypertension-Part 1.Ultraschall Med,2011,32:548-571.
[10]Augustin S,Millán L,González A,et al.Detection of early portalhypertension with routinedataand liverstiffnessin patients with asymptomatic liver disease:a prospective study.J Hepatol,2014,60(3):561-569.
[11]Berzigotti A,Seijo S,Arena U,et al.Elastography,spleen size,and platelet count identify portal hypertension in patients with compensated cirrhosis.Gastroenterology,2013,144(1):102.
[12]Berzigotti A.Non-invasive evaluation of portal hypertension using ultrasound elastography.J Hepatol,2017,67(2):399.
[13]Caldwell S,Marchesini G.Cryptogenic vs NASH-cirrhosis:The rose exists well before its name.J Hepatology,2017[ahead of print].
[14]Procopet B,Berzigotti A.Diagnosis of cirrhosis and portal hypertension:imaging,non-invasivemarkersoffibrosisand liver biopsy.Gastroenterol Rep,2017,5(2):79-89.
[15]Ponziani FR,Gasbarrini A,Pompili M.Use of liver imaging and biopsy in clinical practice.New Engl J Med,2017,377(8):756.

