miR-381-3p通过BDNF减轻抑郁症大鼠海马区细胞损伤
雷 娜, 张学平, 王 创
(杭州市第七人民医院精神科, 浙江 杭州 310013)
抑郁症(depression)是一种常见慢性神经性疾病,临床常表现有情绪低落、行为缺乏主动和思维迟缓等症状。若长期得不到治疗或改善,将影响患者的生命以及增加家庭负担[1]。内分泌系统紊乱,致使皮质醇水平上升,引起神经细胞损伤,是抑郁症患者的一个重要病理特征[2-3]。因此,保护神经细胞免受损伤是抑郁症治疗的一个重要方向。
随着神经生物学和分子生物学的发展,研究者们发现通过调控一些神经保护相关基因可以保护神经细胞免受损伤[4-5]。既往研究表明,脑源性神经营养因子(brain-derived neurotrophic factor,BDNF)表达减少与抑郁症发生有关[6]。接受抗抑郁症治疗可以增加BDNF表达,所以调控BDNF表达可以成为抗抑郁症的潜在治疗靶点[7-8]。BDNF是一个受多种微小RNA(microRNA, miRNA, miR)调控的分子。Sun等[9]发现miR-206过表达通过靶向BDNF减轻了大黄素的神经疼痛; Li等[11]发现miR-613可以通过调节小鼠海马区BDNF表达参与阿尔茨海默病的发生过程。已有研究表明,miR-381-3p是一个抑癌分子,其过表达可以抑制肿瘤细胞增殖[11],而且miR-381-3p还可以调控神经干细胞的增殖和分化过程[12],提示miR-381-3p在调控细胞生长中的关键作用。但miR-381-3p是否参与抑郁症发生过程,以及是否可以通过调控抑郁症大鼠海马神经元(hippocampal neurons)中BDNF表达保护神经元免受损伤尚未可知。因此本研究通过建立大鼠皮质酮(corticoste-rone,CORT)抑郁症模型,观察miR-381-3p和BDNF在氟西汀(fluoxetine)治疗抑郁症过程的表达变化,并进一步通过建立miR-381-3p沉默的新生大鼠海马神经元细胞株,观察沉默miR-381-3p对海马神经元活力及BNDF表达的影响。
材 料 和 方 法
1 主要材料及试剂
成年雄性Sprague-Dawley (SD)大鼠,体重160~200 g,购自上海实验动物研究中心;CORT、氟西汀和二甲基亚砜(dimethyl sulfoxide,DMSO)购自Sigma, CORT和氟西汀分别溶于0.1% DMSO,皮下注射时用0.1% Tween-80生理盐水稀释, CORT用于细胞培养时,用DMEM培养基(上海百赛生物技术有限公司)稀释;抗BDNF、Bcl-2和Bax抗体购自Abcam;PC12细胞来源于大鼠肾上腺髓质嗜铬细胞瘤克隆的细胞株,从结构和功能上类似于神经元,是研究神经元较为理想的细胞模型,购自上海生命科学院细胞库;HEK293T细胞购自上海生命科学院细胞库;去甲肾上腺素(norepinephrine,NE)ELISA试剂盒购自R&D; miR-381-3p inhibitor购自上海吉玛公司。
2 方法
2.1动物实验分组 35只SD大鼠随机分成4组:对照(control,n=10)组、造模(model,n=10)组、治疗(treatment,n=10)组和氟西汀(fluoxetine,n=5)组。造模组以CORT按40 mg/kg剂量对大鼠进行皮下注射,持续24 d;治疗组大鼠前12 d按40 mg/kg剂量皮下注射CORT,后12 d在皮下注射CORT前按5 mg/kg剂量腹腔注射氟西汀;氟西汀组大鼠前12 d注射等体积生理盐水,后12 d按5 mg/kg剂量腹腔注射氟西汀;对照组注射等体积生理盐水。
2.2抑郁症评估 (1)体重测定:造模前以及造模后第6、12、18和24天称取大鼠体重;(2)旷场试验:造模后第24天行旷场试验观察大鼠水平运动,4只脚水平跨过计算为1次,每5 min累积一次;(3)NE水平检测:造模后第24天,取大鼠的血清和海马组织,利用ELISA试剂盒检测NE含量。
2.3细胞培养 (1)新生大鼠海马神经元培养:对新生大鼠进行消毒、大脑半球暴露处理,分开皮层取两侧海马组织,剪成1 mm×1 mm×1 mm小块后用胰蛋白酶消化,当组织块消失后加入胎牛血清终止消化并离心出细胞,获得的细胞沉淀用DMEM培养基悬浮培养; (2)PC12细胞培养:PC12细胞培养在DMEM细胞培养基中; (3)HEK293T细胞培养:HEK293T细胞培养在DMEM细胞培养基中。所有细胞放置细胞培养箱,于37 °C、5% CO2、湿化条件下培养,隔天更换新鲜培养基。
2.4miR-381-3p inhibitor转染 将新生大鼠海马神经元接种至6孔板上继续培养,待细胞长至80%融合时,使用Lipofectamine 2000转染试剂盒,将miR-381-3p inhibitor或者阴性对照序列(miRNA-NC)转染至神经元细胞中。转染24 h后,收集细胞进行下一步实验。
2.5MTT法检测细胞活力 已转染miR-381-3p inhibitor的海马神经元在含CORT的DMEM培养基中继续培养24 h,进行MTT检测。移去含CORT的DMEM培养基,加入含MTT的DMEM培养基继续培养4 h;孵育结束后,利用DMSO溶解甲臜结晶;溶解结束后,在570 nm处检测各样本的吸光度(A)值。
2.6Real-time PCR检测miR-381-3p和BDNF mRNA的表达 利用Trizol试剂分别提取海马组织和海马神经元中的总RNA, 反转录成cDNA,进行real-time PCR反应;miR-381-3p的表达量以U6为内参照,BDNF mRNA的表达量以β-actin为内参照,表达量计算均按照2-ΔΔCt法。
2.7Western blot检测BDNF、Bcl-2和Bax的蛋白表达 利用RIPA细胞裂解液提取各组大鼠海马组织以及细胞中总蛋白,BCA法定量总蛋白后,取等量各组样本进行10% SDS-PAGE;将凝胶上的蛋白转膜至PVDF膜;对膜先进行2 h的封闭,再孵育I抗于4 °C条件过夜;第2天取出膜于室温下孵育辣根过氧化物酶标记的II抗;蛋白条带通过ECL化学发光剂显示、拍照。
2.8萤光素酶报告基因分析 根据生物信息学软件预测BDNF启动子上miR-381-3p的结合位点,PCR扩增靶启动子片段,插入萤光素酶报告基因质粒中,构建pGL3-BDNF 3’-UTR萤光素酶基因报告载体;PC12细胞和HEK293T细胞分别接种至24孔板上,待生长至80%融合,共转染miR-381-3p和pGL3-BDNF 3’-UTR萤光素酶载体;转染24 h后,检测萤光素酶活性。
3 统计学处理
所有数据均采用SPSS 16.0软件进行统计学分析。数据以均数±标准差(mean±SD)表示。组间比较采用单因素方差分析。以P<0.05为差异有统计学意义。
结 果
1 氟西汀对抑郁症大鼠的治疗效果
抑郁症大鼠造模成功的指标是体重下降、旷场活动次数减少及去甲肾上腺素水平下降。与模型组相比,治疗组大鼠体重逐渐恢复,在治疗的第7天(即造模后第18天)显著增加并持续到治疗后第13天,见图1;治疗第24天,治疗组大鼠水平活动次数显著增加,血清和海马区域NE含量均显著增加(P<0.01),见图2、3。
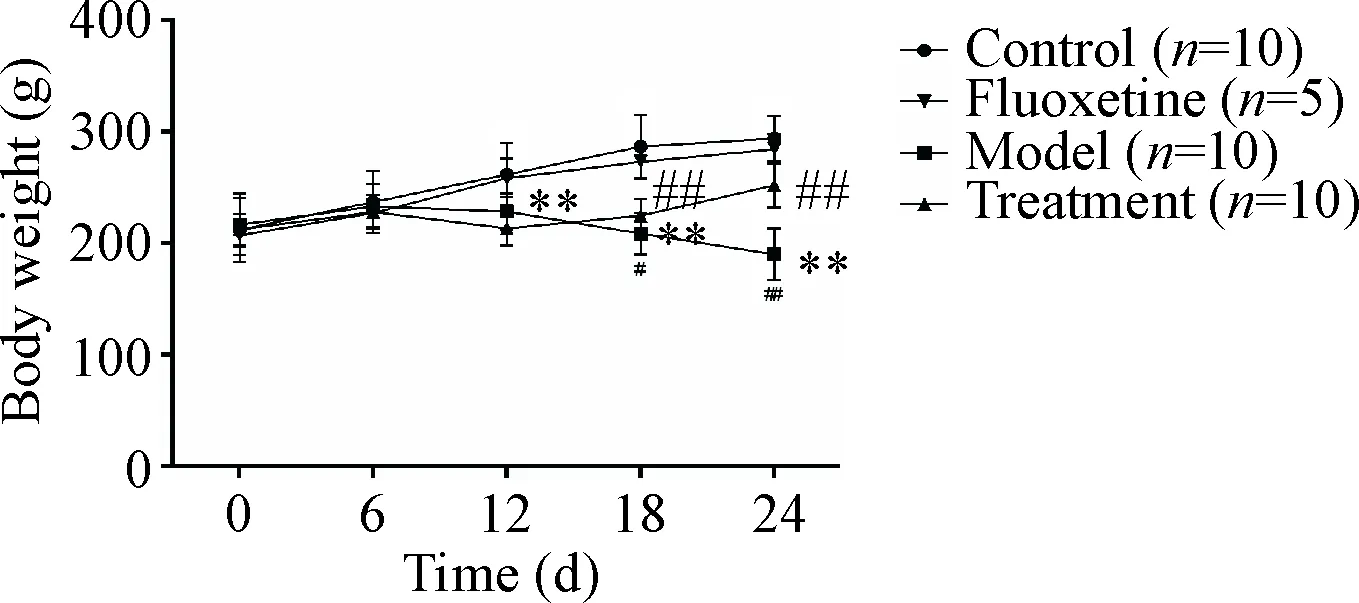
Figure 1. The changes of body weight in the rats. Mean±SD.**P<0.01vscontrol group;#P<0.05,##P<0.01vsmodel group.
图1大鼠体重的变化
2 海马组织分子表达情况
与对照组相比,模型组大鼠海马组织miR-381-3p表达显著增加,BDNF的 mRNA及蛋白水平显著下降,凋亡抑制因子Bcl-2蛋白表达下调,凋亡促进因子Bax蛋白表达上调(P<0.01);与模型组相比,治疗组海马组织miR-381-3p表达显著下调,BDNF的mRNA及蛋白水平显著上升,Bcl-2蛋白表达上调,Bax蛋白表达下调(P<0.01),见图4、5。
3 沉默miR-381-3p对海马神经元活力的影响
CORT处理可促使海马神经元活力显著下降;而CORT对神经元的毒性可被miR-381-3p沉默逆转,促进细胞活力增强(P<0.01),见图6。
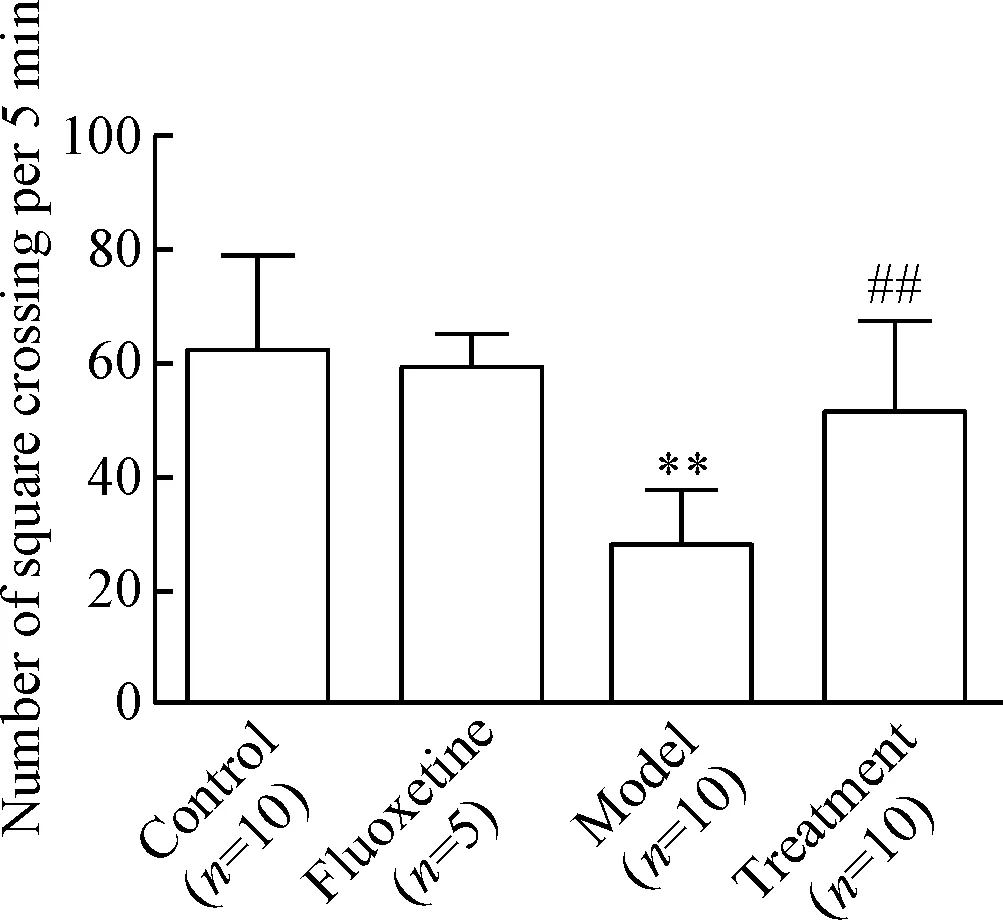
Figure 2. The number of cross-field activities. Mean±SD.**P< 0.01vscontrol group;##P<0.01vsmodel group.
图2大鼠旷场试验水平活动次数的比较

Figure 3. The content of norepinephrine (NE). Mean±SD.**P<0.01vscontrol group;##P<0.01vsmodel group.
图3NE含量的变化

Figure 4. The expression of BNDF mRNA and miR-381-3p in the hippocampus. Mean±SD.n=3.**P<0.01vscontrol group;##P<0.01vsmodel group.
图4海马组织miR-381-3p和BDNFmRNA的表达
4 沉默miR-381-3p对海马神经元中BDNF、Bcl-2及Bax表达的影响
CORT处理可促使海马神经元中miR-381-3p表达显著上调,BDNF mRNA水平显著下调;而CORT对miR-381-3p和BDNF mRNA表达的影响可被miR-381-3p沉默所逆转,促使miR-381-3p表达显著下降,BDNF的mRNA水平显著上调(P<0.01),见图7。

Figure 5. The protein expression of BNDF, Bcl-2 and Bax in the hippocampus. Mean±SD.n=3.**P<0.01vscontrol group;
##P<0.01vsmodel group.
图5海马组织BDNF、Bcl-2和Bax的蛋白表达
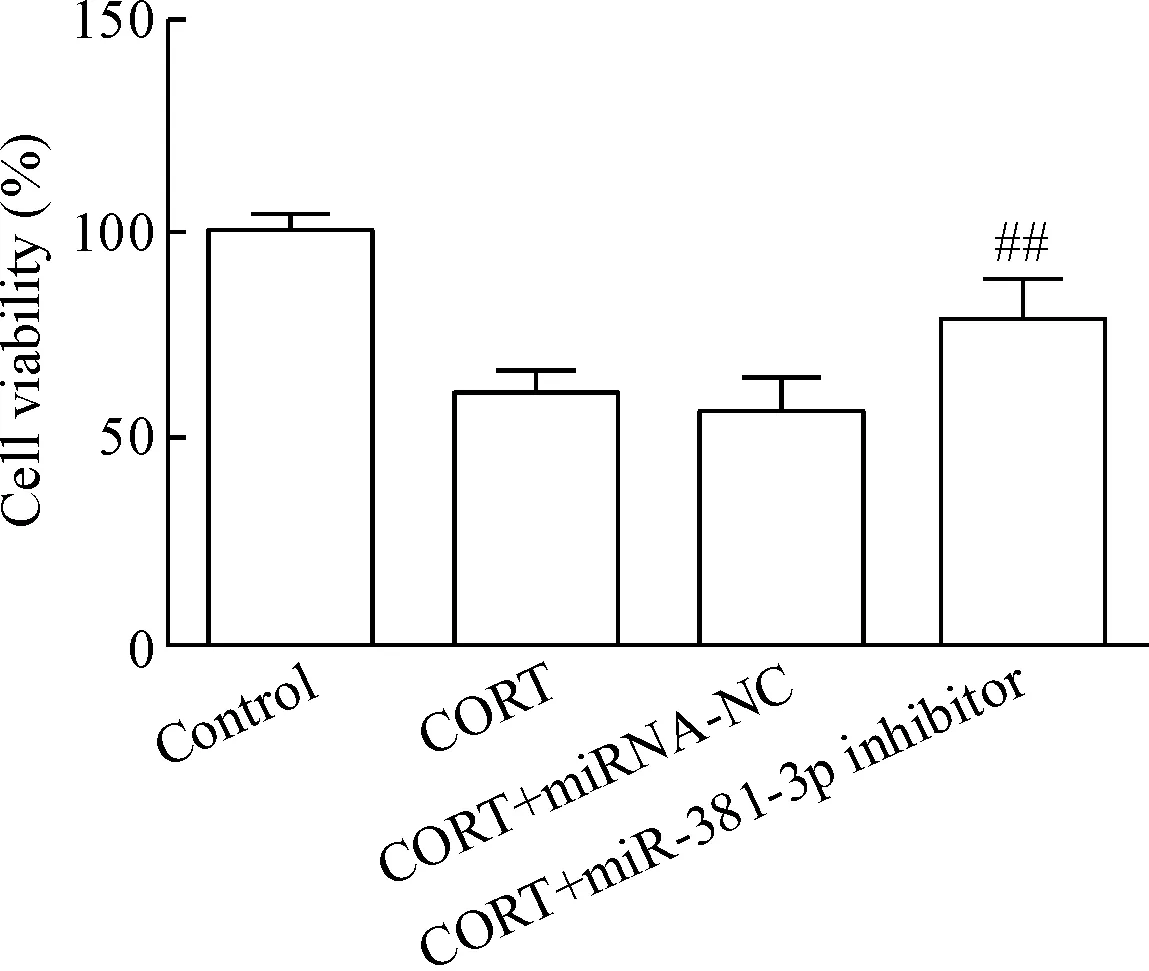
Figure 6. The viability of hippocampal neurons. Mean±SD.n=3.**P<0.01vscontrol group;##P<0.01vsCORT+miRNA-NC group.
图6细胞活力的检测
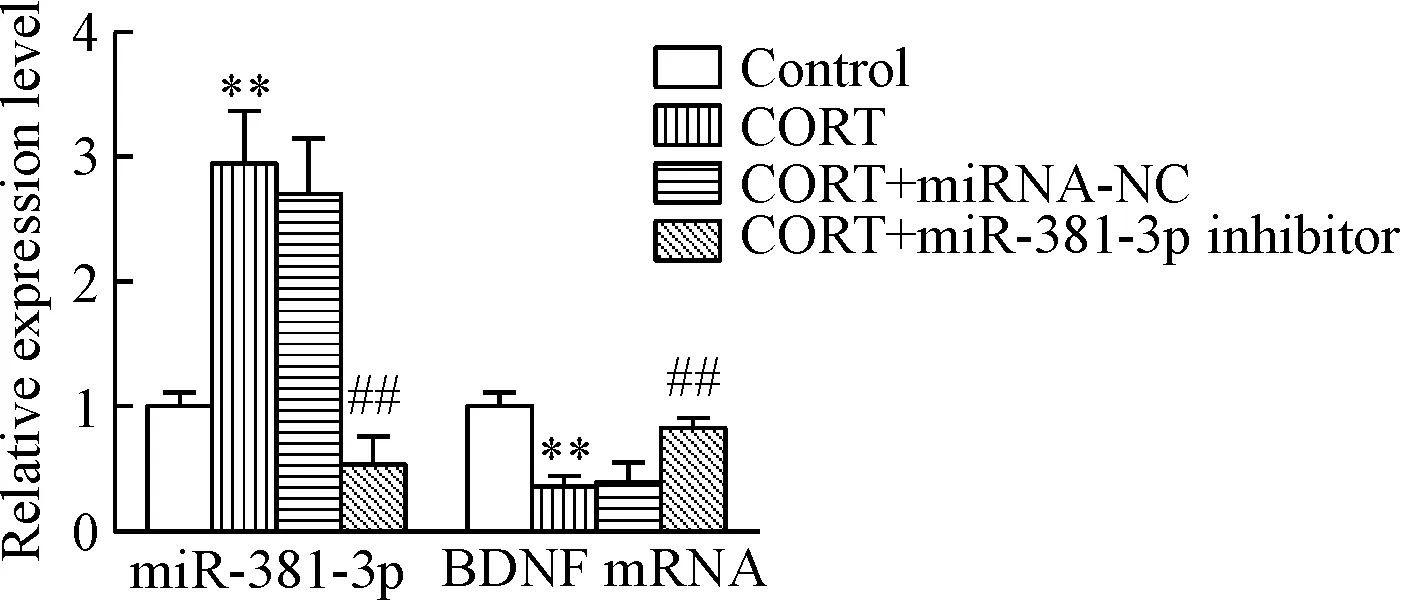
Figure 7. The expression of miR-381-3p and BDNF mRNA in the hippocampal neurons. Mean±SD.n=3.**P<0.01vscontrol group;##P<0.01vsCORT+miRNA-NC group.
图7沉默miR-381-3p对海马神经元中miR-381-3p和BDNFmRNA表达的影响
同时,miR-381-3p沉默逆转了CORT对BDNF、Bcl-2和Bax蛋白表达的影响,促进了BDNF和Bcl-2的表达,抑制了Bax的表达(P<0.01),见图8。
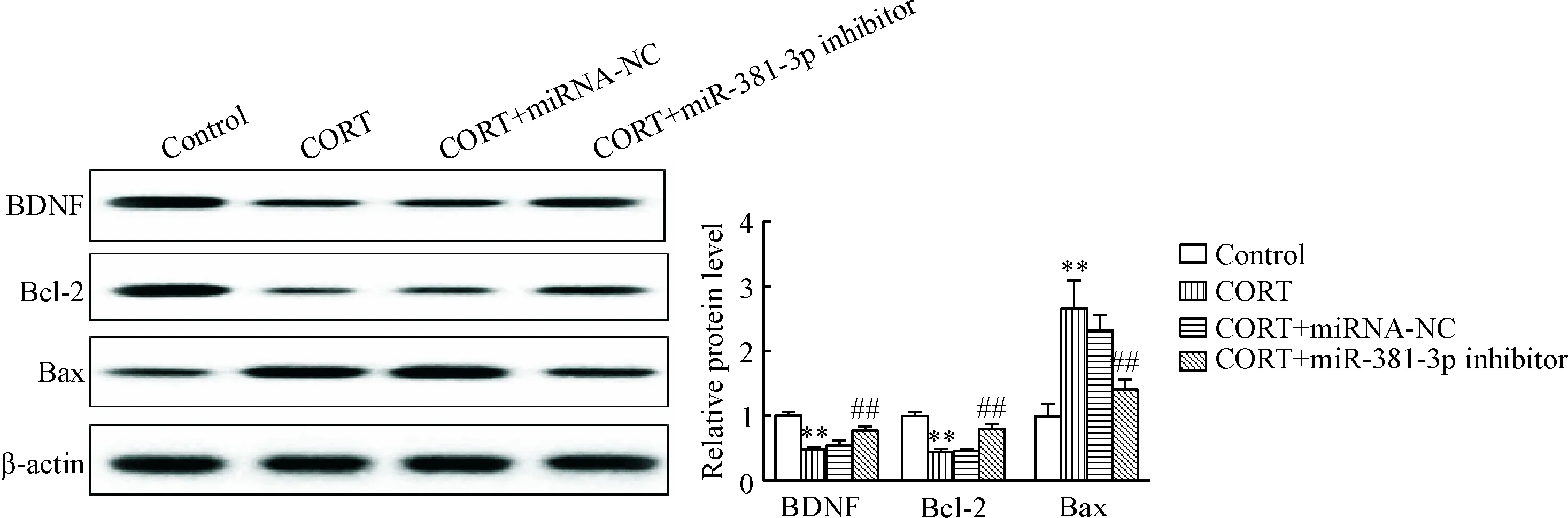
Figure 8. The protein expression of BDNP, Bcl-2 and Bax in the hippocampal neurons. Mean±SD.n=3.**P<0.01vscontrol group;##P<0.01vsCORT+miRNA-NC group.
图8沉默miR-381-3p的海马神经元中BDNF、Bcl-2和Bax的蛋白表达
5 miR-381-3p靶向BDNF的验证
miR-381-3p与BDNF 3’-UTR区有潜在配对序列区域。萤光素酶报告基因结果显示,miR-381-3p抑制BDNF转录活性,见图9。
讨 论
抑郁症一种严重影响患者生命、增加家庭负担的慢性神经精神障碍类疾病。目前临床抑郁症治疗效果仍不理想,药物治疗代替电休克治疗方法为患者带来福音,但药物产生的毒副作用对患者造成不良后果。因此,从探讨抑郁症发生机制出发,寻找抗抑郁症的新的治疗靶点显得尤为重要。从逆转神经元损伤角度改善抑郁症症状的方法已有研究,有望成为一个安全有效的治疗策略。分子生物学和生物信息学的发展为疾病治疗提供的一个新的研究方向。探讨疾病发生的机制,寻找有效的治疗基因靶点,具有疾病治疗的潜在意义。通过敲除靶基因调控基因表达的方法,在调控心血管疾病、肿瘤和脑部疾病发生过程中的作用已有大量研究[13-15]。本研究探讨miR-381-3p和其靶向调控的BDNF在改善大鼠抑郁症中的作用,发现沉默miR-381-3p可减轻大鼠海马神经元的CORT损伤。
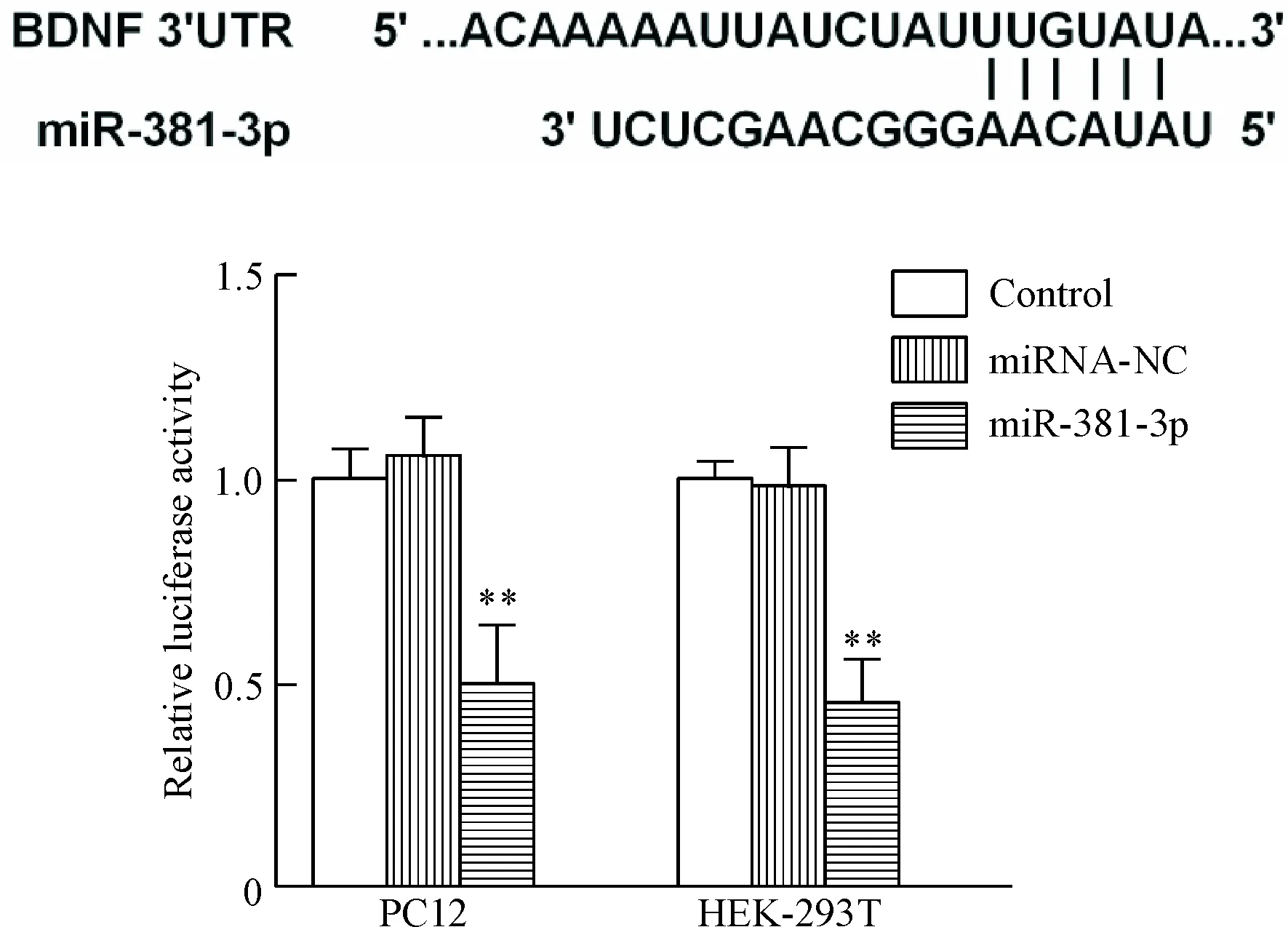
Figure 9. miR-381-3p targeted regulation of BNDF expression. Mean±SD.n=3.**P<0.01vscontrol group.
图9萤光素酶报告基因法验证miR-381-3p靶向调控BDNF
既往研究发现miR-381-3p是一个肿瘤相关miRNA分子。在调控肿瘤细胞增殖、生长和侵袭中起重要作用。另外,研究发现miR-381-3p在调控神经干细胞增殖和分化方面也发挥作用。我们的结果发现,在氟西汀治疗抑郁症大鼠的海马区组织中,miR-381-3p表达显著受到抑制,表明miR-381-3p可能与抑郁症发生以及治疗有关。氟西汀是临床抑郁症常用药物,可以通过增加突触间隙中单胺类神经递质含量改善抑郁症的指征[16]。近期研究发现氟西汀能减轻各种有害因素对神经细胞的损害作用,也保护神经元免受CORT毒性[3, 5]。那么,我们在氟西汀治疗组发现的受氟西汀抑制表达的miR-381-3p是否参与抑郁症大鼠海马神经元免受CORT损伤过程仍需进一步验证。因此,我们培养了新生大鼠海马神经元,并沉默细胞中miR-381-3p,观察其对CORT处理后的神经元活力的影响。我们发现miR-381-3p沉默逆转了CORT的效应,增加的细胞存活率,同时促进了凋亡抑制蛋白Bcl-2表达并抑制了凋亡促进蛋白Bax的表达。这些结果表明沉默miR-381-3p在保护海马神经元、减轻抑郁症损伤中起了关键作用。
另外,我们还发现BDNF是miR-381-3p靶向调控分子。BDNF是一个神经损伤和修复相关的分子,在抑郁症病理生理发生过程中起至关重要的作用。BDNF信号通路在抑郁症大鼠海马区水平下调,而这种下调可被抗抑郁症药物氟西汀逆转[17]。BDNF基因敲除小鼠表现出对轻度应激的易感性[18]。而接受侧脑室BDNF治疗的大鼠表现长时间持续的抗抑郁效果[19]。鉴于此,靶向调控BDNF有可能成为抗抑郁症治疗途径。本研究发现在神经元CORT毒性实验中,BDNF可被miR-381-3p靶向调控。
综上所述,在氟西汀治疗CORT-抑郁症大鼠过程中可促使miR-381-3p/BDNF通路受抑制。miR-381-3p沉默可通过促进BDNF表达保护神经元,减轻CORT对神经元的损伤。miR-381-3p有可能成为抗抑郁症治疗的潜在靶点。
[参考文献]
[1] 张绘宇, 赵玉男, 王中立. 慢性皮质酮注射对小鼠抑郁样行为及脑糖原水平的影响[J]. 中国病理生理杂志, 2015, 31(5):828-833.
[2] Anacker C, Zunszain PA, Carvalho LA, et al. The glucocorticoid receptor: pivot of depression and of antidepressant treatment?[J]. Psychoneuroendocrinology, 2011, 36(3):415-425.
[3] Freitas AE, Egea J, Buendía I, et al. Agmatine induces Nrf2 and protects against corticosterone effects in hip-pocampal neuronal cell line[J]. Mol Neurobiol, 2015, 51(3):1504-1519.
[4] Mamdani F, Rollins B, Morgan L, et al. Variable telomere length across post-mortem human brain regions and specific reduction in the hippocampus of major depressive disorder[J]. Transl Psychiatry, 2015, 5:e636.
[5] Zeng B, Li Y, Niu B, et al. Involvement of PI3K/Akt/FoxO3a and PKA/CREB signaling pathways in the protective effect of fluoxetine against corticosterone-induced cytotoxicity in PC12 cells[J]. J Mol Neurosci, 2016, 59(4):567-578.
[6] Salehi I, Hosseini SM, Haghighi M, et al. Electroconvulsive therapy (ECT) and aerobic exercise training (AET) increased plasma BDNF and ameliorated depressive symptoms in patients suffering from major depressive disorder[J]. J Psychiatr Res, 2016, 76:1-8.
[7] Rocha RB, Dondossola ER, Grande AJ, et al. Increased BDNF levels after electroconvulsive therapy in patients with major depressive disorder: a meta-analysis study[J]. J Psychiatr Res, 2016, 83:47-53.
[8] Jiang B, Wang YJ, Wang H, et al. Antidepressant-like effects of fenofibrate in mice via the hippocampal brain-derived neurotrophic factor signalling pathway[J]. Br J Pharmacol, 2017, 174(2):177-194.
[9] Sun W, Zhang L, Li R. Overexpression of miR-206 ame-liorates chronic constriction injury-induced neuropathic pain in rats via the MEK/ERK pathway by targeting brain-derived neurotrophic factor[J]. Neurosci Lett, 2017, 646:68-74.
[10] Li W, Li X, Xin X, et al. MicroRNA-613 regulates the expression of brain-derived neurotrophic factor in Alzheimer's disease[J]. Biosci Trends, 2016, 10(5):372-377.
[11] Xue Y, Xu W, Zhao W, et al. miR-381 inhibited breast cancer cells proliferation, epithelial-to-mesenchymal transition and metastasis by targeting CXCR4[J]. Biomed Pharmacother, 2016, 86:426-433.
[12] Shi X, Yan C, Liu B, et al. miR-381 Regulates neural stem cell proliferation and differentiation via regulating Hes1 expression[J]. PLoS One, 2015, 10(10):e0138973.
[13] Zong Y, Wu P, Nai C, et al. Effect of microRNA-30e on the behavior of vascular smooth muscle cells via targeting ubiquitin-conjugating enzyme E2I[J]. Circ J, 2017, 81(4):567-576.
[14] Wang XL, Shi WP, Shi HC, et al. Knockdown of TRIM65 inhibits lung cancer cell proliferation, migration and invasion: a therapeutic target in human lung cancer[J]. Oncotarget, 2016, 7(49):81527-81540.
[15] Yadav S, Gandham SK, Panicucci R, et al. Intranasal brain delivery of cationic nanoemulsion-encapsulated TNFα siRNA in prevention of experimental neuroinflammation[J]. Nanomedicine, 2016, 12(4):987-1002.
[16] Ventura-Juncá R, Symon A, López P, et al. Relationship of cortisol levels and genetic polymorphisms to antidepressant response to placebo and fluoxetine in patients with major depressive disorder: a prospective study[J]. BMC Psychiatry, 2014, 14:220.
[17] Razzoli M, Domenici E, Carboni L, et al. A role for BDNF/TrkB signaling in behavioral and physiological consequences of social defeat stress[J]. Genes Brain Behav, 2011, 10(4):424-433.
[18] Advani T, Koek W, Hensler JG. Gender differences in the enhanced vulnerability of BDNF+/-mice to mild stress[J]. Int J Neuropsychopharmacol, 2009, 12(5):583-588.
[19] Hoshaw BA, Malberg JE, Lucki I. Central administration of IGF-I and BDNF leads to long-lasting antidepressant-like effects[J]. Brain Res, 2005, 1037(1-2):204-208.

